
1.1. Основные достижения биотехнологии
Быстрый рост народонаселения земного шара вызывает необходимость дальнейшего увеличения производства продуктов питания. Так, за последние сто лет население планеты возросло с 1,5 до 6 млрд (к 2020 г. оно составит 8 млрд). Хотя за прошедшие 40 лет производство продуктов питания увеличилось в 2,5 раза, дальнейшее значительное улучшение маловероятно. Интенсификация сельскохозяйственного производства с использованием традиционных методов (селекция пород животных и сортов растений, химизация, мелиорация и т.д.) в большинстве случаев достигла своего предела. Кроме того, существующие сельскохозяйственные технологии не являются возобновляемыми: в течение всего лишь 20 последних лет мы потеряли более 15% плодородного почвенного слоя, а используемые природные источники энергии также небезграничны. Наконец, большая часть пригодных к возделыванию почв уже вовлечена в сельскохозяйственное производство. Все это привело к возникновению ряда экономических и экологических проблем, связанных с загрязнением окружающей среды, истощением энергетических ресурсов, возрастанием затрат на единицу продукции и т.д. Необходим поиск новых подходов, которые в дальнейшем позволили бы повысить урожаи и улучшить качество основных сельскохозяйственных культур, но были бы экономичны в производстве и не наносили вреда окружающей среде. Одним из таких подходов является биотехнология.
Биотехнология - наука, создающая теоретические предпосылки для разработки способов и схем получения практически ценных веществ и процессов на основе культивирования микроорганизмов, а также свободно растущих клеток многоклеточных организмов (растений и животных).
Биотехнология - это интегральная по своей природе область науки и техники, которая опирается на теоретические и методические положения микробиологии и биохимии, молекулярной биологии и генетики, физиологии и цитологии, а также использует прогрессивные химические технологии. В таком ее понимании биотехнология занимается теми процессами, которые можно вести не в природе, а в искусственно созданных условиях биохимического производства, то есть круглогодично и повсеместно, независимо от сезона, климатических, погодных и географических условий.
Существенное внимание уделяется оптимизации конкретных биотехнологий, направленному изменению процессов для достижения максимального выхода целевого продукта. Именно эти положения принципиально отличают биотехнологию от сельскохозяйственной науки, где климатические и другие природные условия являются самым мощным фактором, препятствующим созданию стабильных долгосрочных технологий, и существенно ограничивают возможности научного прогнозирования и управления (Глеба, 2000).
Функцию биотехнологии можно охарактеризовать как целенаправленное превращение материи и энергии с помощью организмов или продуктов их жизнедеятельности. |
По существу, биотехнология использует методы живой природы. Можно назвать первым биотехнологом того, кто впервые собрал и посеял зерна растений, чтобы получить продукцию, полезную для человека. Аналогично и с разведением животных. Поэтому сельское хозяйство - важнейшая отрасль, где используют методы биотехнологии.
Получая многие продукты питания, например, хлеб, вино, квашеную капусту, уксус, человек сначала не подозревал, что в этих технологиях используются микроорганизмы, пока их роль не была продемонстрирована Луи Пастером. В последующем с помощью микроорганизмов научились получать разнообразные органические вещества: спирт, ацетон, белки, аминокислоты, витамины. Специализированные микроорганизмы осуществляют также гидролиз отходов растениеводства и животноводства и могут давать при этом дешевое топливо - биогаз, в основном состоящий из метана. В свою очередь, другие микроорганизмы могут использовать метан в качестве источника питания, в результате чего получают кормовой белок.
Важную роль играют микроорганизмы в очистке вод от отходов молочной и целлюлозно-бумажной промышленности. Микробы разлагают и выводят из окружающей среды различные пластмассы, моющие средства, помогают избавиться от загрязнения почвы и воды нефтью, пестицидами. Микроорганизмы эффективно используются для рекультивации земель, особенно отвалов горно-рудных предприятий. Они восстанавливают структуру почвы, помогая растениям извлекать труднодоступные формы фосфора и других питательных элементов.
Биотехнологию рассматривают в двух аспектах: традиционном (классическом) и современном. В традиционном смысле биотехнологию определяют как науку о методах и технологиях производства, хранения и переработки продукции с использованием обычных (нетрансгенных) растений, животных и микроорганизмов. К новейшей биотехнологии относят науку о генно-инженерных и клеточных методах и технологиях создания генетически трансформированных организмов с целью получения новых видов продуктов.
Генная инженерия появилась после расшифровки молекулярной структуры гена. Методы генной инженерии основаны на активации или вставке отдельных генов в геном организма (разрезании и сшивании фрагментов ДНК). В данном случае самыми распространенными объектами являются микроорганизмы. Уже давно замечено, что в природе микробы довольно легко обмениваются между собой генетической информацией. В первую очередь это относится к безъядерным организмам (прокариотам). Так, устойчивость к некоторым антибиотикам от обычной кишечной палочки может передаваться другим кишечным бактериям. Выяснилось, что такая устойчивость закодирована не в хромосомной ДНК бактерии, а в относительно небольших кольцевых молекулах ДНК, которые имеют свойство автономно размножаться. Они были названы плазмидами.
Плазмиды сыграли большую роль в разработке генно-инженерной технологии. Если плазмиду разрезать определенными ферментами (рестриктазами), то образуются линейные молекулы, которые можно «сшивать» с любыми другими фрагментами ДНК (генами). Так образуется новая генетическая конструкция - рекомбинантная ДНК. Такие конструкции способны вновь проникать в клетки бактерий и воспроизводиться в них. Это и есть метод клонирования генов в делящихся клетках бактерий. Его успешно используют для переноса генов, в том числе в клетки растений и животных.
Большим достижением новейшей биотехнологии явилось создание генно-инженерного инсулина. Ранее в медицине использовали животный инсулин, извлекаемый из поджелудочной железы свиньи. Это давало ряд побочных эффектов. Генно-инженерный инсулин представляет собой биотехнологический продукт. Чтобы его создать, сначала выяснили, какой участок ДНК человека отвечает за выработку данного белка (инсулина). Затем этот ген cинтезировали и поместили в клетку бактерии E. coli, которая может продуцировать инсулин в неограниченных количествах. Сейчас производством генно-инженерного инсулина занимаются фирмы США, Дании и Германии.
Биотехнология рисует перспективы воссоздания вымершего организма по остаткам молекул ДНК. Новые возможности открывает обнаружение фермента теломеразы, особенно много его в бессмертных раковых клетках. Фермент отвечает за наращивание теломеров (концов хромосом), которые укорачиваются при каждом делении клетки. Селективное ингибирование фермента помогло бы остановить развитие раковых клеток, а активирование фермента в нормальных клетках перспективно для продления жизни.
Ветвью генной инженерии является клеточная инженерия, занимающаяся конструированием клеток путем объединения органелл, несущих генетическую информацию от разных родителей. Основой клеточной инженерии служит культура клеток.
Известно, что отдельные изолированные части растений способны долго жить в воде. А если в воду добавить минеральные соли, то срок их жизни удлиняется. Отсюда возникла идея длительно выращивать отдельные ткани (клетки) растений в культуре и воспроизводить из них целое растение.
Из клеточных технологий следует отметить микроклонирование (размножение) растений. Практически из каждого растения можно выделить кусочек ткани, перенести его на питательную среду и вырастить неограниченное количество каллусных клеток. Замечено, что если брать для этого меристематические ткани (верхушки побегов и другие периферические зоны с делящимися клетками), то формирующиеся из них каллусные культуры и регенирировавшие растения свободны от вирусов. Это эффективный способ получения безвирусных растений. Правда, после высаживания в открытый грунт они через некоторое время вновь заражаются вирусами. Но первое поколение жизнеспособно и продуктивно, что важно для элитного семеноводства.
Конкретные условия микроклонирования и получения микроклубней картофеля впервые были разработаны в нашей стране во ВНИИ сельскохозяйственной биотехнологии. Сейчас это широко распространенная в сельскохозяйственном производстве технология.
Важным этапом в развитии биотехнологии явилось использование соматической гибридизации - слияния протопластов (клеток без оболочки) разных растений или внесение в протопласт ДНК из растения другого вида. Таким способом осуществляют полную комбинацию геномов двух форм или же только частичный перенос генов. Для слияния протопластов разработаны специфические методы, которые будут рассмотрены в соответствующей главе. Путем слияния протопластов созданы широко известные соматические гибриды картофеля и томатов, получившие название поматы. В данном случае на одном растении получали и “корешки” и “вершки”.
![]() Прежде чем перейти к значению биотехнологии в защите растений, нельзя не упомянуть о выдающемся открытии 1997 г. в области биотехнологии (Шотландия). Имеется в виду создание генетического дубликата овцы из одной клетки ее вымени (эпителия молочной железы).
Прежде чем перейти к значению биотехнологии в защите растений, нельзя не упомянуть о выдающемся открытии 1997 г. в области биотехнологии (Шотландия). Имеется в виду создание генетического дубликата овцы из одной клетки ее вымени (эпителия молочной железы).
Сейчас известно, что ДНК каждой клетки хранит полную информацию о целом организме, но работает лишь один ген, а остальные являются «молчащими». Ученые создали стрессовые условия, чтобы разбудить все молчащие гены в клетке, взятой из вымени. Однако чтобы пошла репликация, окружающие условия генов должны были соответствовать среде яйцеклетки. Тогда взяли яйцеклетку от другой овцы и вынули оттуда весь генетический материал - получился ооцит без ядра. После этого провели соматическую гибридизацию пустого ооцита с клеткой вымени. Гибридные клетки размножали in vitro и инъецировали (трансплантировали) третьей овце - суррогатной маме. У нее родился ягненок Долли - точная генетическая копия первой овцы, у которой была взята клетка вымени (рис. 1.1).
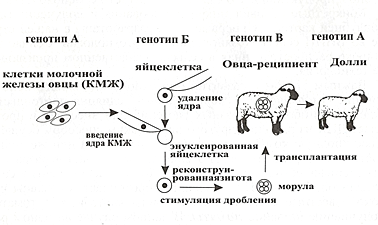
Рисунок 1.1. Схема клонирования овцы Долли
![]() Позднее были клонированы разные виды животных. Интересно отметить, что в России еще в 1987 г. в академическом журнале «Биофизика» была опубликована статья советских исследователей Л.М. Чайлахяна, Б.Н. Вепренцева, Т.Д. Свиридовой, В.А. Никитина «Электростимулируемое слияние клеток в клеточной инженерии», где подробно описаны собственные исследования авторов по реконструкции мышиных зигот сочетанием микрохирургии и электростимулируемого слияния клеток. Правда, российские ученые брали клетки для клонирования из ранних эмбрионов, а не от взрослого животного, как шотландцы. Эмбриональные клетки были уже репрограммированы самой природой. Тем не менее эксперименты советских исследователей в итоге впервые привели к появлению на свет клонированного млекопитающего - мышки. К сожалению, статью не опубликовали в международном журнале и она осталась не замеченной мировой общественностью.
Позднее были клонированы разные виды животных. Интересно отметить, что в России еще в 1987 г. в академическом журнале «Биофизика» была опубликована статья советских исследователей Л.М. Чайлахяна, Б.Н. Вепренцева, Т.Д. Свиридовой, В.А. Никитина «Электростимулируемое слияние клеток в клеточной инженерии», где подробно описаны собственные исследования авторов по реконструкции мышиных зигот сочетанием микрохирургии и электростимулируемого слияния клеток. Правда, российские ученые брали клетки для клонирования из ранних эмбрионов, а не от взрослого животного, как шотландцы. Эмбриональные клетки были уже репрограммированы самой природой. Тем не менее эксперименты советских исследователей в итоге впервые привели к появлению на свет клонированного млекопитающего - мышки. К сожалению, статью не опубликовали в международном журнале и она осталась не замеченной мировой общественностью.
Неоднократно в средствах массовой информации появляются сообщения о готовящемся подобном эксперименте с клетками человека. Однако комитет контроля над генно-инженерными исследованиями выступил против клонирования человека, разрешив лишь работы на уровне клеток in vitro. Считается более перспективным направлением биотехнологии использование стволовых клеток для лечения некоторых заболеваний.
Стволовые клетки — предшественники всех клеток человека |
![]() Необходимо отметить, что основа науки о стволовых стромальных клетках была заложена около 30 лет назад советскими учеными А.Я. Фриденштейном и И.Л. Чертковым. В 1999 г. эти клетки «переоткрыли» американские ученые, за чем последовал лавинообразный рост работ в этой области.
Необходимо отметить, что основа науки о стволовых стромальных клетках была заложена около 30 лет назад советскими учеными А.Я. Фриденштейном и И.Л. Чертковым. В 1999 г. эти клетки «переоткрыли» американские ученые, за чем последовал лавинообразный рост работ в этой области.
Стромальные клетки костного мозга - плюрипотентные стволовые клетки взрослого организма, образующие строму костного мозга. Для того чтобы устранить повреждение клеток мышечной, костной, нервной либо другой ткани, их нужно восстановить. Здесь и играют свою ключевую роль стволовые клетки, расположенные в костном мозге. Стромальные стволовые клетки костного мозга универсальны. Получив сигнал о травме, они поступают с кровотоком в поврежденный орган или ткань и там под влиянием различных сигнальных веществ превращаются в нужные специализированные клетки, которые замещают погибшие, но необходимые организму в данный момент клетки: костные, мышечные, печеночные, сердечной мышцы или нервные клетки. Запас стволовых клеток (не прошедших дифференциацию) в организме не безграничен, а к старости их восстановительный потенциал понижается. Достижения биотехнологии позволяют вносить стволовые клетки в организм искусственно. В последние несколько лет опубликовано большое количество работ, подтверждающих, что стромальные стволовые клетки, попадая на повреждённые участки самых различных органов, превращаются именно в клетки того типа, который необходим, чтобы залечить повреждение. Попадая в поражённое инфарктом сердце, они преобразуются в клетки сердечной мышцы - миоциты, в поражённом инсультом головном мозгу - в нейроны и глиальные клетки. Стволовые клетки могут превращаться в клетки печени, костного мозга и т.д. Это даёт надежду на излечение огромного количества самых различных заболеваний. Особенно важно сохранение стволовых клеток для их использования самим донором. Хранение при температурах ниже -130°С может осуществляться в течение многих десятков лет. Это позволяет хранить детские клетки донора до возникновения потребности в них при заболевании или в старости. Реакция отторжения на собственные клетки исключена полностью. Поэтому будущее клеточной терапии и трансплантологии связано с использованием стволовых клеток, применяемых с целью замещения структурной и функциональной недостаточности различных органов.
В последнее время в литературе уделяется достаточно много внимания региональным стволовым клеткам (РСК), которые найдены уже почти во всех органах. Региональные стволовые клетки - взрослые соматические плюрипотентные стволовые клетки различных органов, способные к дифференцировке в клетки «своего» органа. Перспективно использование особенностей их роста в культуре и способности к дифференцировке. Установлено, что многие из них способны дифференцироваться не только в клетки того органа, в котором они находятся, но и в клетки других органов и тканей, происходящих даже из другого зародышевого листка. Основные преимущества РСК заключаются в том, что они могут быть использованы при необходимости как аутогенный клеточный материал. Поэтому не возникнет никаких иммунологических проблем, а также этических препятствий к их использованию. Недостатки и проблемы при использовании РСК для клеточной терапии связаны с тем, что ещё недостаточно изучены факторы их дифференцировки in vitro, их трудно получить в достаточном количестве для развития клинического эффекта после трансплантации. Кроме того, с возрастом их количество и терапевтический потенциал уменьшаются.

