Органическая химия

Амины – органические производные аммиака NH3, в молекуле которого один, два или три атома водорода замещены на углеводородные радикалы: RNH2; R2NH; R3N. |
Простейший представитель – метиламин:
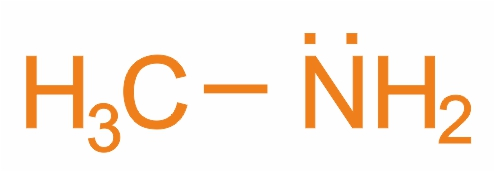
- 1. По количеству радикалов, связанных с атомом азота различают амины:
- ● первичные RNH2,
- ● вторичные R2NH,
- ● третичные амины R3N.
- 2. По характеру углеводородного радикала различают амины:
- ● алифатические (жирные),
- ● ароматические,
- ● смешанные (или жирноароматические).
АМИНЫ |
Первичные |
Вторичные |
Третичные |
Алифатические (жирные) |
|
|
|
Ароматические |
|
|
|
Смешанные |
– |
|
|
Номенклатура аминов
Названия аминов образуют из названий углеводородных радикалов и суффикса -амин:
CH3-NH2 |
Метиламин |
CH3-CH2-NH2 |
Этиламин |
Если радикалы разные их перечисляют по старшенству:
CH3-CH2-NH-CH3 |
Метилэтиламин |
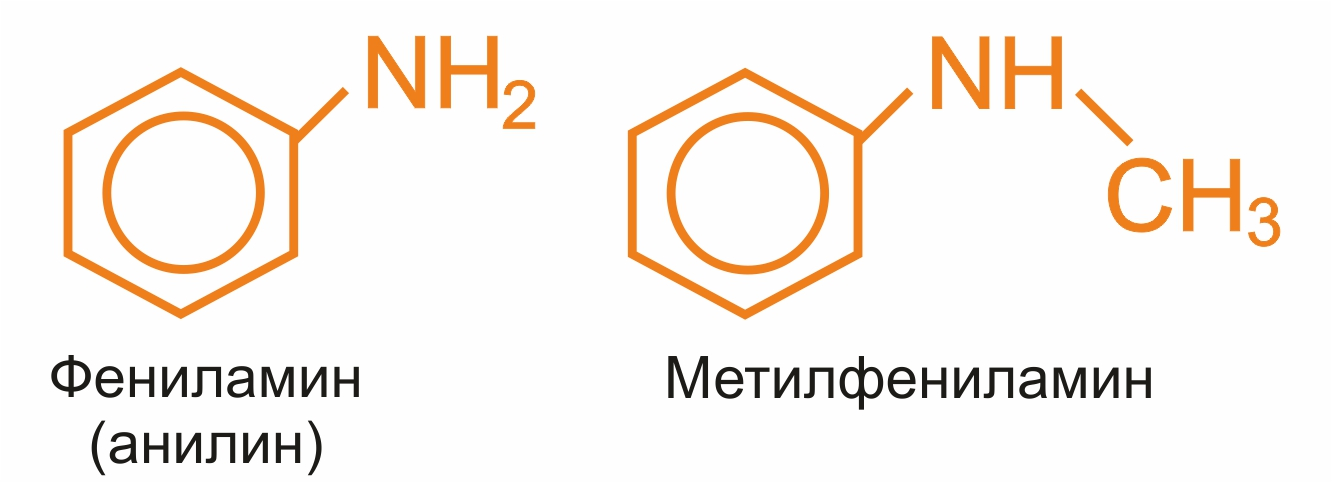
При наличии одинаковых радикалов используют приставки ди и три:
(CH3)2NH |
Диметиламин |
● углеродного скелета, начиная с С4H9NH2:
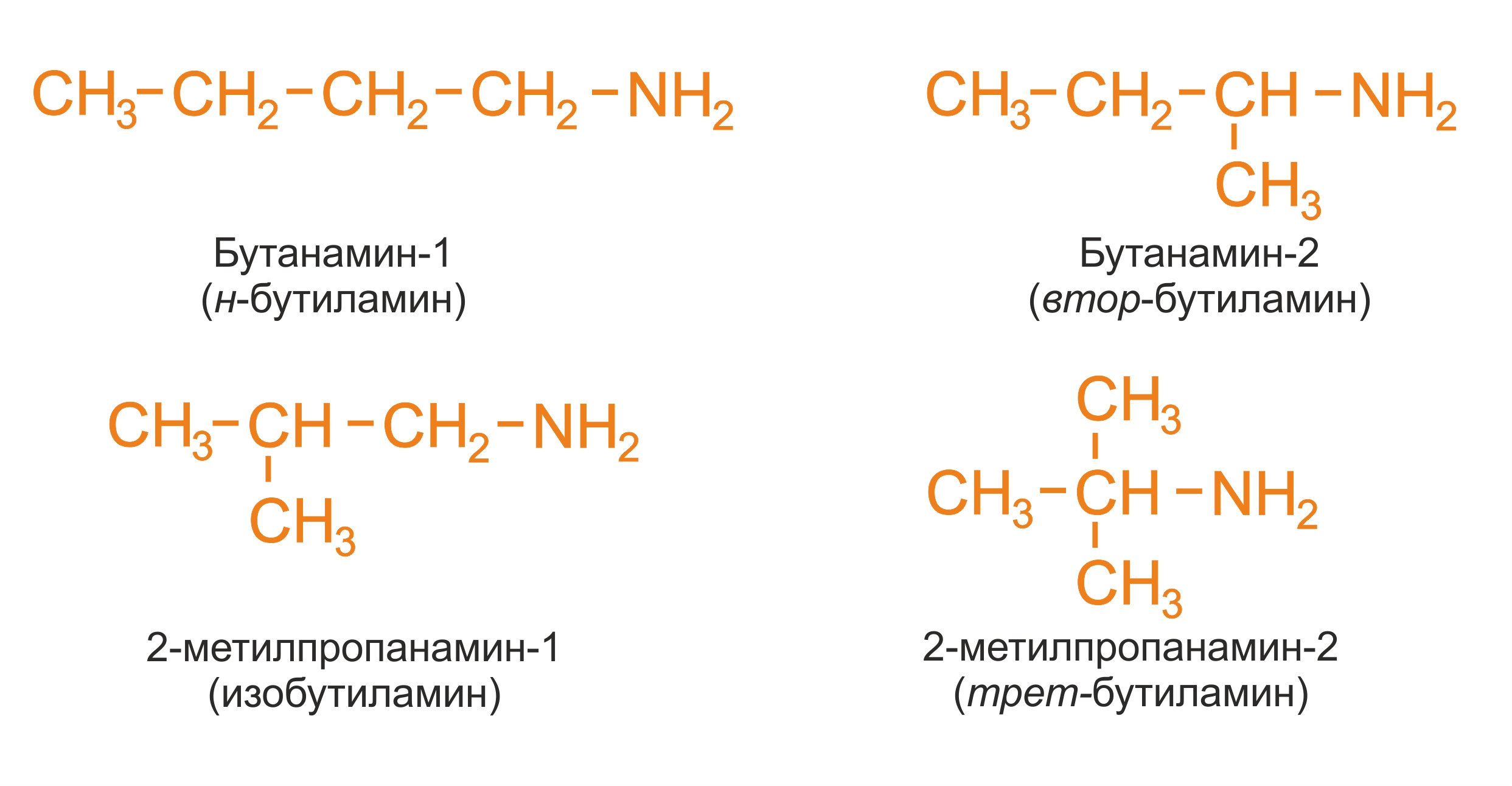
● положения аминогруппы, начиная с С3H7NH2:
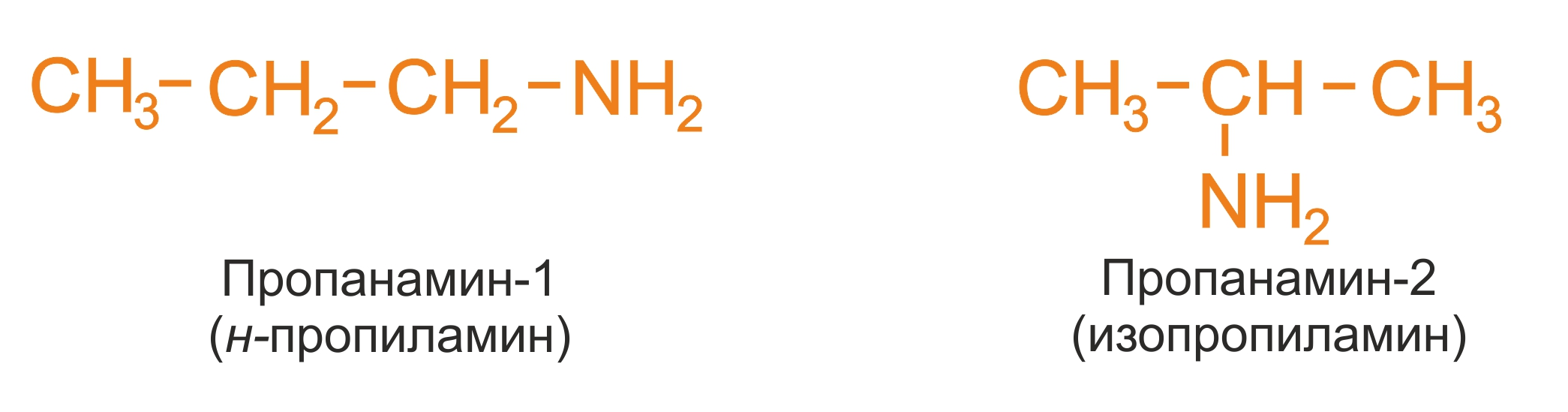
● изомерия аминогруппы, связанная с изменением степени замещенности атомов водорода при азоте, т.е. между типами аминов:
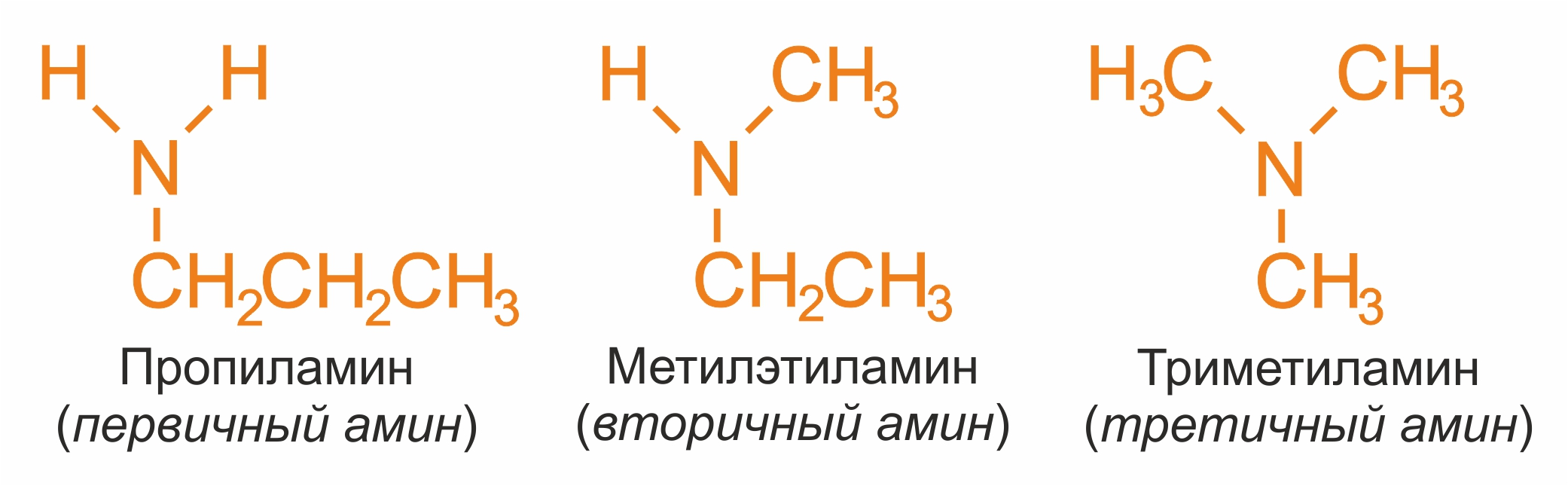
Пространственная изомерия - оптическая , начиная с С4H9NH2:
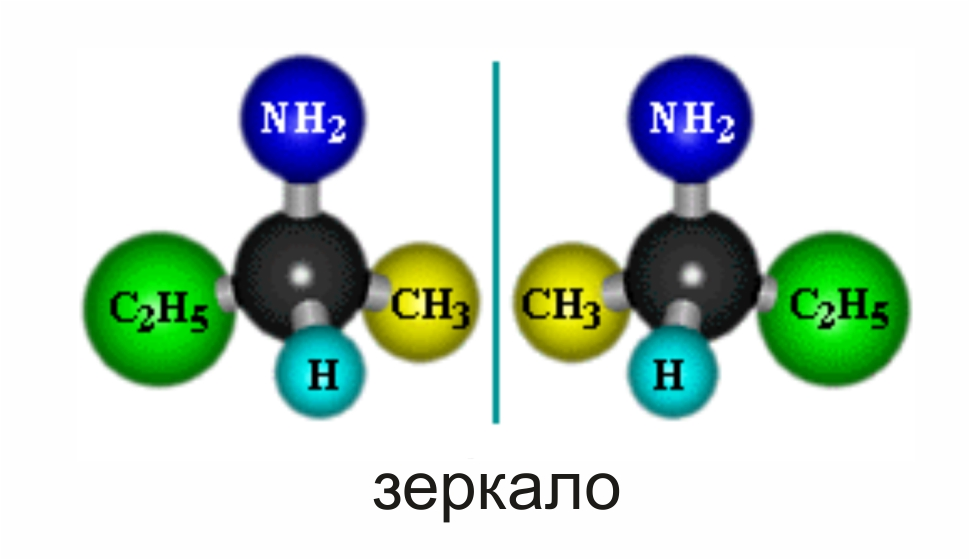
Получение аминов
1. Восстановление нитросоединений, при этом образуются первичные амины:
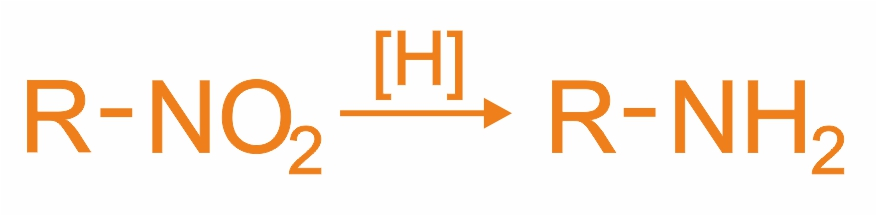
Важнейший ароматический амин - анилин - образуется при восстановлении нитробензола (восстановители - водород в присутствии металлических катализаторов, Fe + HCl, сульфиды):
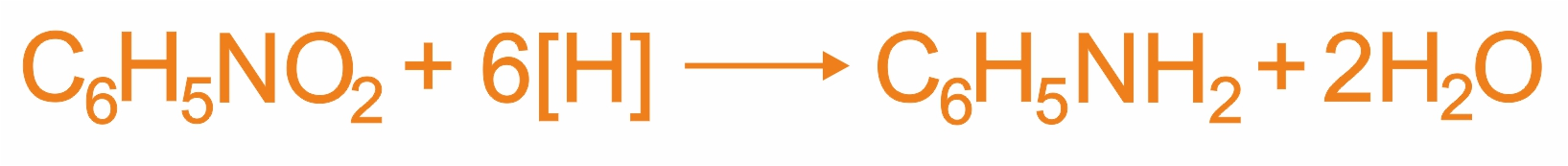
Эта реакция носит имя русского химика Н.Н. Зинина, осуществившего ее впервые в 1842 г.

(25.08.1812 - 18.02.1880)
2. Восстановление амидов (восстановитель - алюмогидрид лития LiAlH4):
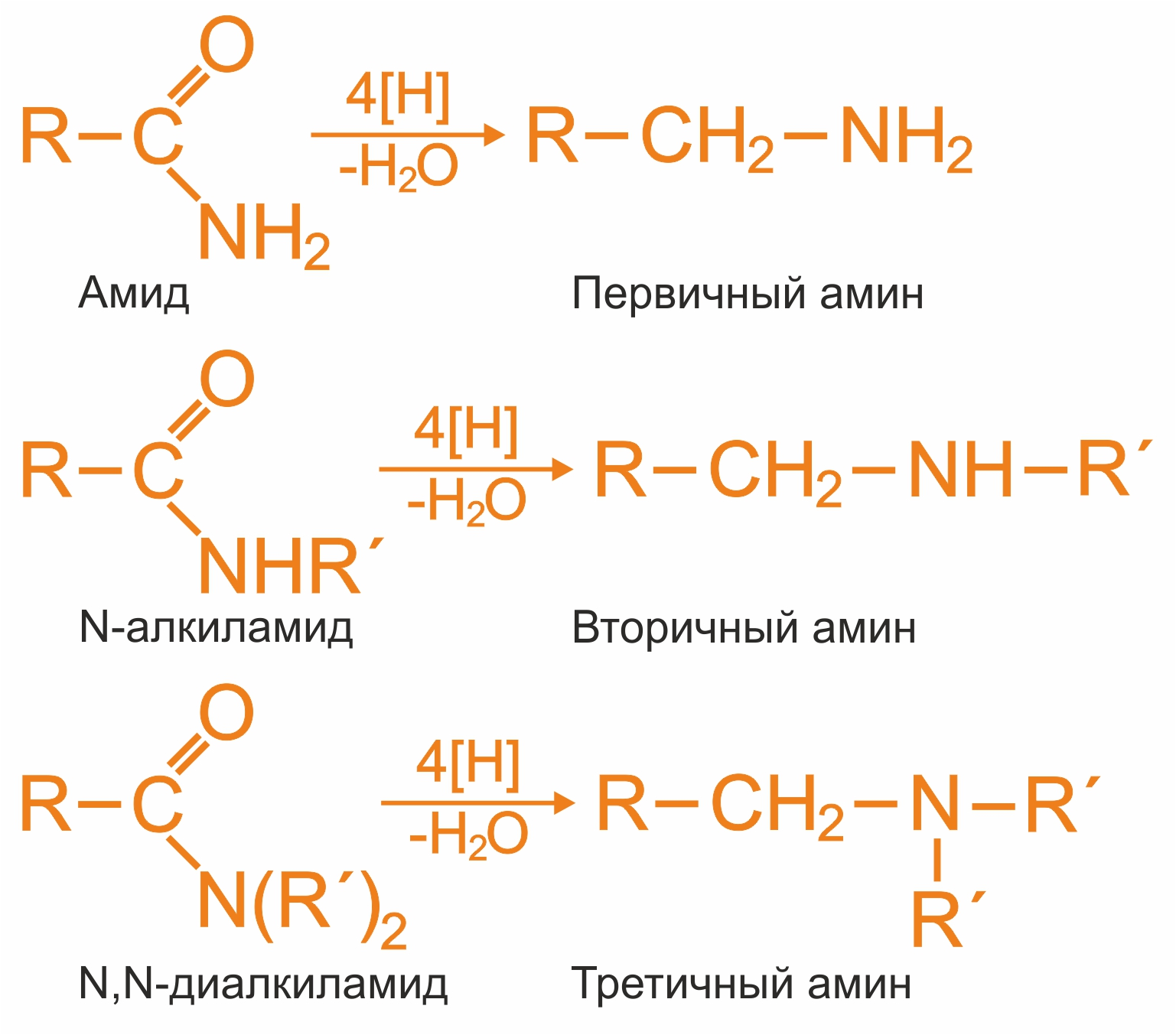
3. Восстановление нитрилов с образованием первичных аминов:
![]()
Этим способом в промышленности получают гексаметилендиамин, который используется в производстве полиамидного волокна найлон.
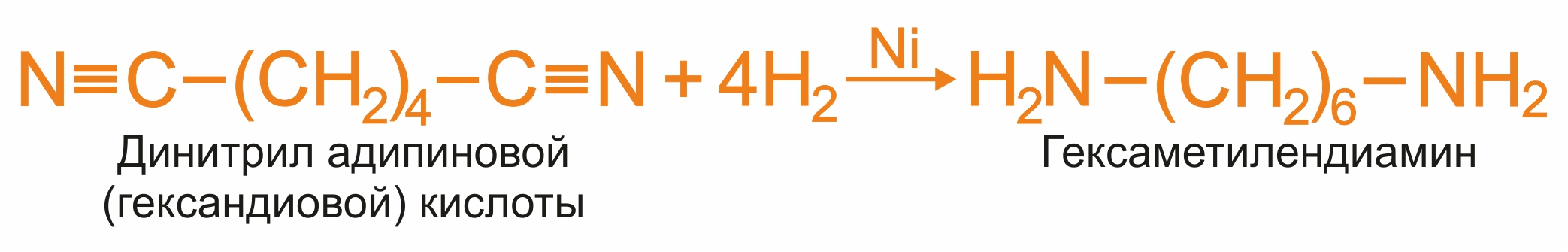
- При нагревании галогеналканов с аммиаком образуется смесь первичных, вторичных и третичных аминов:
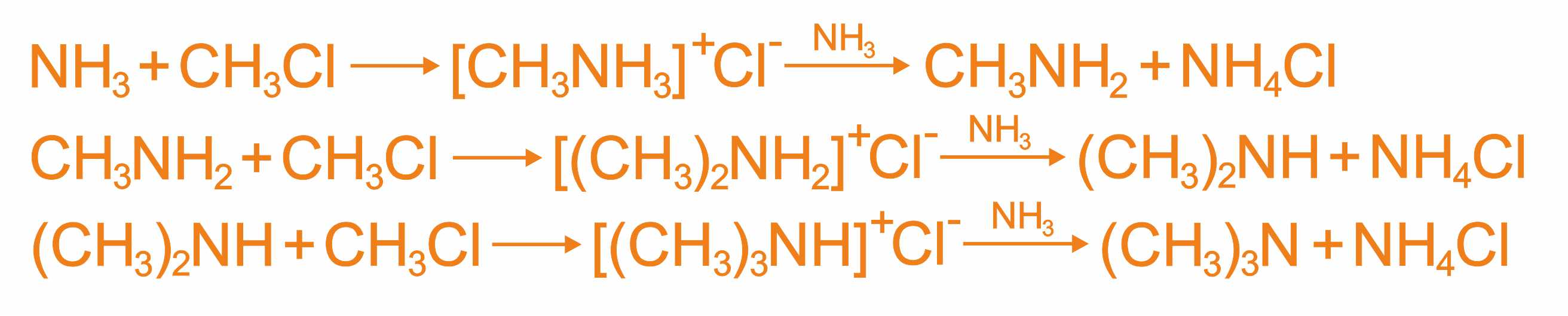
В основе этих превращений лежит реакция нуклеофильного замещения галогена в галогеналканах. Роль нуклеофила играют молекулы аммиака и аминов, имеющие неподеленную пару электронов на атоме азота. В промышленности алкилирование аммиака в большинстве случаев проводится не галогеналканами, а спиртами, в молекулах которых происходит нуклеофильное замещение ОН - группы на аминогруппу:
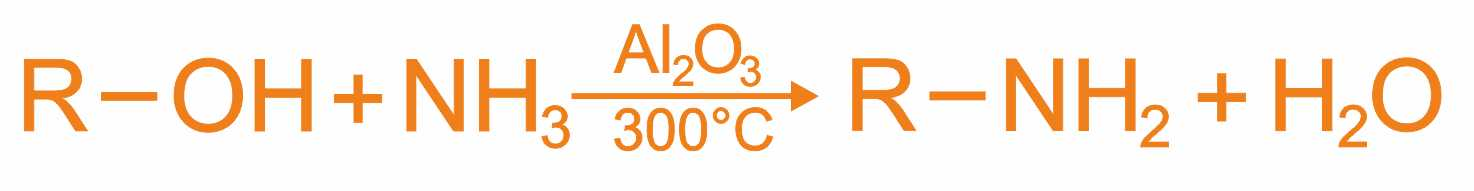
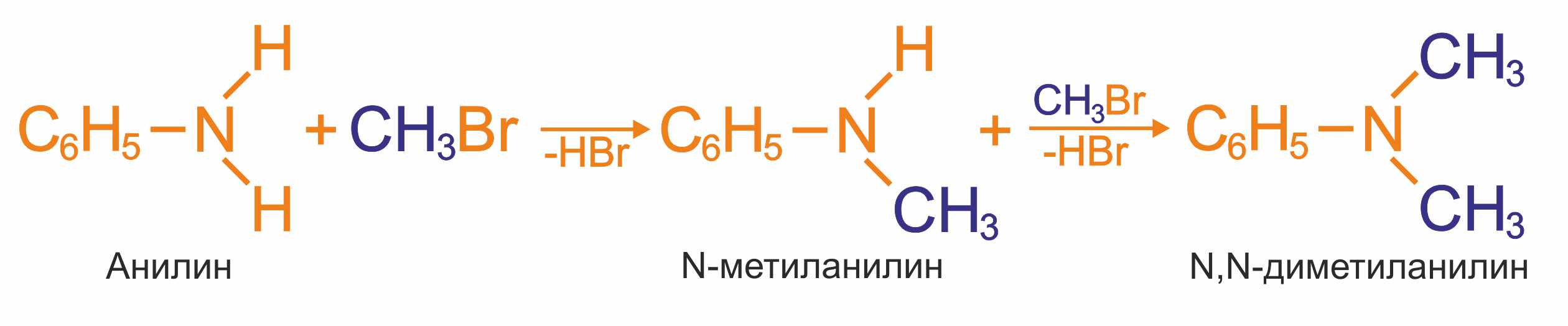
- Действием галогеналканов на первичные алифатические и ароматические амины получают вторичные и третичные амины, в том числе, смешанные.
Физические свойства аминов
Связь N–H является полярной, поэтому первичные и вторичные амины образуют межмолекулярные водородные связи ( более слабые, чем водородные связи с участием группы О–Н).
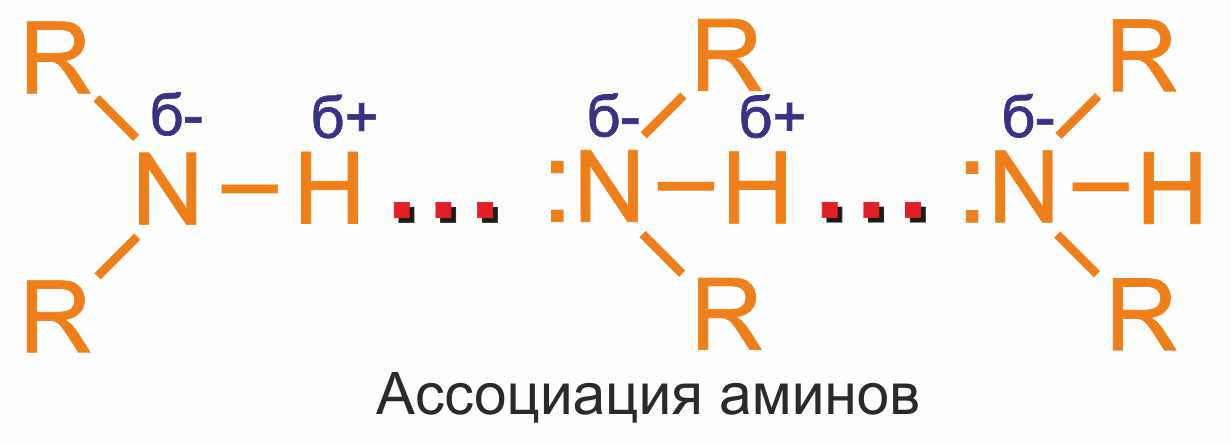
Это объясняет относительно высокую температуру кипения аминов по сравнению с неполярными соединениями со сходной молекулярной массой.
Например:
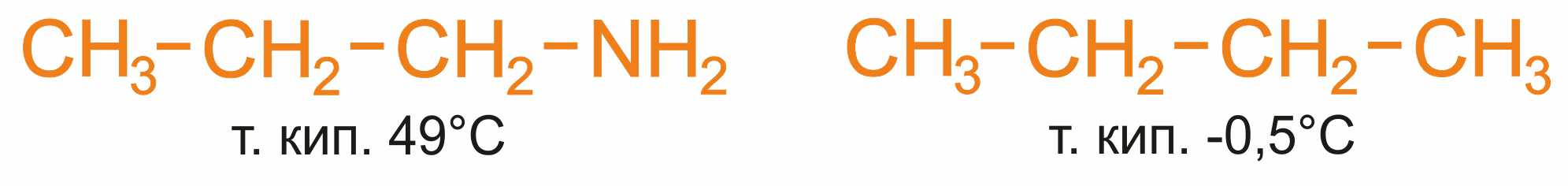
Третичные амины не образуют ассоциирующих водородных связей (отсутствует группа N–H). Поэтому их температуры кипения ниже, чем у изомерных первичных и вторичных аминов (триэтиламин кипит при 89°С, а н-гексиламин – при 133°С).
При обычной температуре только низшие алифатические амины CH3NH2, (CH3)2NH и (CH3)3N – газы (с запахом аммиака), средние гомологи – жидкости (с резким рыбным запахом), высшие – твердые вещества без запаха. Ароматические амины – бесцветные высококипящие жидкости или твердые вещества.
Амины способны к образованию водородных связей с водой:
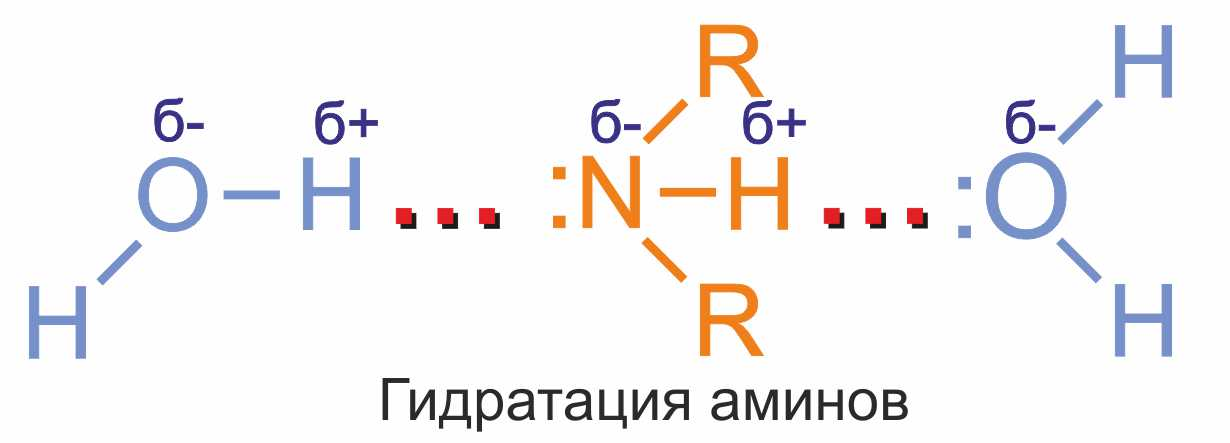
Поэтому низшие амины хорошо растворимы в воде. С увеличением числа и размеров углеводородных радикалов растворимость аминов в воде уменьшается, т.к. увеличиваются пространственные препятствия образованию водородных связей. Ароматические амины в воде практически не растворяются.
Химические свойства аминов
Амины имеют сходное с аммиаком строение и проявляют подобные ему свойства:
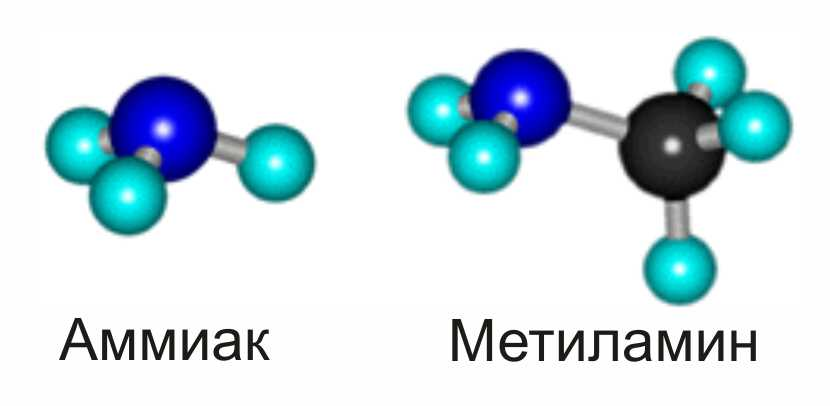
Как в аммиаке, так и в аминах атом азота имеет неподеленную пару электронов:
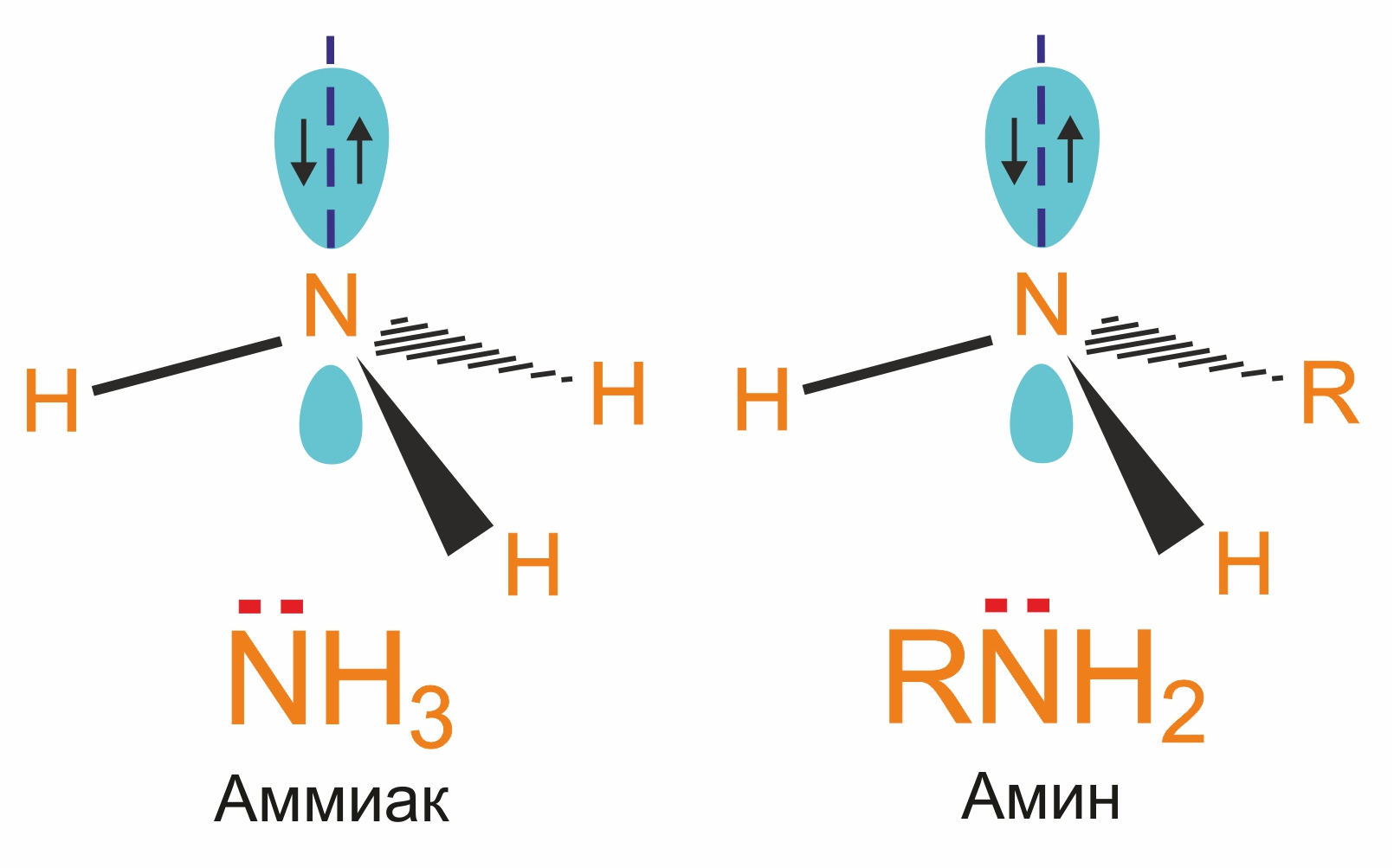
Поэтому амины и аммиак обладают свойствами оснований (акцепторов протона) и нуклеофильных реагентов (частиц, способных предоставить пару электронов для связи с атомом углерода).
1. Основность аминов
Для аминов характерны ярко выраженные основные свойства (за что их часто называют органическими основаниями).
- Водные растворы алифатических аминов проявляют щелочную реакцию, т.к. при их взаимодействии с водой образуются гидроксиды алкиламмония, аналогичные гидроксиду аммония:

Связь протона с амином, как и с аммиаком, образуется по донорно-акцепторному механизму за счет неподеленной электронной пары атома азота – более сильные основания, чем аммиак, т.к. алкильные радикалы увеличивают электронную плотность на атоме азота за счет +I-эффекта. По этой причине электронная пара атома азота удерживается менее прочно и легче взаимодействует с протоном.
Ароматические амины являются более слабыми основаниями, чем аммиак, поскольку неподеленная электронная пара атома азота смещается в сторону бензольного кольца, вступая в сопряжение с его π-электронами.
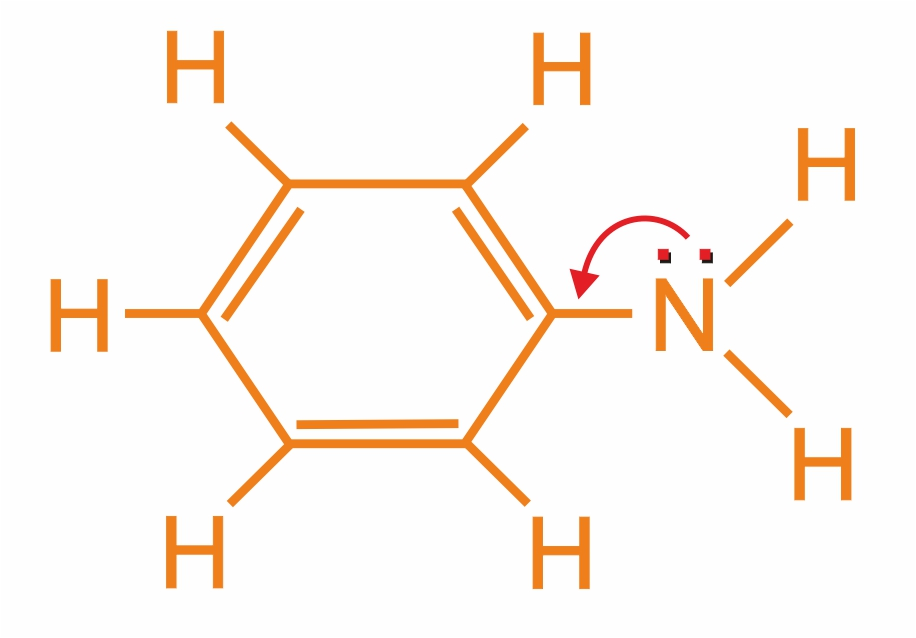 или
или 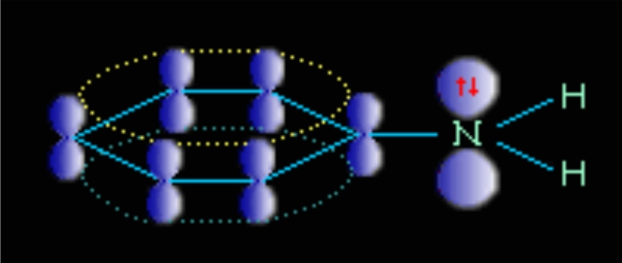
Уменьшение электронной плотности на атоме азота приводит к снижению способности отщеплять протоны от слабых кислот. Поэтому анилин взаимодействует лишь с сильными кислотами (HCl, H2SO4) и, в отличие от алифатических аминов и аммиака, не образует с водой гидроксида.
- Взаимодействуя с кислотами, амины образуют соли:
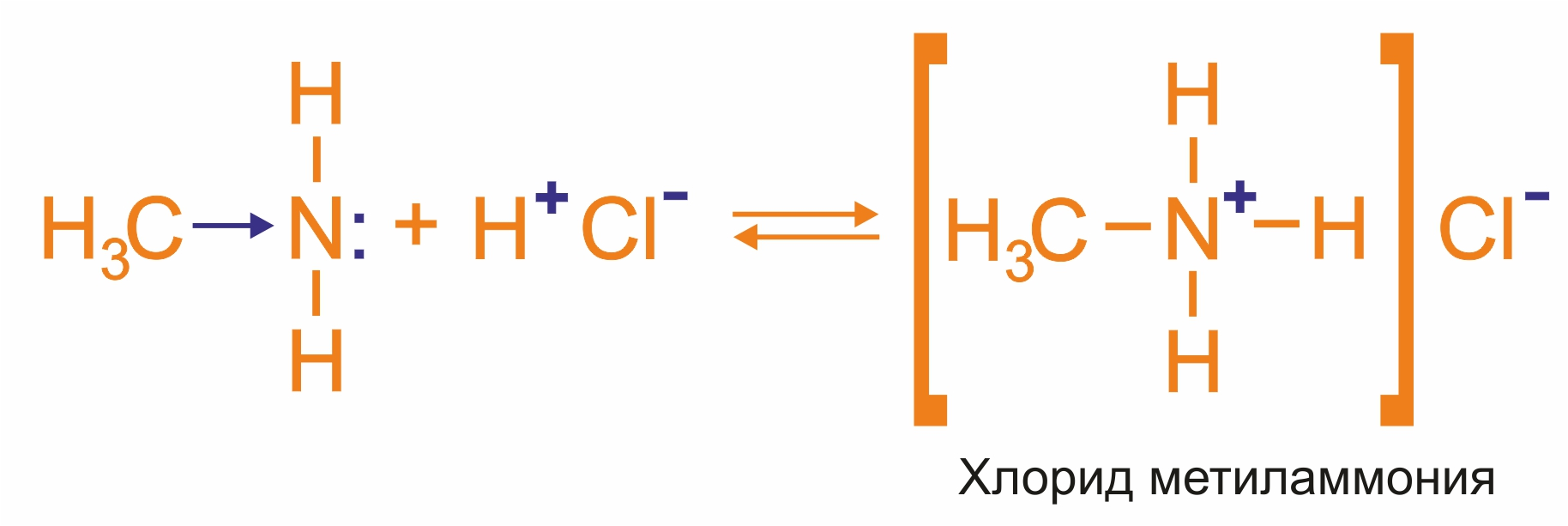
Взаимодействие анилин с соляной кислотой
Соли аминов – твердые вещества, хорошо растворимые в воде. |
![]() Щелочи (более сильные основания) легко вытесняют из них амины:
Щелочи (более сильные основания) легко вытесняют из них амины:

Основность простейших аминов (в растворе) возрастает в ряду:
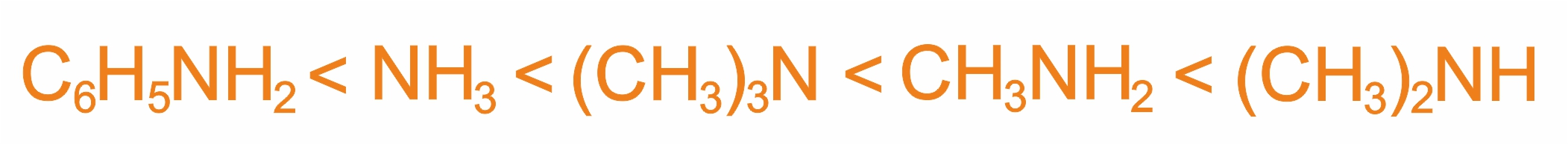
2. Окисление аминов
 Алифатические амины окисляются под действием сильных окислителей. В отличие от аммиака, низшие газообразные амины способны воспламеняться от открытогопламени.
Алифатические амины окисляются под действием сильных окислителей. В отличие от аммиака, низшие газообразные амины способны воспламеняться от открытогопламени.
Реакция горения (полного окисления) аминов на примере метиламина:

- Ароматические амины легко окисляются даже кислородом воздуха. Являясь в чистом виде бесцветными веществами, на воздухе они темнеют. Неполное окисление ароматических аминов используется в производстве красителей. Например, действием на анилин дихроматом калия в кислой среде получают краситель анилиновый черный, представляющий собой смесь сложных соединений.
Окисление анилина раствором дихромата калия
- Один из компонентов этого красителя имеет формулу:
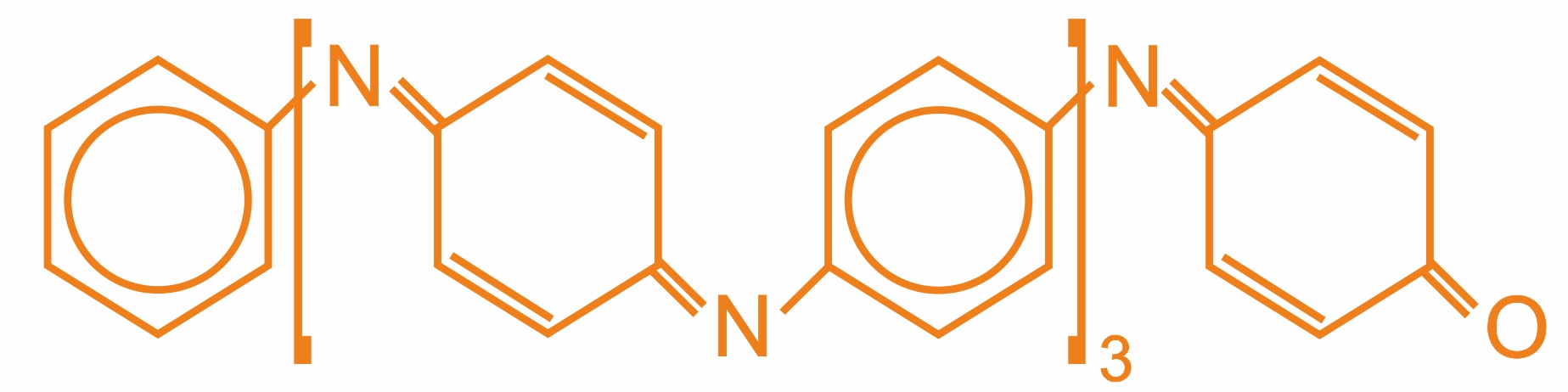
Краситель бензидиновый синий образуется при окислении дифениламина азотной (или азотистой) кислотой:
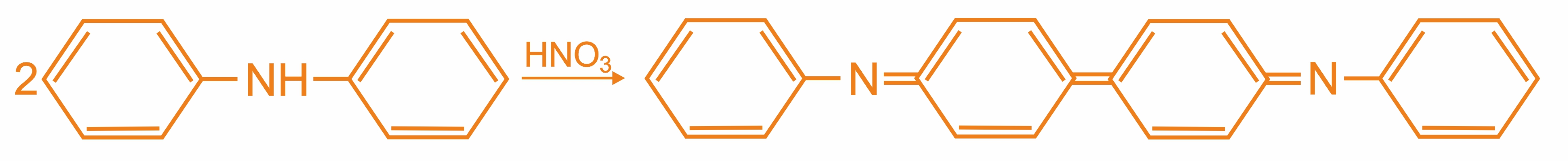
Эта реакция применяется в экологии для определения нитратов и нитритов (качественная реакция на NO3- и NO2-).
- Первичные алифатические амины c HNO2 образуют спирты. Характерным признаком реакции является выделение азота (дезаминирование аминов):

- Первичные ароматические амины при комнатной температуре реагируют аналогично, образуя фенолы и выделяя азот.
- Вторичные амины (алифатические, ароматические и смешанные) под действием HNO2 превращаются в нитрозоамины R2N-N=O – маслообразные вещества желтого цвета (нитрозо – название группы - N=O):
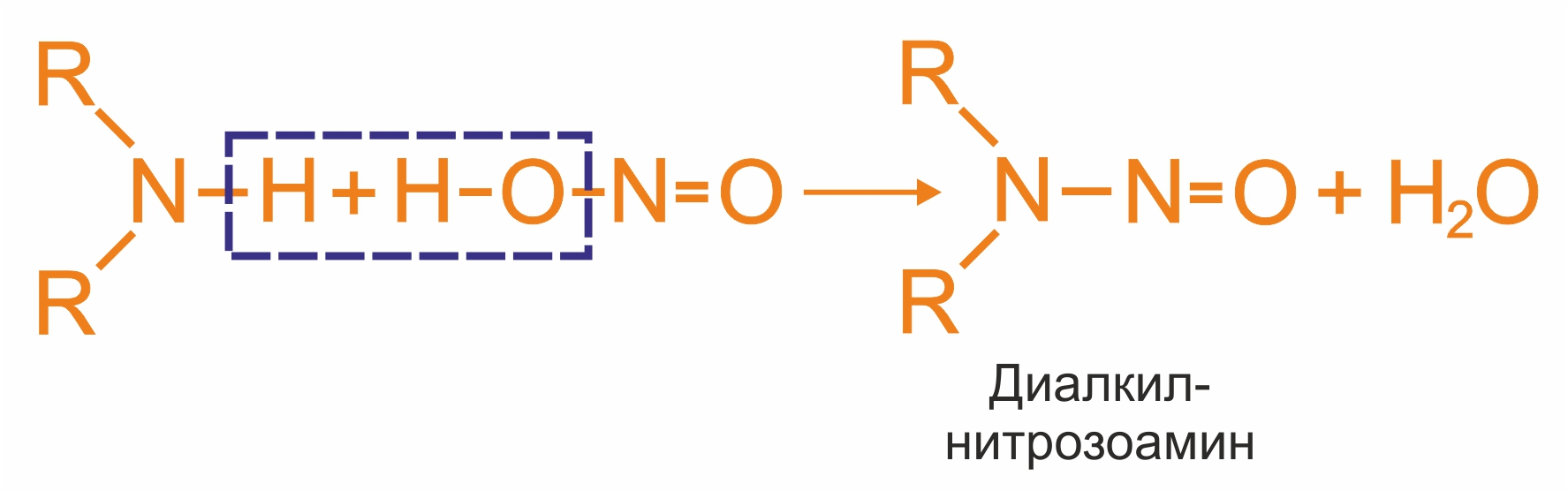
- Третичные алифатические амины при комнатной температуре и низкой концентрации HNO2 с ней не реагируют. Реакция при нагревании приводит к образованию смеси продуктов и не имеет практического значения.
Анилин
Анилин (фениламин) С6H5NH2 – важнейший из ароматических аминов:
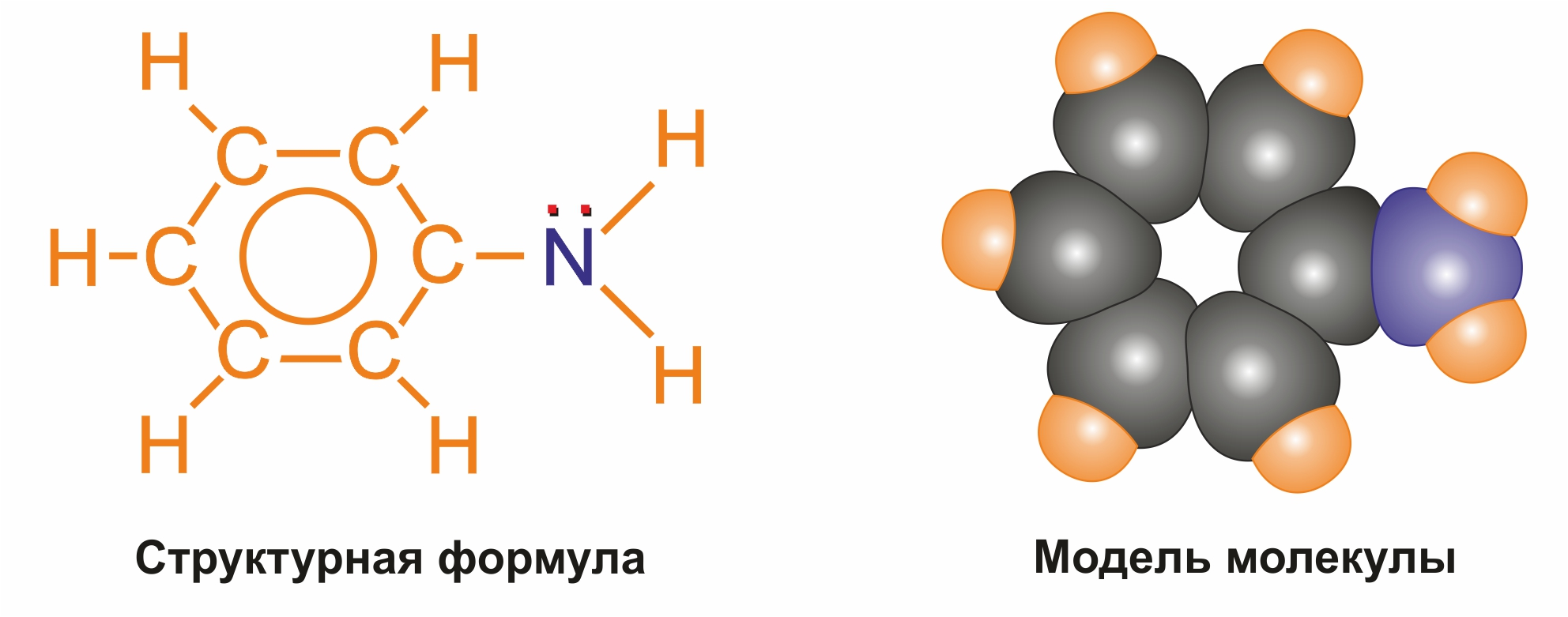
Физические свойства анилина
Анилин представляет собой бесцветную маслянистую жидкость с характерным запахом (т. кип. 184оС, т. пл. – 6оС). На воздухе быстро окисляется и приобретает красно-бурую окраску. Ядовит.
Химические свойства анилина
Для анилина характерны реакции: как по аминогруппе, так и по бензольному кольцу. Особенности этих реакций обусловлены взаимным влиянием атомов.
С одной стороны, бензольное кольцо ослабляет основные свойства аминогруппы по сравнению алифатическими аминами и даже с аммиаком.
С другой стороны, под влиянием аминогруппы бензольное кольцо становится более активным в реакциях замещения, чем бензол.
Например, анилин энергично реагирует с бромной водой с образованием 2,4,6-триброманилина (белый осадок).
Взаимодействие анилина с бромной водой
Эта реакция может использоваться для качественного и количественного определения анилина:
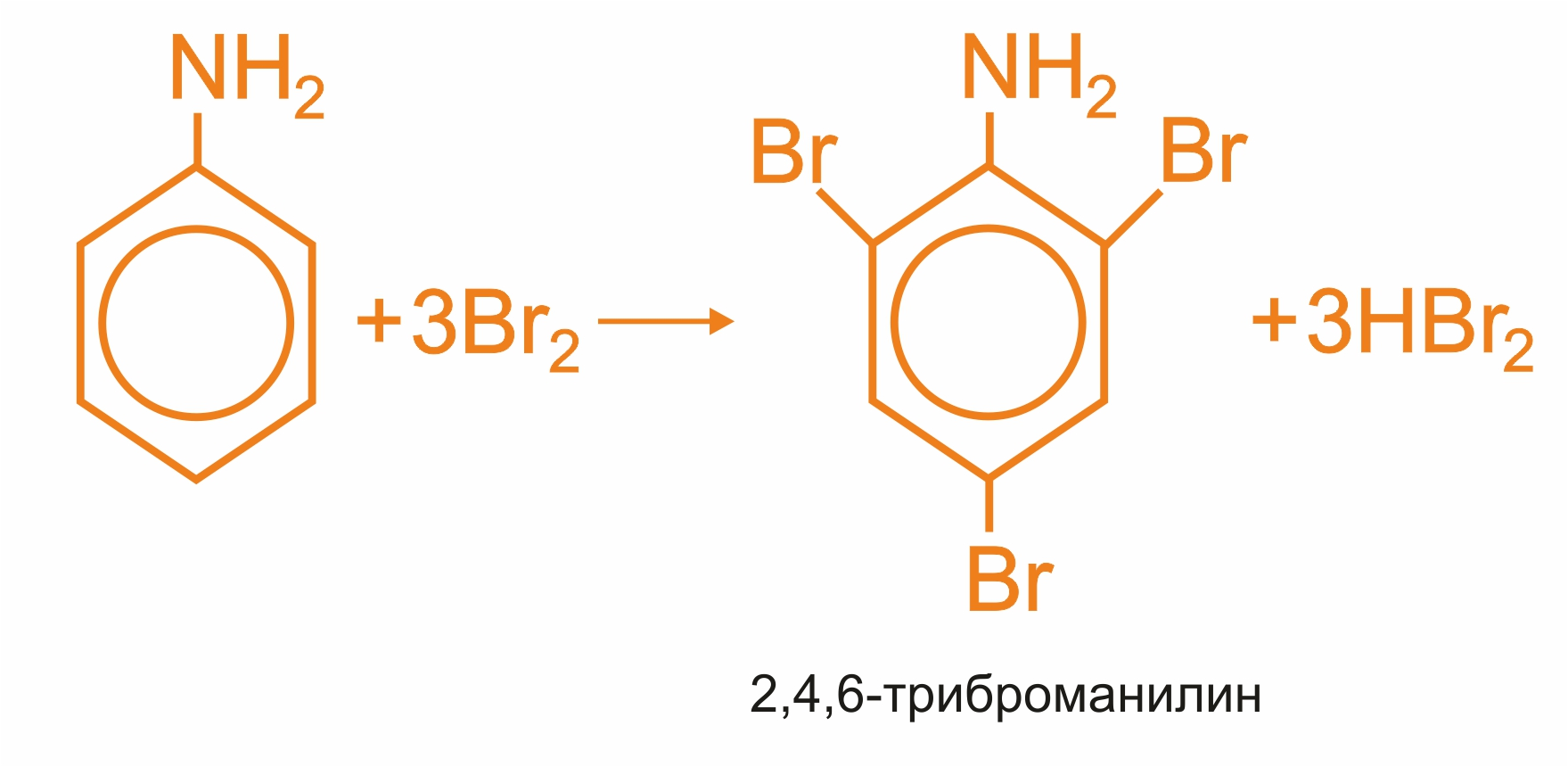
Аминогруппа - заместитель 1-го рода (активирующий орто-пара-ориентант в реакциях электрофильного замещения в ароматическом ядре).
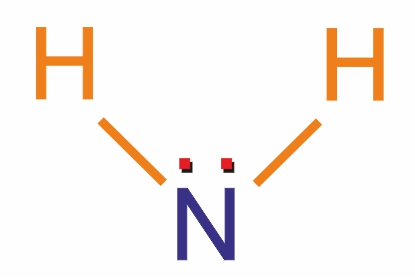
Такое взаимное влияние атомов в молекуле анилина объясняется сопряжением π-электронов бензольного кольца с неподеленной электронной парой атома азота (+M-эффект аминогруппы):
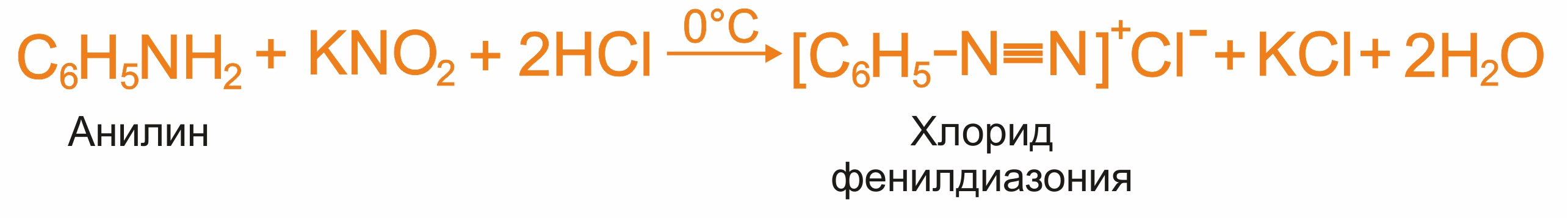
Практическое значение имеет реакция анилина с азотистой кислотой при пониженной температуре (около 0оС). В результате этой реакции (реакции диазотирования) образуются соли диазония (арилдиазониевые соли), которые используются в синтезе азокрасителей и ряда других соединений.
При более высокой температуре реакция идет с выделением азота и анилин превращается в фенол:
![]()
Анилин находит широкое применение в качестве полупродукта в производстве красителей, взрывчатых веществ и лекарственных средств (сульфаниламидные препараты).
Вредное воздействие аминов
Амины являются очень токсичными веществами. Опасно как вдыхание их паров, так и контакт с кожей. Амины, например анилин, способны всасываться сквозь кожу в кровь и нарушать функции гемоглобина, что может привести к летальному исходу. Симптомами отравления крови амином являются посинение кончиков пальцев, носа, губ, одышка, учащенное дыхание и сердцебиение, потеря сознания. В случае попадания амина на незащищенные участки кожи необходимо быстро и аккуратно, не увеличивая площадь поражения, очистить пораженный участок кожи ватой, смоченной в спирте. В случае отравления вывести пострадавшего на свежий воздух, обратиться к врачу. Большинство алкалоидов являются аминами (некоторые амидами).