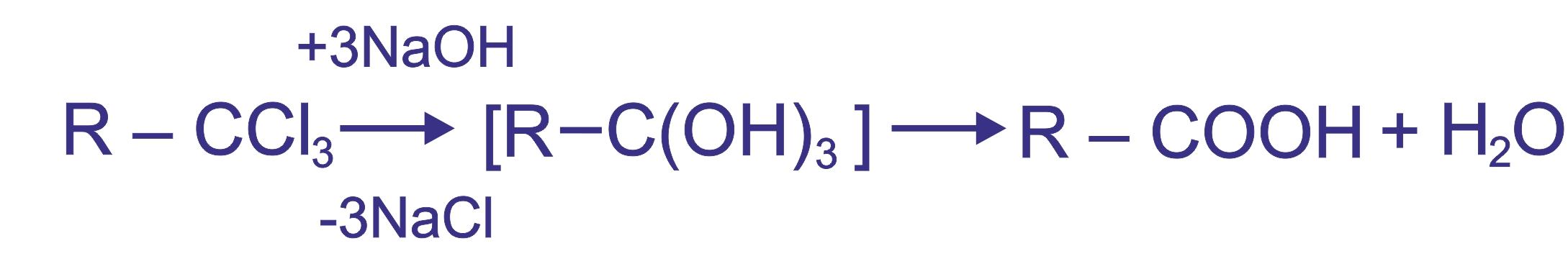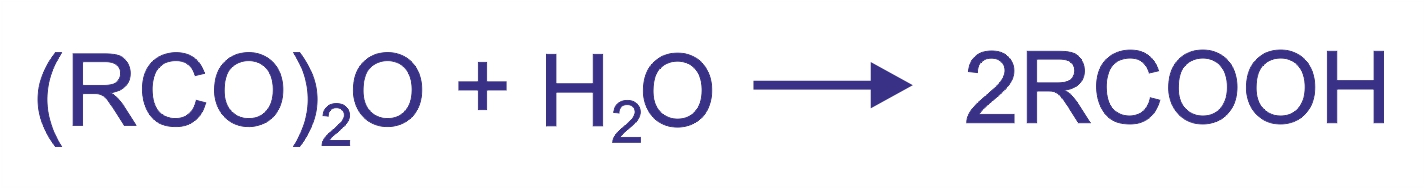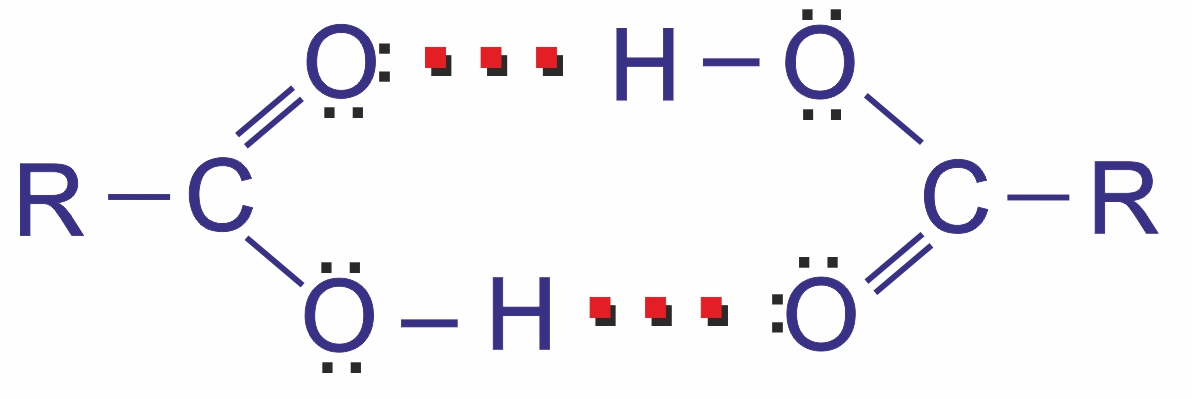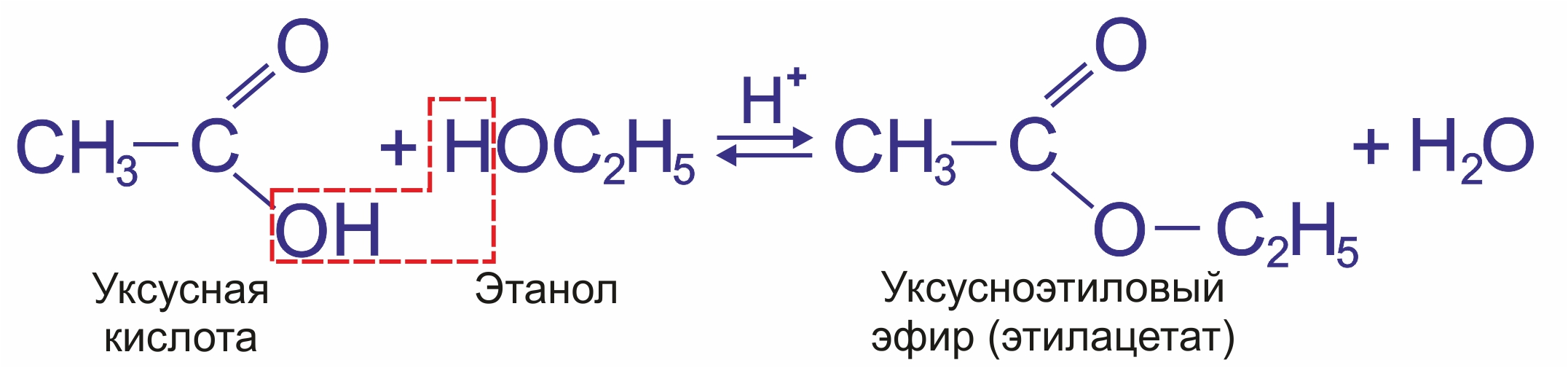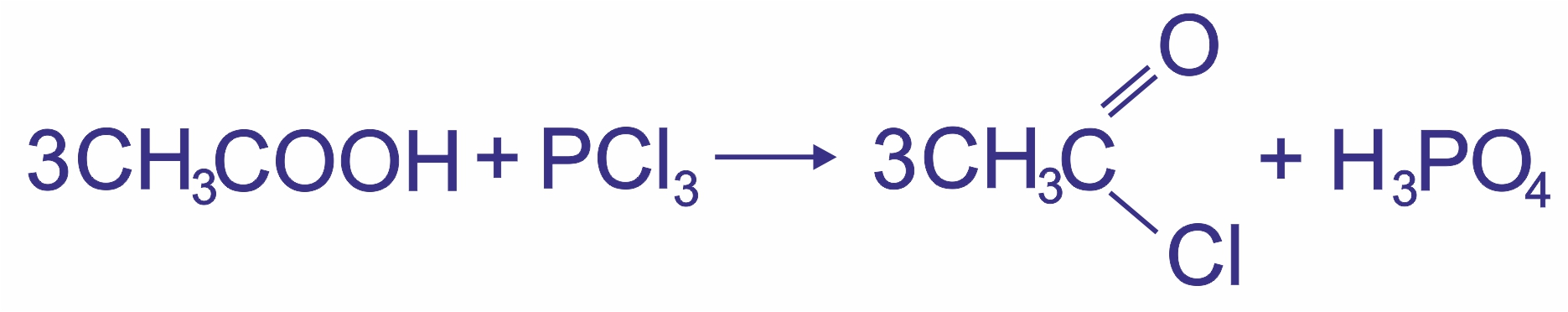Органическая химия

Тема 3.4. КАРБОНОВЫЕ КИСЛОТЫ. ЖИРЫ
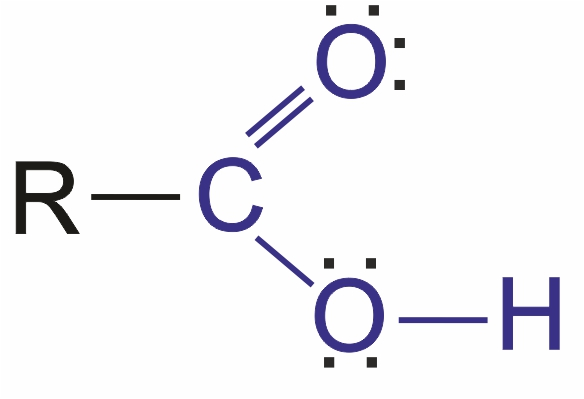
Карбоновые кислоты — органические соединения, содержащие одну или несколько карбоксильных групп –СООН. |
Эта группа носит название карбоксильная, происходящее от названий составляющих ее групп — карбонильной и гидроксильной.
Простейшие карбоновые кислоты |
||
Название |
Формула |
Модель |
Муравьиная кислота (метановая) |
|
|
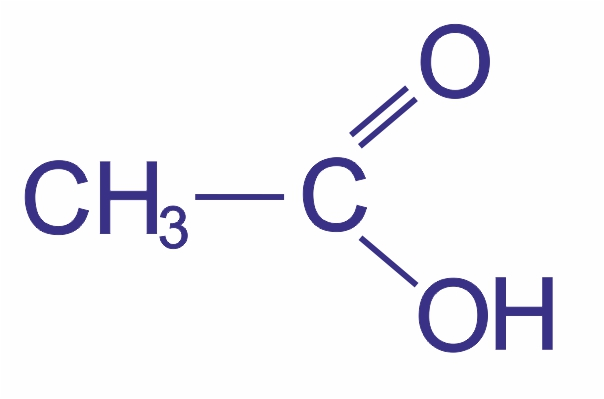
Уксусная кислота (этановая) |
|
|
Пропионовая кислота (пропановая) |
|
|
Классификация карбоновых кислот
1. |
По числу карбоксильных групп различают кислоты: |
|
• |
одноосновные (монокарбоновые):
|
|
• |
многоосновные (дикарбоновые, трикарбоновые и т.д.):
|
|
2. |
По характеру углеводородного радикала различают кислоты: |
|
• |
предельные (бутановая — CH3CH2CH2COOH); |
|
• |
непредельные (бутеновая — CH2=CH-CH2COOH); |
|
• |
ароматические (содержат бензольное кольцо RC6H4COOH); |
|
• |
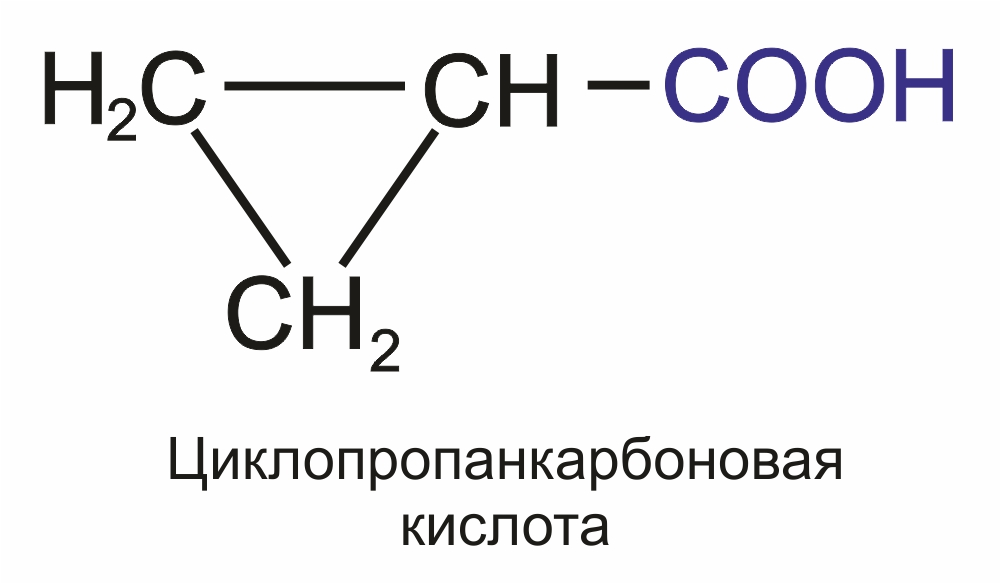
алициклические:
|
|
![]() Номенклатура карбоновых кислот
Номенклатура карбоновых кислот
По правилам международной номенклатуры ИЮПАК названия кислот даются по названию соответствующего углеводорода с добавлением суффикса -овая и слова кислота. Чтобы указать положение заместителя (или радикала), нумерацию углеродной цепи начинают от атома углерода карбоксильной группы.
Например:
![]()
Для органических кислот широко используются тривиальные названия, по природному источнику, где они были впервые обнаружены.
Некоторые одноосновные кислоты
Формула |
Название кислоты R-COOH |
Название остатка RCOO- |
|
систематическое |
тривиальное |
||
HCOOH |
Метановая |
Муравьиная |
Формиат |
CH3COOH |
Этановая |
Уксусная |
Ацетат |
C2H5COOH |
Пропановая |
Пропионовая |
Пропионат |
C3H7COOH |
Бутановая |
Масляная |
Бутират |
C4H9COOH |
Пентановая |
Валериаяновая |
Валерат |
C5H11COOH |
Гексановая |
Капроновая |
Капрат |
C15H31COOH |
Гексадекановая |
Пальмитиновая |
Пальмитат |
C17H35COOH |
Октадекановая |
Стеариновая |
Стеарат |
C6H5COOH |
Бензолкарбоновая |
Бензойная |
Бензоат |
CH2=СH-COOH |
Пропеновая |
Акриловая |
Акрилат |
Для многоосновных кислот применяют суффиксы -диовая, -триовая и т.д.
Например:
• |
HOOC-COOH — этандиовая (щавелевая) кислота; |
• |
HOOC-CH2-COOH — пропандиовая (малоновая) кислота. |
Изомерия карбоновых кислот
• |
изомерия скелета в углеводородном радикале (начиная с C4); |
• |
межклассовая изомерия, начиная с C2. |
• |
цис-, транс-изомерия в случае непредельных карбоновых кислот; |
• |
оптическая изомерия наблюдается у карбоновых кислот, в молекулах которых присутствует асимметрический атом углерода. |
Способы получения карбоновых кислот
1. |
Окисление альдегидов и первичных спиртов — общий способ получения карбоновых кислот. В качестве окислителей применяются KМnО4 и K2Сr2О7
|
|
2. |
Гидролиз трехгалоидпроизводных углеводородов (галогены находятся на одном атоме углерода). При этом образуются спирты, содержащие группы -ОН у одного атома углерода — такие спирты неустойчивы и отщепляют воду с образованием карбоновой кислоты:
|
|
3. |
||
• |
Получение нитрила:
|
|
• |
Образующийся нитрил (метилцианид) при нагревании легко гидролизуется с образованием карбоновой кислоты:
|
|
4. |
Гидролиз ангидридов кислот:
|
|
5. |
Гидролиз сложных эфиров:
|
|
Физические свойства монокарбоновых кислот
• |
Низшие члены этого ряда при обычных условиях представляют собой жидкости, обладающие характерным острым запахом. Например, этановая (уксусная) кислота имеет характерный уксусный запах. При -17°С она замерзает, превращаясь в льдистое вещество, которое получило название ледяная уксусная кислота. Средние представители этого гомологического ряда — вязкие, маслообразные жидкости; начиная с С10 — твердые вещества. |
• |
Кислоты, содержащие 1-3 углеродных атома, неограниченно смешиваются с водой. При увеличении углеводородного радикала растворимость монокарбоновых кислот уменьшается, твердые высшие жирные кислоты в воде не растворяются. |
• |
В жидком состоянии и в неводных растворах молекулы монокарбоновых кислот димеризуются в результате образования между ними водородных связей: Образование димеров карбоновых кислот
|
Это объясняет гораздо более высокие температуры кипения карбоновых кислот по сравнению со спиртами и альдегидами с тем же числом атомов углерода; температуры плавления и кипения с ростом молекулярной массы возрастают.
Химические свойства карбоновых кислот
Свойства карбоновых кислот
1. |
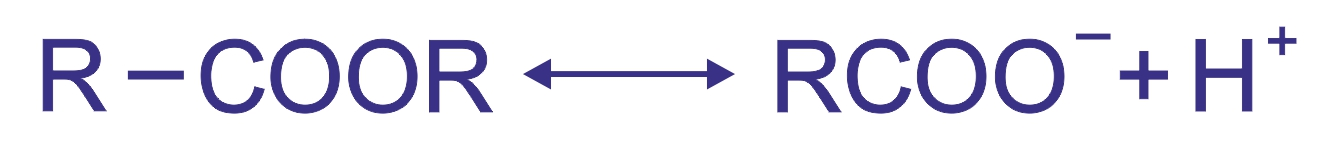
Диссоциация на ионы в водном растворе, карбоновые кислоты — слабые электролиты, равновесие реакции сильно смещено влево:
|
2. |
Названия солей составляют из названий кислотного остатка RCOO– и металла. Например: CH3COONa — ацетат натрия; (HCOO)2Ca — формиат кальция; C17H35COOK — стеарат калия и т.п. |
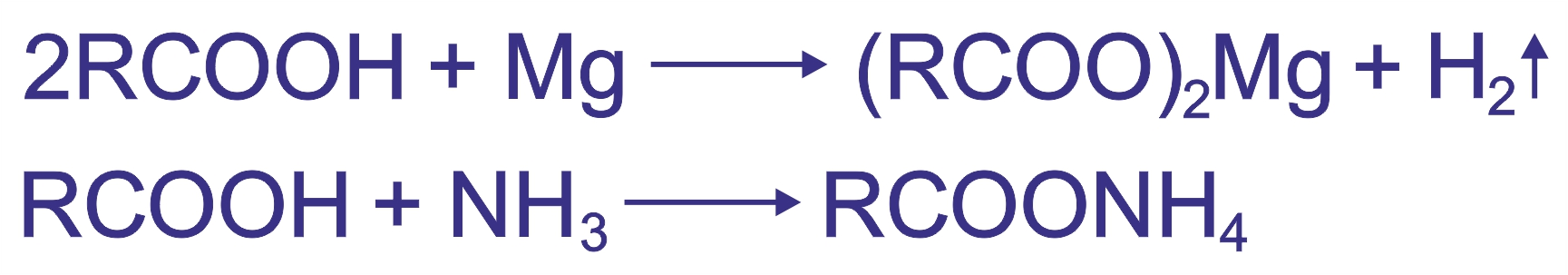
3. |
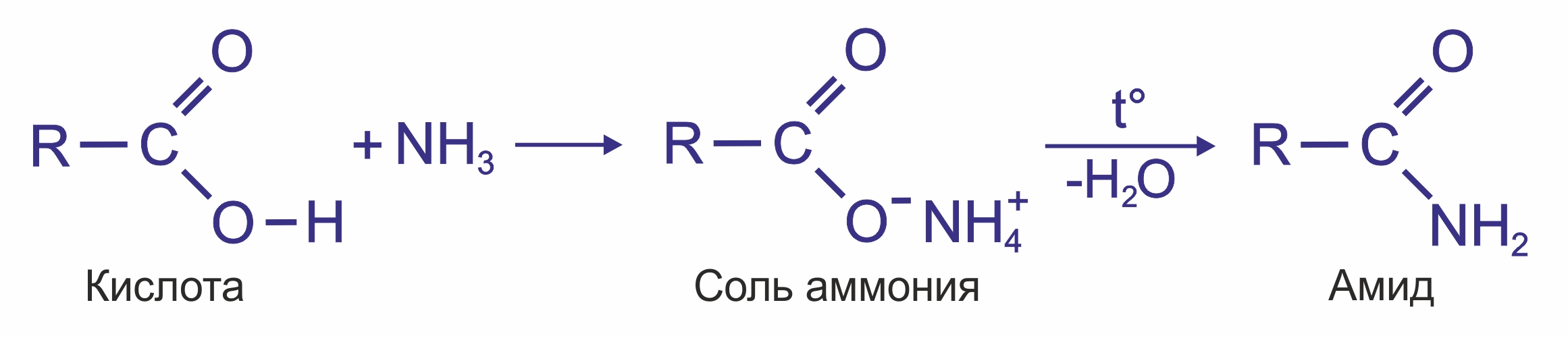
|
4. |
|
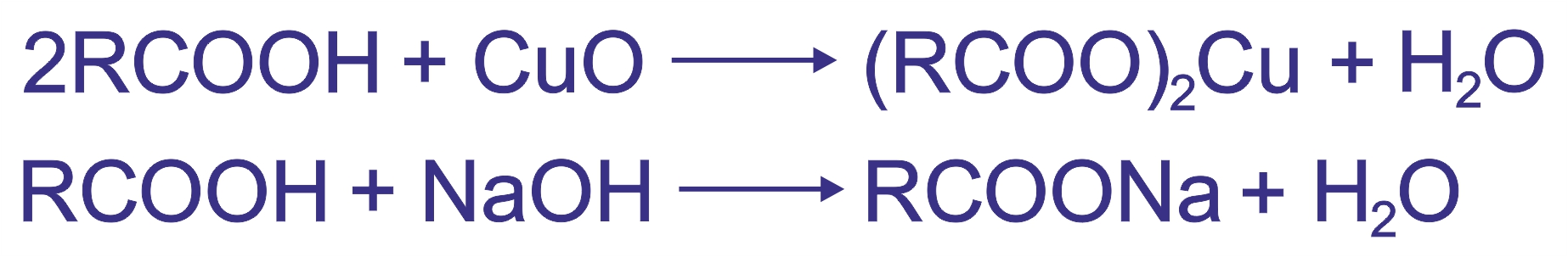
5. |
|
6. |
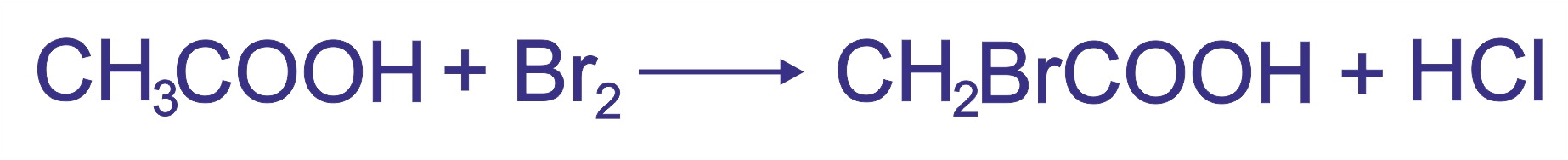
Галогенирование кислот:
|
Применение карбоновых кислот
Муравьиная кислота применяется в качестве восстановителя, в медицине используется муравьиный спирт (1,25%-й спиртовой раствор муравьиной кислоты).
Уксусная кислота применяется для синтеза красителей, медицинских препаратов, сложных эфиров, при производстве ацетатных волокон. В домашнем хозяйстве — как вкусовое и консервирующее вещество.
Пальмитиновая и стеариновая кислоты встречаются в природе в виде глицериновых эфиров, которые являются главными составными частями растительных и животных жиров.
Терефталевая кислота широко используется в производстве синтетических волокон.
Непредельные акриловая и метакриловая кислоты полимеризуются, образуя полиакрилаты. Это разнообразный класс пластических масс, имеющий большое техническое значение.
Жиры — это сложные эфиры глицерина и высших одноосновных карбоновых кислот.
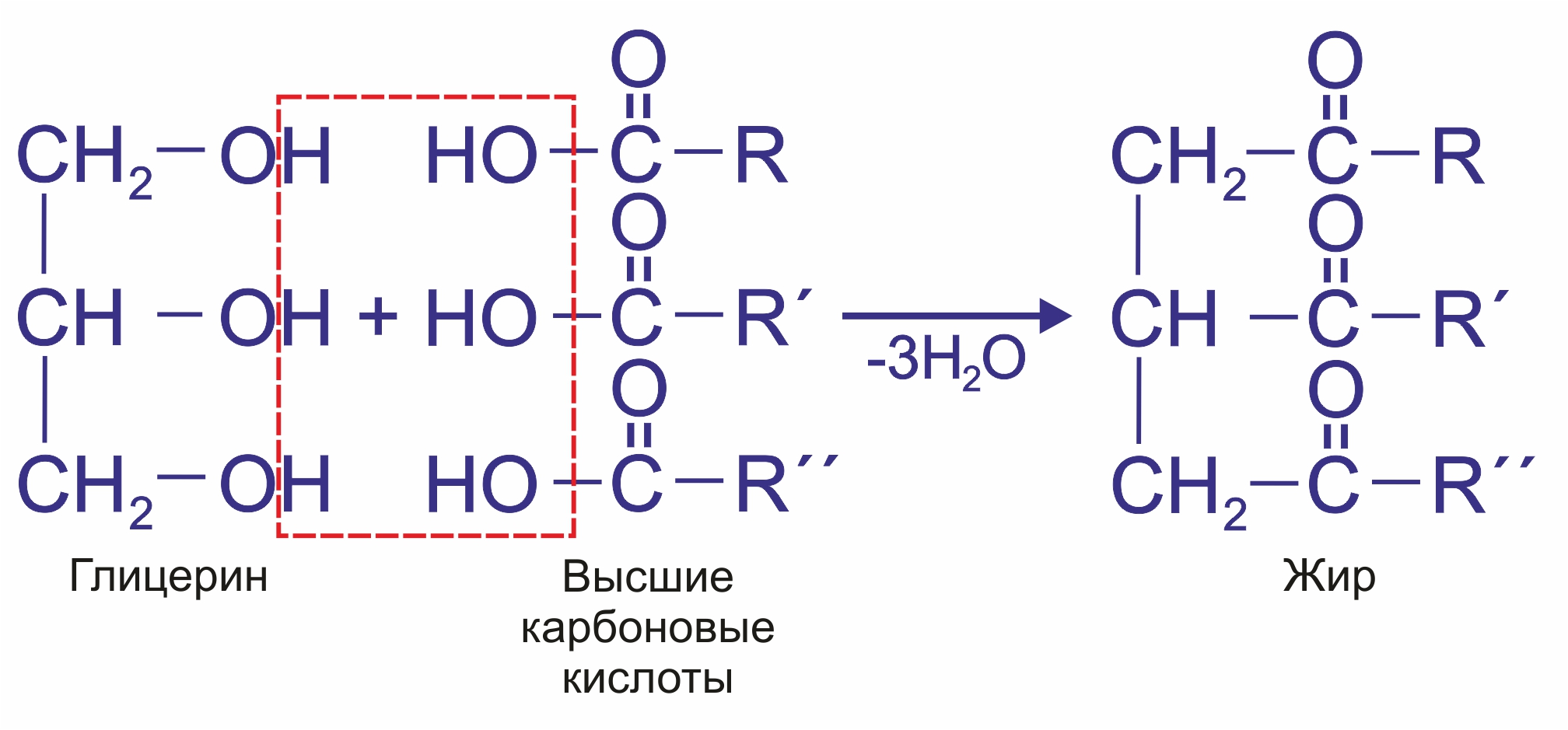
![]() В состав природных триглицеридов входят остатки кислот:
В состав природных триглицеридов входят остатки кислот:
• |
насыщенных (предельных): пальмитиновой C15H31COOH, стеариновой C17H35COOH и др. |
• |
ненасыщенных (непредельных): олеиновой C17H33COOH, линолевой C17H31COOH, линоленовой C15H29COOH и др. |
• |
Животные жиры (бараний, свиной, говяжий и т.п.), как правило, являются твердыми веществами с невысокой температурой плавления (исключение — рыбий жир). В твёрдых жирах преобладают остатки насыщенных кислот. |
• |
Растительные жиры — масла (подсолнечное, соевое, хлопковое и др.) — жидкости (исключение — кокосовое масло, масло какао-бобов). Масла содержат в основном остатки ненасыщенных (непредельных) кислот. |
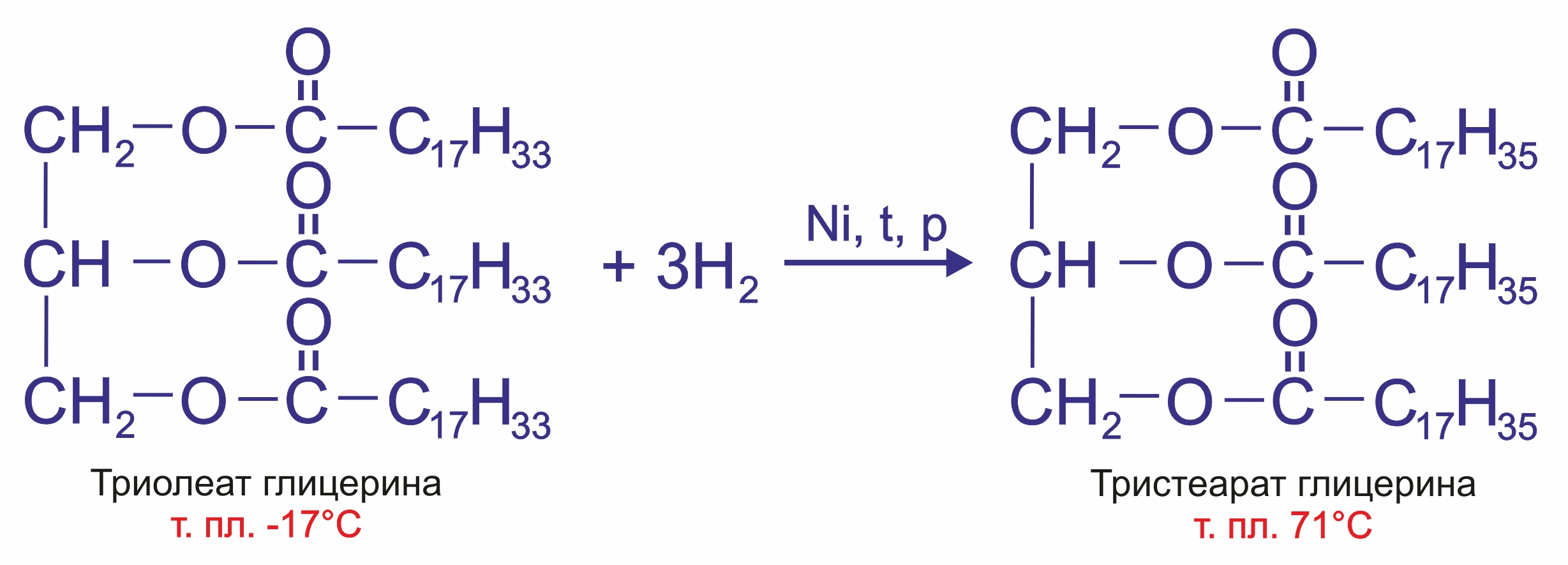
1. |
Гидрогенизация жира (каталитическое гидрирование). При этом водород присоединяется по двойной связи, содержащейся в углеводородном радикале молекул масел и жидкие жиры превращаются в твердые:
|
2. |
Продуктами в этом случае являются мыла — соли высших карбоновых кислот и щелочных металлов.
|
Натриевые соли высших карбоновых кислот — твердые мыла, калиевые — жидкие. |
Большое значение имеют так называемые высыхающие масла (льняное, тунговое и др.), которые входят в состав красок и лаков (в частности, олифы). Эти масла отличаются высоким содержанием остатков кислот с двумя или тремя двойными связями. Они образуют на окрашенной поверхности прочную пленку за счет полимеризации по кратным связям под действием кислорода воздуха.