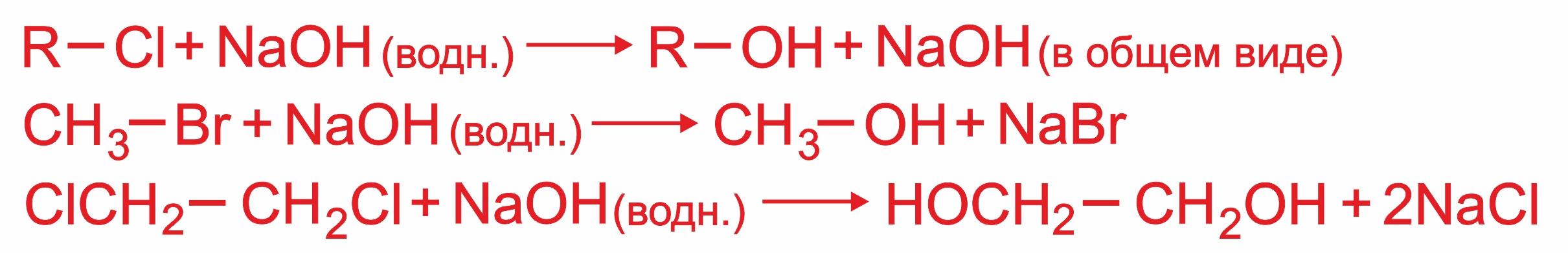Органическая химия

Тема 3.1. СПИРТЫ
Спирты – это органические соединения, производные углеводородов, содержащие в своем составе одну или несколько гидроксильных групп –ОН. |
Простейшие спирты |
||
Название |
Формула |
Модели |
Метиловый спирт (метанол) |
CH3-OH |
|
Этиловый спирт (этанол) |
CH3CH2-OH |
|
Классификация спиртов
1. |
В зависимости от строения углеводородного радикала различают спирты: |
• |
предельные – алканолы (например, СH3CH2–OH – этиловый спирт, этанол); |
• |
непредельные – алкенолы (например, CH2=CH–CH2–OH – пропенол-1); |
• |
ароматические – группа –ОН связана с бензольным кольцом через один или несколько атомов углерода (например, C6H5CH2–OH). |
2. |
От количества групп –ОН: |
• |
одноатомные (одна группа –ОН) – например, CH3–OH метанол; |
• |
2-атомные (две группы –ОН) – диолы , гликоли, например, этиленгликоль HO–СH2–CH2–OH (м.н. этандиол); |
• |
3-атомные (три группы –ОН) – триолы, например, глицерин HO–СH2–СН(ОН)–CH2–OH (м.н. пропантриол-1,2,3); |
• |
многоатомные (несколько групп –ОН) – полиолы. |
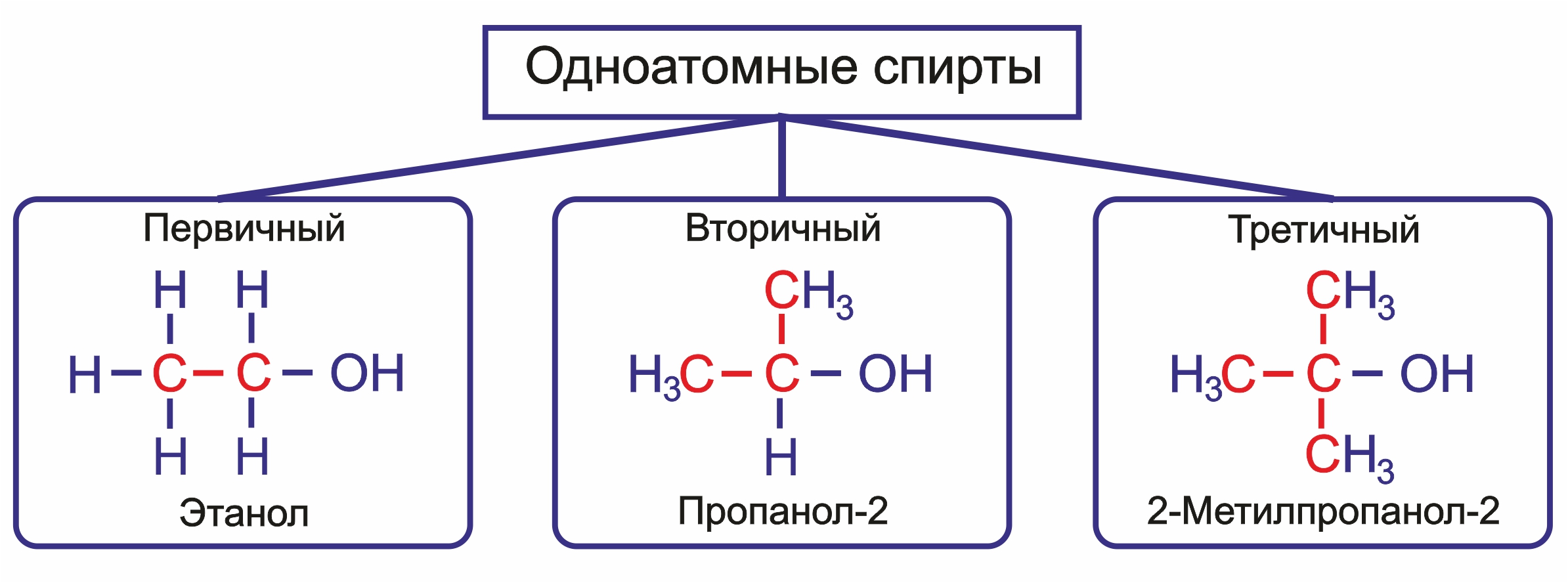
3. |
Предельные одноатомные спирты в зависимости от того, при каком углеродном атоме находится гидроксильная группа, делятся на: |
• |
первичные (RСН2ОН); |
• |
вторичные (R2СНОН); |
• |
третичные (R3СОН). |
Общая формула гомологического ряда предельных одноатомных спиртов – CnH 2n + 1OH или R – OH
Номенклатура спиртов
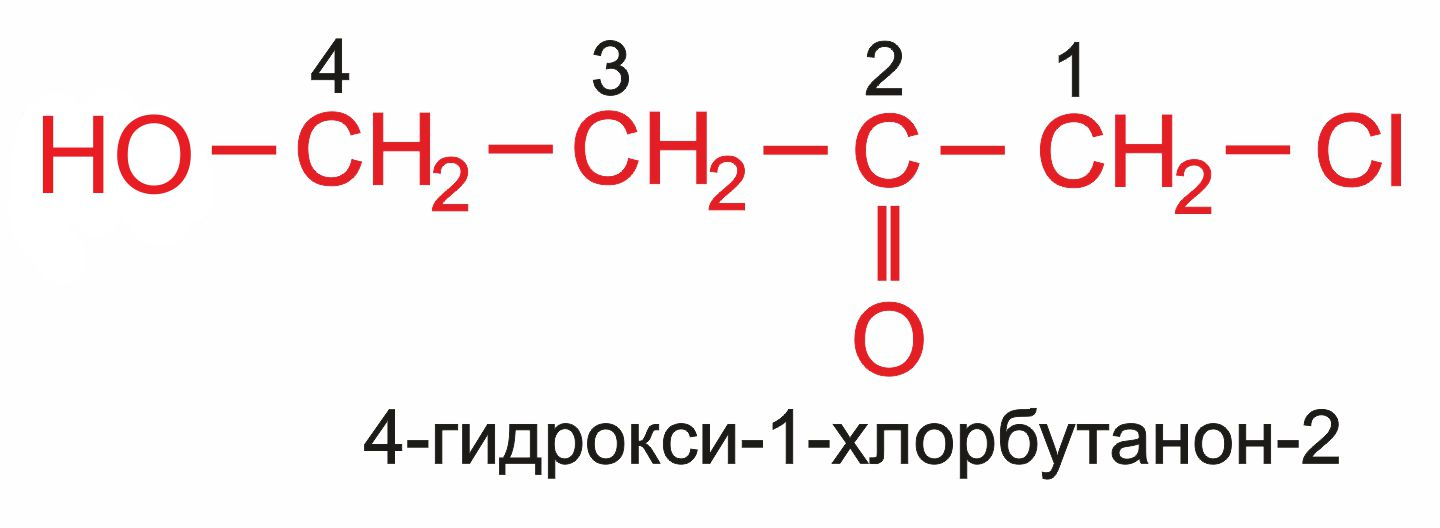
В соответствии с номенклатурой ИЮПАК при построении названия одноатомного спирта к названию родоначального углеводорода добавляется суффикс –ол и цифра, указывающая, на каком атоме углерода находится группа –ОН. При наличии в соединении более старших функций гидроксильная группа обозначается префиксом гидрокси- (окси-). В качестве основной цепи выбирается наиболее длинная цепь углеродных атомов, в состав которой входит атом углерода, связанный с гидроксильной группой; если соединение является ненасыщенным, то в эту цепь включается также и кратная связь.
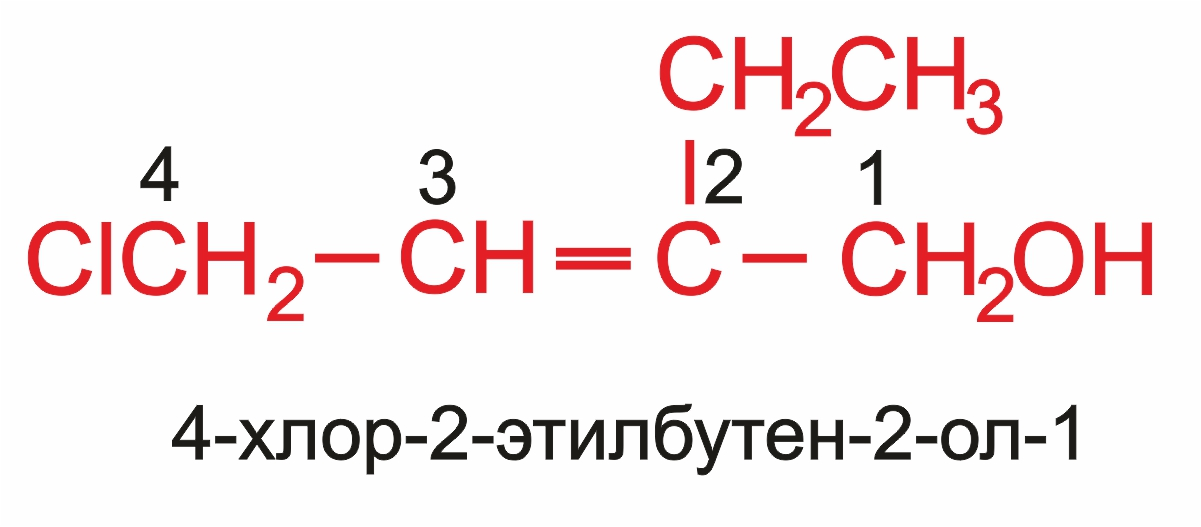
При определении порядка нумерации учитывают, что гидроксильная функция имеет преимущество перед галогеном, двойной связью и алкилом. |
Нумерацию начинают с того конца цепи, ближе к которому расположена гидроксильная группа:
|
|
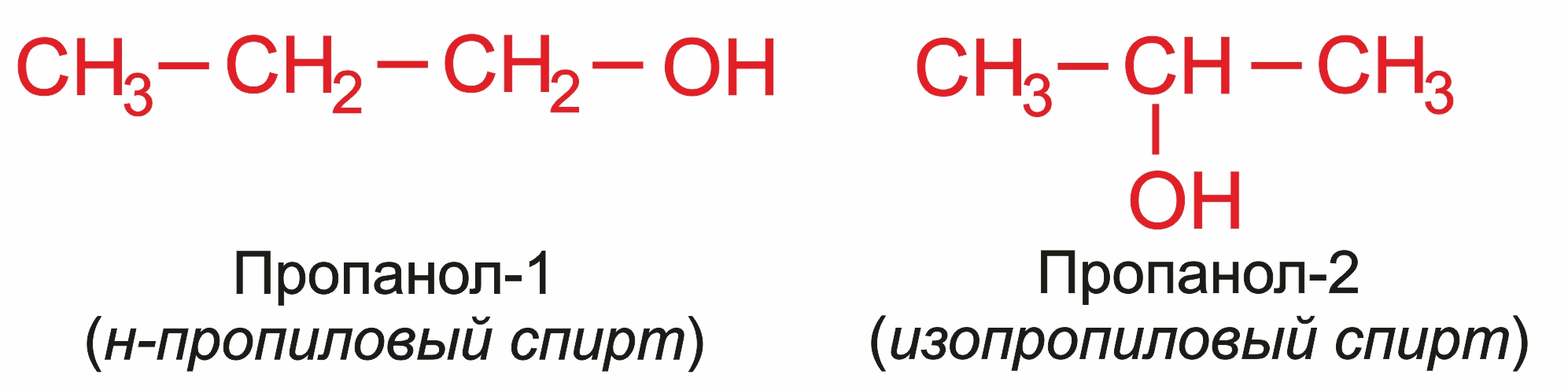
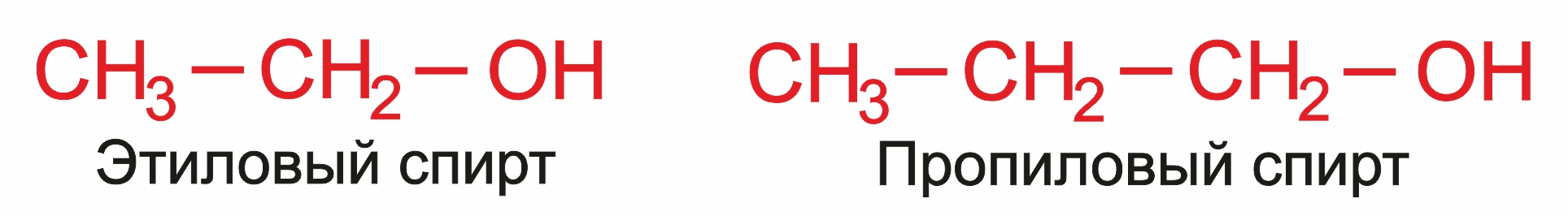
Часто названия простейших спиртов производят от названий радикалов с добавлением окончания –овый и слова спирт:
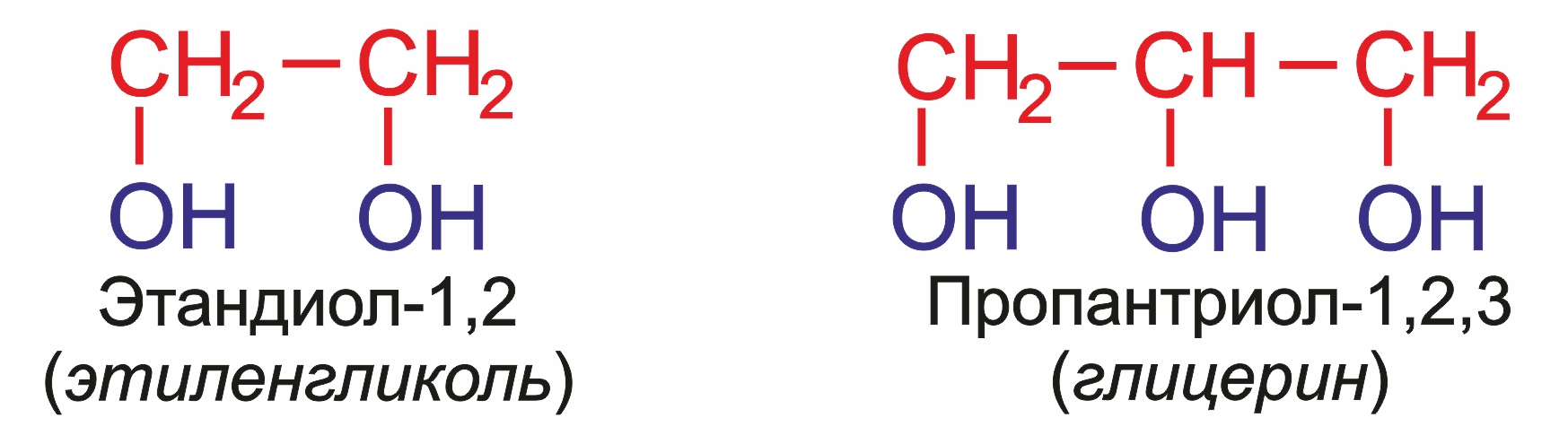
В названиях многоатомных спиртов (полиолов) положение и число гидроксильных групп указывают соответствующими цифрами и суффиксами -диол (две ОН-группы), -триол (три ОН-группы) и т.д.
Например:
1. |
Изомерия положения группы -ОН (начиная с С3);
|
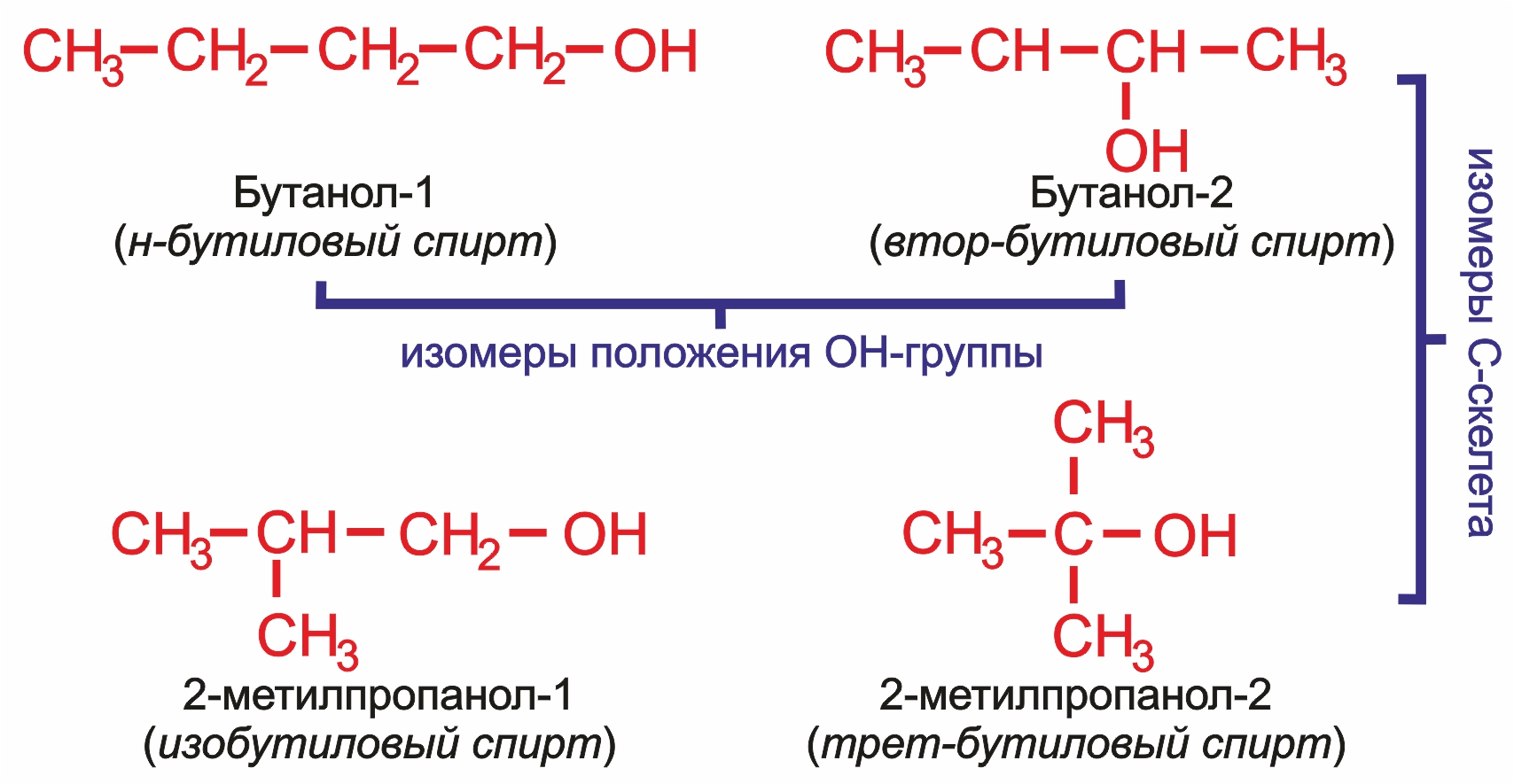
2. |
Изомерия углеродного скелета (начиная с С4). Например, формуле C4H9OH соответствуют 4 структурных изомера:
|
3. |
Межклассовая изомерия с простыми эфирами. Например, молекулярной формуле С2Н6О соответствует и этиловый спирт СН3CH2–OH, и диметиловый эфир CH3–O–CH3. |
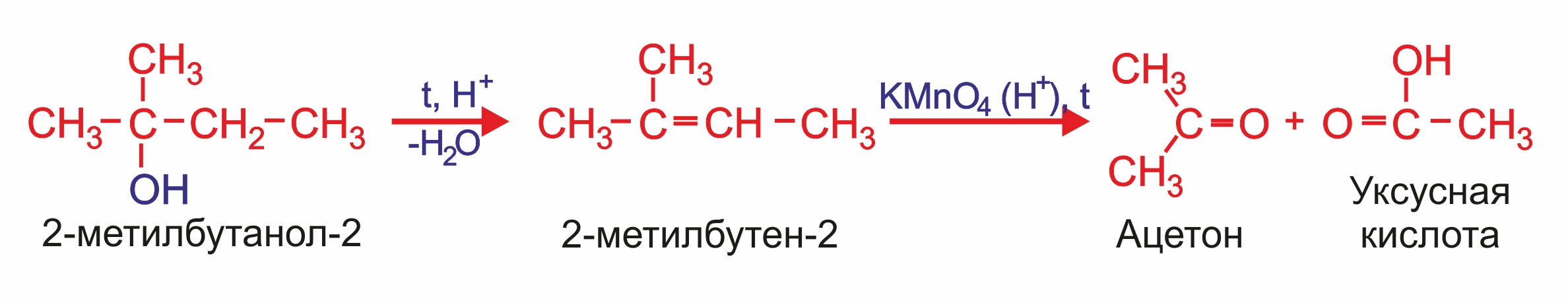
Получение спиртов
1. |
Присоединение воды к несимметричным алкенам идет по правилу Марковникова. |
|
2. |
Действие водного раствора щелочи на галогенопроизводное углеводорода (щелочной гидролиз галогенопроизводных):
|
|
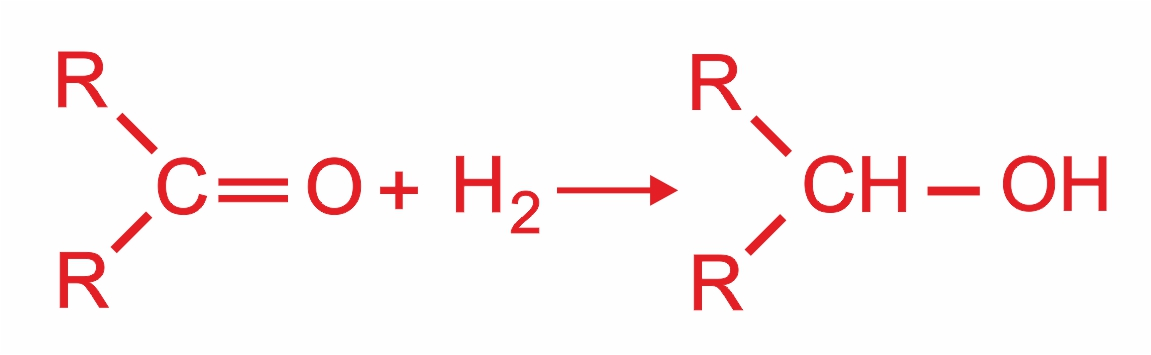
3. |
|
|
4. |
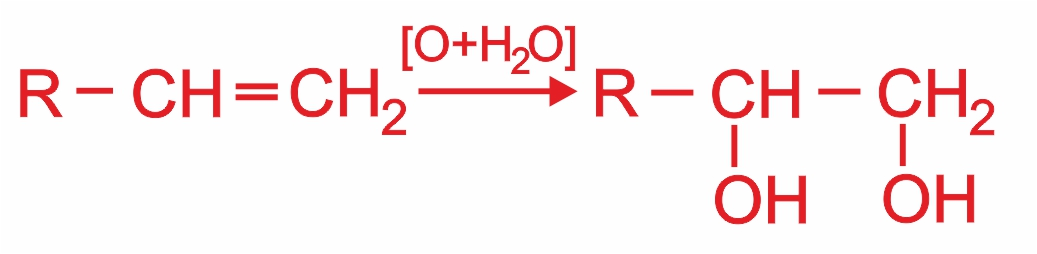
Гликоли получают окислением алкенов щелочным раствором KMnO4 (реакция Вагнера):
|
|
5. |
На практике используют 2 способа: |
|
• |
сбраживание растительного сырья, содержащего крахмал (картофель, рис, пшеница) и последующая перегонка; получают спирт ректификат (медицинский); |
|
• |
гидролиз непищевых продуктов (древесины); при этом получают гидролизный (технический) спирт. |
|
Физические свойства спиртов
От строения углеводородного радикала, количества гидроксильных групп и их положения зависят физические свойства спиртов. Первые представители гомологического ряда спиртов — жидкости, высшие — твердые вещества.
Метанол и этанол смешиваются с водой в любых соотношениях. С ростом молекулярной массы растворимость спиртов в воде падает. Высшие спирты практически не растворимы в воде.
Физические свойства спиртов
Спирты обладают более высокими температурами кипения по сравнению с углеводородами. Это объясняется сильной ассоциацией молекул спирта в жидком состоянии за счет образования водородных связей:
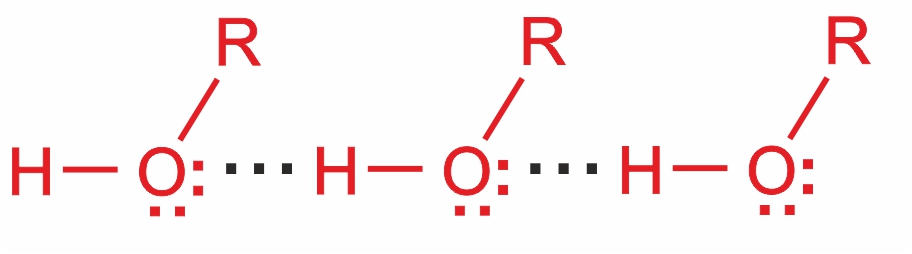
Водородные связи непрочные (17-22 кДж/моль) и при испарении спиртов легко разрываются.
Химические свойства спиртов
В химических реакциях спиртов возможно разрушение одной из двух связей:
• |
С–ОН с отщеплением группы –ОН; |
• |
О–Н с отщеплением водорода. |
Возможны реакции замещения, в которых происходит замена –ОН или –Н, или реакция отщепления (элиминирования), когда образуется двойная связь.
Первый тип реакций — замещение атома водорода в гидроксильной группе (реакции по связи О–Н) |
Алкоголяты под действием воды полностью гидролизуются с выделением спирта и гидроксида металла:

![]() Спирты — более слабые кислоты, чем вода. Поэтому при взаимодействии спиртов со щелочами алкоголяты практически не образуются:
Спирты — более слабые кислоты, чем вода. Поэтому при взаимодействии спиртов со щелочами алкоголяты практически не образуются:

(равновесие этой реакции сдвинуто влево, т.к. соли спиртов в воде гидролизуются)
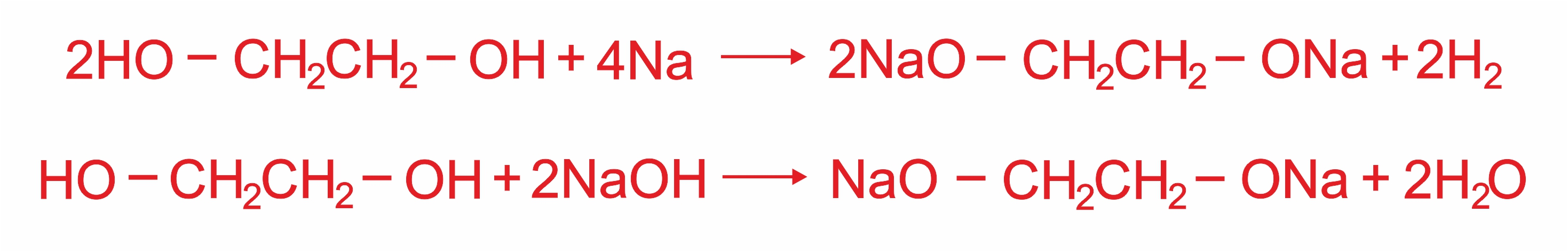
Многоатомные спирты с группами –ОН у соседних атомов углерода (этиленгликоль, глицерин и т.п.) являются более сильными кислотами, чем одноатомные спирты. Они образуют соли не только в реакциях с активными металлами, но и под действием их гидроксидов:
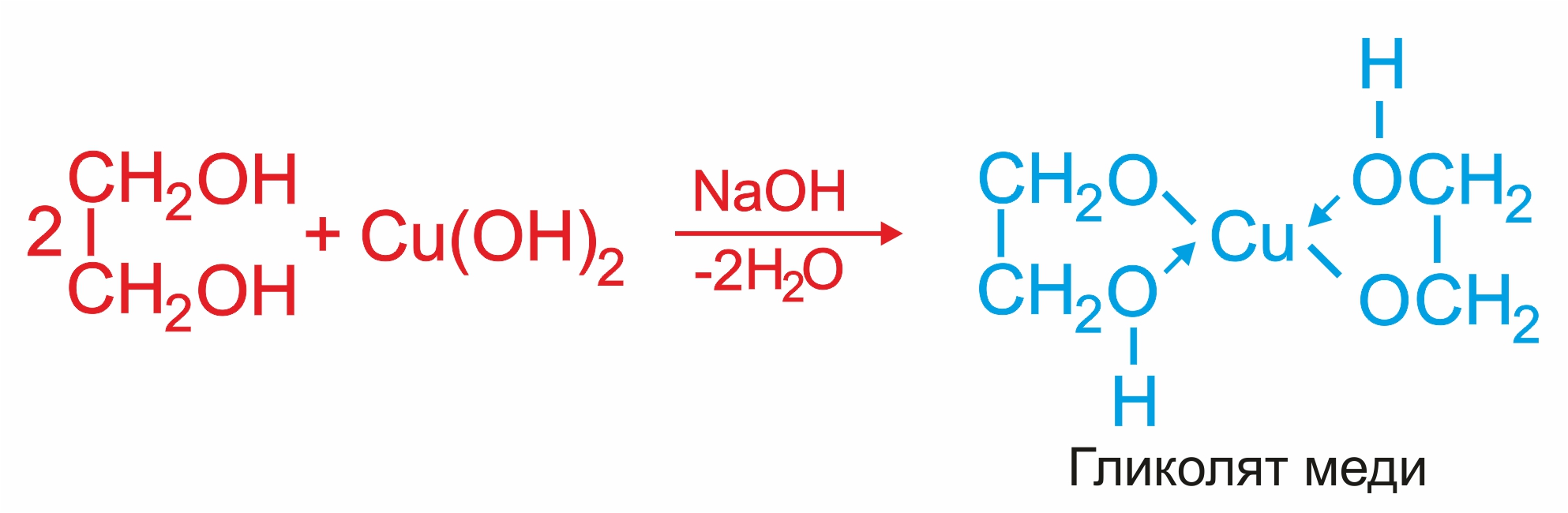
![]() Многоатомные спирты, в отличие от одноатомных, взаимодействуют с раствором гидроксида меди (II) в присутствии щелочи, образуя комплексные соединения, окрашивающие раствор в ярко-синий цвет: качественная реакция на многоатомные спирты.
Многоатомные спирты, в отличие от одноатомных, взаимодействуют с раствором гидроксида меди (II) в присутствии щелочи, образуя комплексные соединения, окрашивающие раствор в ярко-синий цвет: качественная реакция на многоатомные спирты.
![]() Примеры реакций для двухатомного и трехатомного спиртов:
Примеры реакций для двухатомного и трехатомного спиртов:
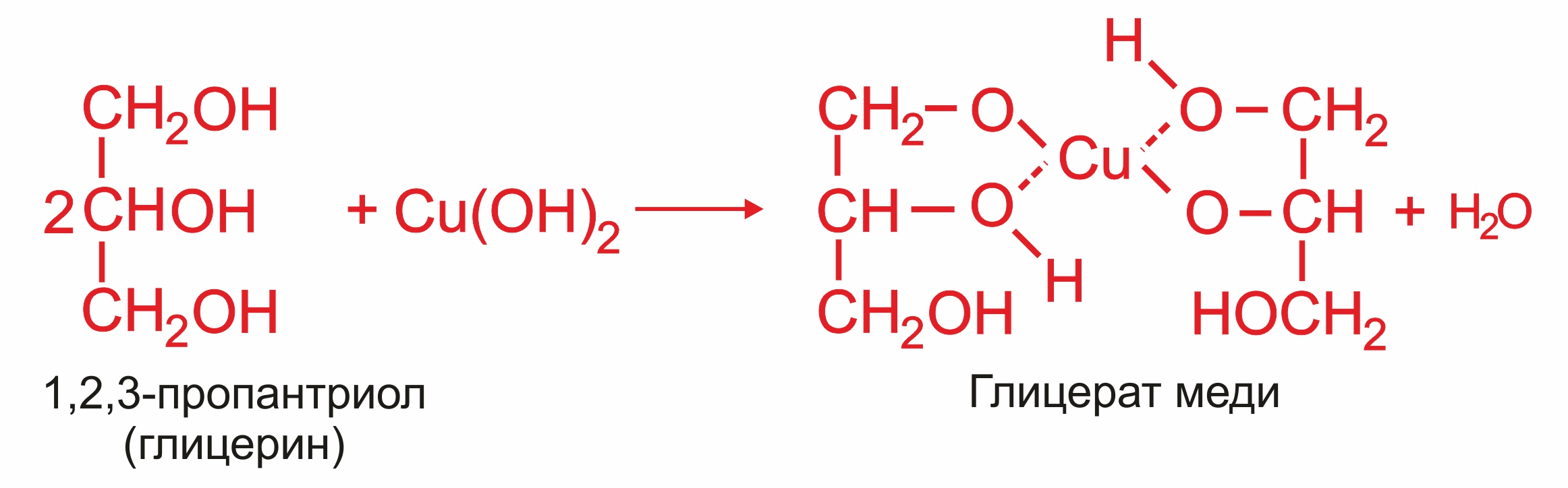
2. |
|
(сложный метиловый эфир уксусной кислоты) |
Данная реакция называется реакция этерификации. Причем кислота может быть как органической, так и неорганической.
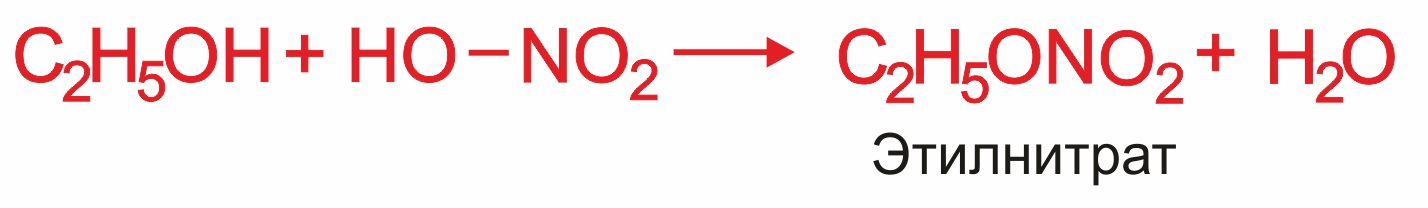
Получение эфиров
3. |
Реакции отщепления водорода при окислении и дегидрировании. |
|
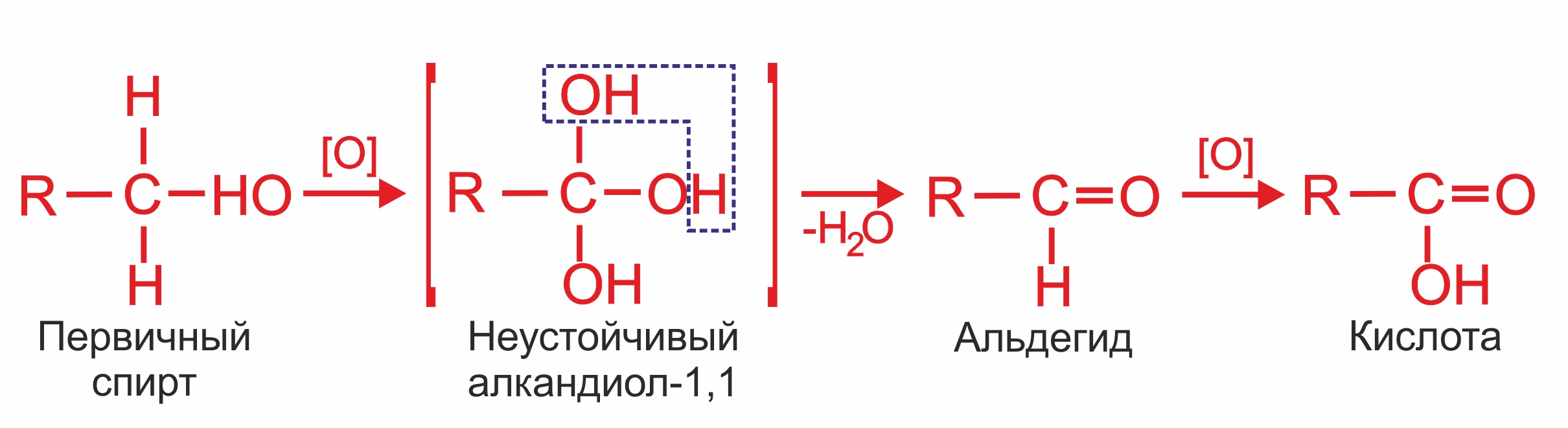
• |
|
|
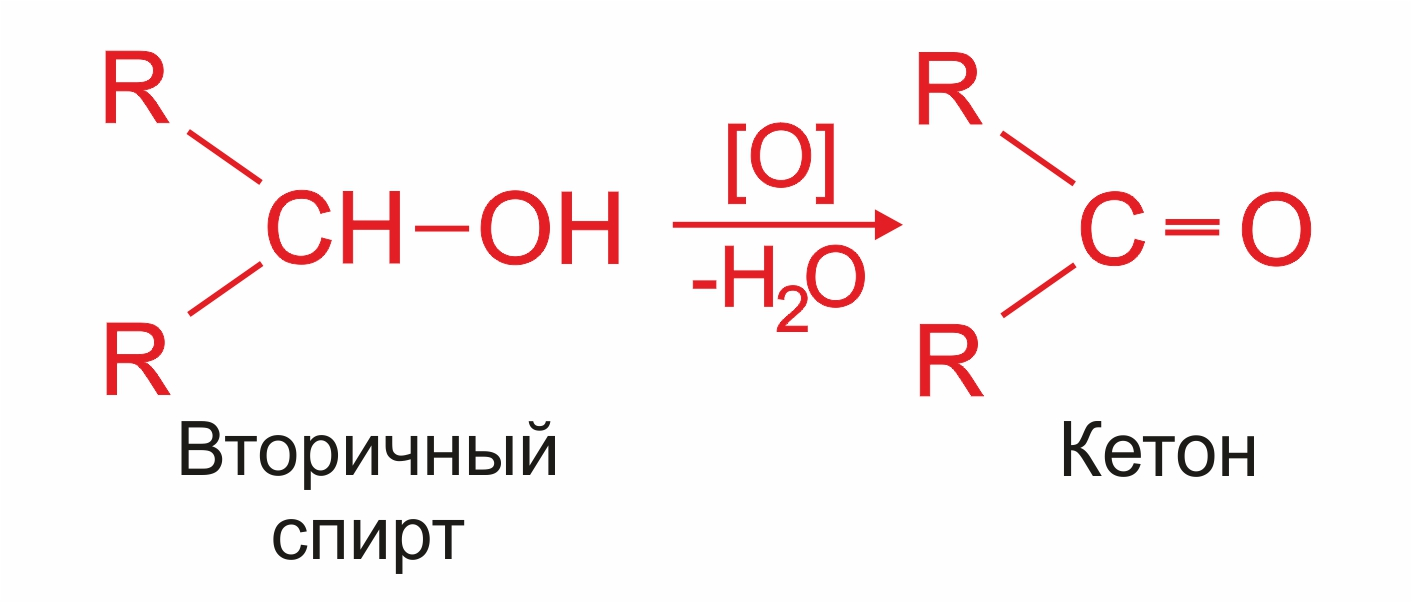
• |
|
|
• |
Третичные спирты более устойчивы к действию окислителей. Они окисляются только в жестких условиях (кислая среда, повышенная температура), что приводит к разрушению углеродного скелета молекулы и образованию смеси продуктов (карбоновых кислот и кетонов с меньшей молекулярной массой).
|
|
Горение спиртов
|
||
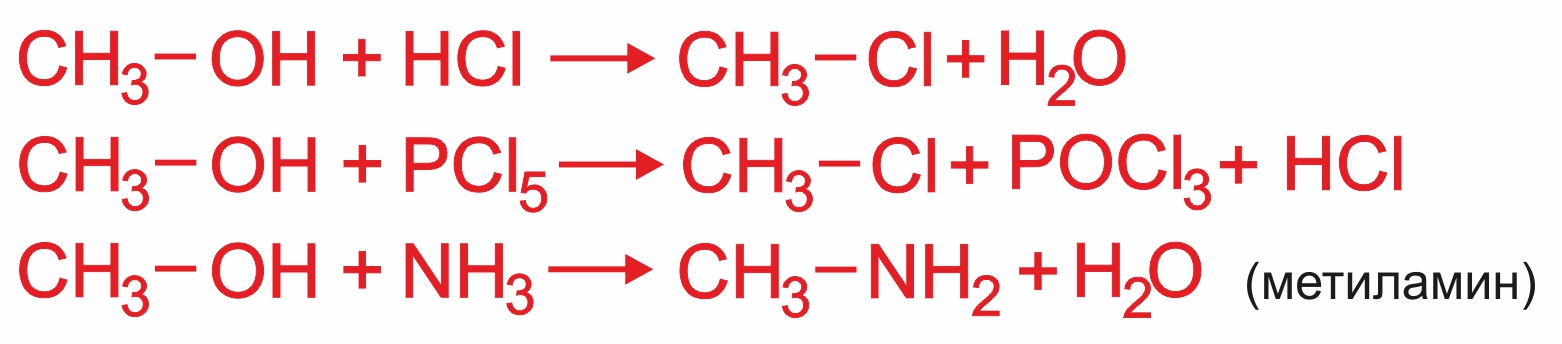
Второй тип реакций — замещение группы –ОН (реакции по связи С–О). |
1. |
|
|
2. |
|
|
• |
Внутримолекулярная дегидратация (в присутствии концентрированной серной кислоты, при повышенной температуре), в ходе реакции образуются алкены.
Реакция внутримолекулярной дегидратации протекает по правилу Зайцева: водород отщепляется от менее гидрогенизированного атома углерода. |
|
• |
|
|
Простые эфиры
Простые эфиры — это органические вещества, молекулы которых состоят из углеводородных радикалов, соединенных атомом кислорода: R–O–R', где R и R' — различные или одинаковые радикалы. |
Простые эфиры — производные спиртов.
Номенклатура простых эфиров
К названиям радикалов добавляется слово эфир. Если радикалы одинаковые, R–O–R, перед названием радикала добавляется приставка ди-, а в названиях несимметричных эфиров R–O–R' радикалы перечисляют, начиная со старшего.
Примеры:
• |
CH3OCH3 — диметиловый эфир; |
• |
C2H5OCH3 — метилэтиловый эфир. |
Получение простых эфиров
1. |
Межмолекулярная дегидратация спиртов:
|
2. |
Взаимодействие алкоголята и углеводорода:
|
Физические свойства простых эфиров
Простые эфиры имеют более низкие температуры кипения и плавления, чем изомерные им спирты. Эфиры практически не смешиваются с водой. Это объясняется тем, что простые эфиры не образуют водородных связей, т.к. в их молекулах отсутствуют полярные связи О–Н.
Химические свойства простых эфиров
Простые эфиры — малоактивные соединения, их реакционная способность гораздо ниже, чем у спиртов. Хорошо растворяют многие органические вещества, и поэтому часто используются как растворители.
Применение спиртов
• |
Метанол и этанол применяются в качестве растворителей и сырья в органическом синтезе. Метиловый спирт — яд, всего 11 мл его вызывают слепоту, а больше — смерть. Этанол используется в пищевой промышленности и медицине. |
• |
Одноатомные высшие твердые спирты встречаются в виде сложных эфиров высших кислот (спермацет, пчелиный, растительный воски). |
• |
Полимеры на основе эфиров виниловых спиртов имеют большое практическое значение. |
• |
Этиленгликоль используется как пластификатор и в производстве синтетических волокон. |
• |
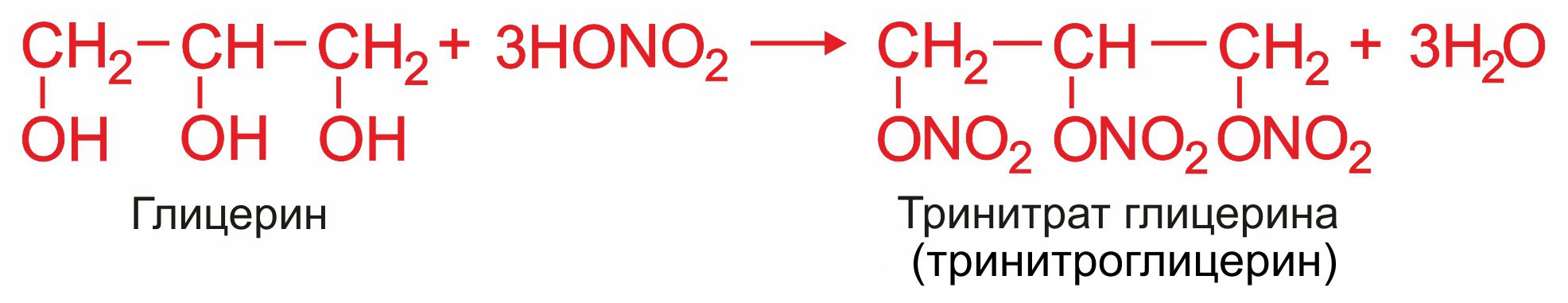
Глицерин широко применяется в парфюмерии, пищевой промышленности, в фармакологии, для получения нитроглицерина, в природных условиях он распространен в виде сложных эфиров с высокомолекулярными карбоновыми кислотами (жиры). |
• |
Многоатомные спирты часто встречаются в природных продуктах (ксилит, сорбит). Многоатомные спирты ряда циклогексана (циклические) также встречаются в природе: кверцит (в желудях), инозит (в семенах многих растений). |
• |
Ненасыщенные спирты являются составной частью эфирных масел растений: цитронеллол — выделен из розового масла, гераниол — из эфирного масла герани, фарнезол — из эфирного масла липы, фитол встречается в природных условиях в виде сложного эфира — хлорофилла — зеленого пигмента растений. |