Экологический мониторинг и экологическая экспертиза

3.4. Определение жесткости воды
|
Определение устранимой (карбонатной) жесткости Санитарная оценка воды по жесткости Трилонометрическое определение жесткости воды |
Жесткостью воды называется суммарное содержание солей кальция и магния в моль-экв./л (Н0). |
Жесткость воды – один из ведущих факторов, обусловливающих развитие биологических объектов в водной среде. Жесткость питьевой воды по ГОСТу должна быть не выше 7 мг-экв/л.
Различают жесткость карбонатную, некарбонатную и общую. Для определения общей жесткости наибольшее применение нашел титриметрический метод анализа. Жесткость воды обусловливается преимущественно присутствием в ней кальция и магния в виде гидрокарбонатов, карбонатов, хлоридов, сульфатов.
При кипячении воды в течение 1 ч жесткость ее заметно уменьшается. Это происходит за счет разрушения гидрокарбонатов кальция и магния до карбонатов, выпадающих в осадок (накипь). Количество, на которое уменьшается общая жесткость после часового кипячения, и составляет устранимую жесткость. Так как последняя бывает почти полностью за счет бикарбонатов, ее еще называют карбонатной жесткостью. После часового кипячения в воде остаются хлориды, сульфаты, частично карбонаты кальция и магния. Они и составляют постоянную жесткость.
Сумма всех солей устранимой и постоянной жесткости составляет общую жесткость. |
При санитарно-гигиенической оценке воды принято считать, что вода с жесткостью выше 10 мг-экв/л, имеющая неприятный вкус, – очень жесткая вода; до 3,5 мг-экв/л – мягкая; от 2,5 до 7 мг-экв/л – средней жесткости; от 7 до 10 мг-экв/л – жесткая. Жесткость воды от 7 до 10 является предельно допустимой по стандарту (ГОСТ 2874-73).
В литературе пока еще встречается оценка общей жесткости, выраженная не только в современных единицах измерения (мг-экв/л), но также и в градусах. За 1° жесткости (немецкий) принимают 10 мг окиси кальция (СаО) в 1 л воды. 1 мг-экв. отвечает содержанию 28 мг окиси кальция и соответствует 2,8° жесткости.
Сейчас широко распространено определение общей жесткости воды при помощи трилона Б. Этот метод требует большего набора реактивов.

0,1 н. раствор соляной кислоты, щелочная смесь, состоящая из равных частей 0,1 н. раствора Nа2СО3 и 0,1 н. раствора NаОН, 0,2%-й раствор метилового красного. Для приготовления 0,1 н. раствора соляной кислоты 3,3 мл крепкой соляной кислоты (уд. масса 1,12) разводят до объема 1000 мл дистиллированной водой.
Устанавливают титр по 0,1 н. раствору NаОН. 1 мл 0,1 н. раствора соляной кислоты соответствует 2,8 мг СаО. Щелочную смесь готовят из равных частей 0,1 н. раствора едкого натра (4 г NаОН на 1 л дистиллированной воды) и 0,1 н. раствора углекислого натра (5,3 г Nа2СО3 на 1 л дистиллированной воды).

- колба емкостью 200-250 мл;
- мерный цилиндр или пипетка на 100 мл;
- две бюретки для титрования; - воронка;
- бумажные фильтры;
- электроплитка.
Определение устранимой (карбонатной) жесткости
В колбу наливают 100 мл исследуемой воды, прибавляют две капли индикатора и титруют 0,1 н. раствором соляной кислоты до появления слабо-розового окрашивания. При титровании имеющиеся в воде бикарбонаты кальция и магния переходят в хлориды с выделением углекислоты по уравнению:
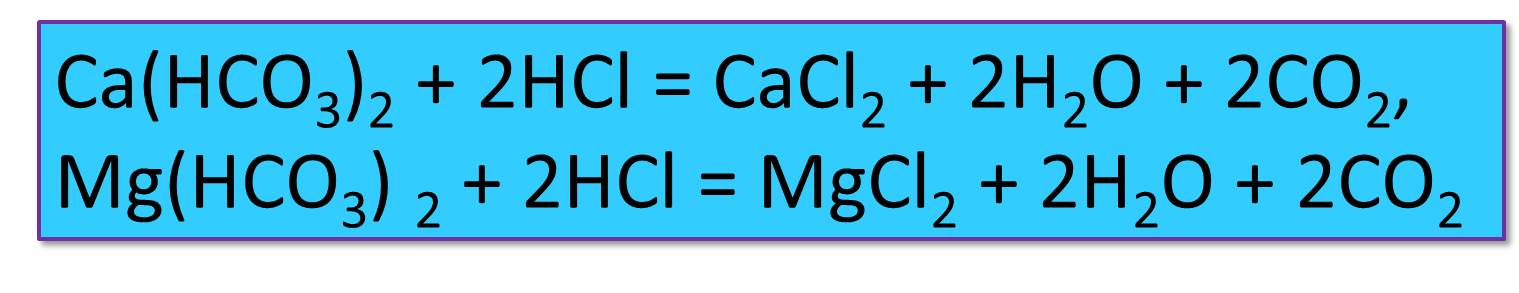
Выше отмечалось, что 0,1 н. раствор НСl, пошедший на титрование, соответствует 2,8 мг СаО.
Это видно из следующего уравнения и расчета:
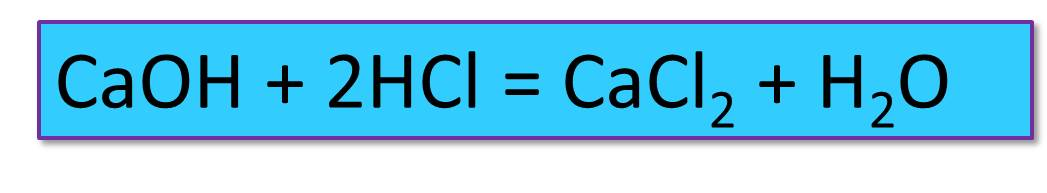
Одна молекула окиси кальция содержит 2 г-экв., а молекулярная масса его равна 56.
Отсюда 1 г-экв. окиси кальция составит 56 : 2 = 28 г.
Поэтому 1 мл 0,1 н. раствора НСl нейтрализует во взятой пробе воды (100 мл) 2,8 мг СаО. Если пересчитать это на 1 л воды, то результат будет равен 28 мг, или 2,8° жесткости. Умножая количество 0,1 н. раствора соляной кислоты (мл) на 2,8, получим показатель количества карбонатной (устранимой) жесткости.

На титрование 100 мл исследуемой воды израсходовано 3,4 мл 0,1 н. раствора соляной кислоты, следовательно, устранимая (карбонатная) жесткость будет равна 3,4 × 2,8 = 9,52° жесткости.
После определения устранимой жесткости в ту же колбу с водой, уже оттитрованной, добавляют из бюретки 20 мл щелочной смеси и кипятят в течение 3 мин. Под влиянием щелочной смеси кальций и магний выпадают в осадок, образуя углекислый кальций и гидрат окиси магния.
После кипячения жидкость охлаждают до 20°С и туда доливают дистиллированную воду до объема 200 мл. Жидкость перемешивают и отфильтровывают 100 мл в чистую мерную колбу.
К отфильтрованной жидкости добавляют 2-3 капли индикатора и титруют 0,1 н. раствором соляной кислоты до слабо-розового окрашивания.
Для титрования было взято только 100 мл воды, количество 0,1 н. раствора соляной кислоты, затраченное на титрование, удваивают, т. е. умножают на 2. Полученное число показывает количество миллилитров щелочного раствора, не вступившего в реакцию. Вычитая это число из 20 мл щелочного раствора, получают количество 0,1 н. раствора соляной кислоты, ушедшей на осаждение солей кальция и магния.
Полученную разность умножают на 2,8 и получают показатель общей жесткости.

На титрование 100 мл фильтрата израсходовано 6,9 мл 0,1н. раствора соляной кислоты. Следовательно, на 200 мл будет израсходовано 13,8 мл (6,9 × 2). Отсюда следует, что из 20 мл щелочной смеси остались неизрасходованными 13,8 мл.
Вычитая это число из 20 мл щелочной смеси, находим количество 0,1 н. раствора соляной кислоты, израсходованной на осаждение солей кальция и магния: 20 – 13,8 = 6,2 мл.
Тогда общая жесткость исследуемой воды будет равна: 6,2 × 2,8 = 17,36°.
Постоянная жесткость представляет собой разность между показателями общей и устранимой жесткости:
общая жесткость – 17,36°, или 6,2 мг-экв/л;
устранимая жесткость – 9,52°, или 3,4 мг-экв/л;
постоянная жесткость – 17,36 – 9,52 =7,84°, или 2,8 мг-экв/л.
Санитарная оценка воды по жесткости
Кроме общей устранимой (карбонатной) и постоянной жесткости, представляют интерес сульфаты (ГОСТ 4389-72). Сульфаты, количество которых в воде превышает 500 мг/л, сообщают воде горько-соленый вкус. Если сульфатов, особенно солей магния, 1000-1500 мг/л, они неблагоприятно влияют на секрецию желудочно-кишечного тракта. Сульфаты могут быть показателем загрязнения водоисточников промышленными сточными водами.
В водопроводной воде содержание 1-5 видов сульфатов не должно быть выше 500 мг/л. Определение сульфатов может быть качественное и количественное.
Качественное определение
Для этого в пробирку берут 5 мл исследуемой воды, подкисляют двумя каплями 10%-го раствора соляной кислоты, прибавляют 5 капель 5%-го раствора хлористого бария. Для приготовления его берут 10 г ВаСl2, растворяют в 200 мл дистиллированной воды и нагревают до кипения.
При наличии сульфатов появляется белая муть из нерастворимого в кислотах серно-кислого бария (BaSO4), что указывает на содержание серно-кислых солей.
Руководствуются следующими показателями: слабая муть, появляющаяся в пробирке с исследуемой водой через несколько минут, указывает на содержание сульфатов от 1,0 до 10 мг/л; слабая муть, появившаяся сразу, – на наличие от 10 до 100 мг/л; сильная муть – 100-500 мг/л. Большой осадок, оседающий на дно пробирки, указывает на наличие в воде сульфатов более 500 мг/л.
Количественное определение сульфатов по методу А. В. Озерова
В стаканчик диаметром 28 мм с плоским дном наливают 10 мл исследуемой воды. Если вода мутная, ее предварительно фильтруют. После этого к воде добавляют две капли 25%-го раствора соляной кислоты и 5 капель 10%-го раствора хлористого бария. С помощью стеклянной палочки исследуемую воду размешивают, ставят стаканчик на специальный шрифт и различают его через слой воды, начиная с самого мелкого шрифта (табл. 5.19).
Таблица 5.19 - Определение сульфатов в воде
(по А. В. Озерову)

Трилонометрическое определение жесткости воды

1. Титрованный раствор трилона Б (0,1 или 0,01 н.) В дистиллированной воде растворяют 18,6 г дигидрата или 16,8 г безводного трилона Б.
Раствор разбавляют в мерной колбе до 1 л. Если раствор мутный, то его следует профильтровать. После фильтрации раствор содержит приблизительно 0,1 н. концентрацию трилона Б. Точное значение титра можно установить по хлориду цинка. (Стандартный раствор ZnCl2 готовят растворением металлического цинка в соляной кислоте (1:1).
2. Аммиачный буферный раствор 10 г хлорида аммония растворяют в дистиллированной воде, добавляют 50 мл концентрированного раствора аммиака. Раствор доводят до 500 мл водой. Раствор следует хранить в плотно закрытой посуде.
3. Индикатор (эриохром черный Т). Растирают в ступке 0,25 г эриохрома черного Т с 50 г хлорида натрия.

1. Коническая колба для титрования.
2. Мерный цилиндр.
3. Пипетка.
4. Бюретка объемом 25 мл с ценой деления 0,05 мл.

Определение общей жесткости проводится в следующей последовательности: к 50 или 100 мл отфильтрованной пробы добавляют 1-2 мл аммиачной буферной смеси (pH 8,5-9,0), сухую смесь индикатора и титруют трилоном Б до перехода окраски из вишневой в синюю.
Общую жесткость рассчитывают по формуле
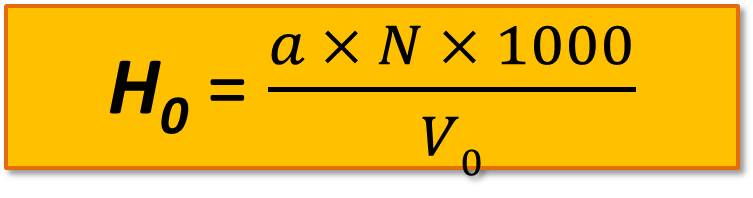
где H0 – общая жесткость, мг-экв/л;
а – количество трилона, мл;
N – нормальность трилона, мг-экв/л;
V0 – объем пробы, мл.
