Экологический мониторинг и экологическая экспертиза

3.2. Окисляемость природных и сточных вод
Общую оценку загрязненности воды, как природной, так и сточной, можно получить по ее окисляемости.
Окисляемость воды – это количество кислорода, необходимое для окисления примесей, содержащихся в одном литре исследуемой воды. |
Окисляемость может быть общей, т.е. может показывать количество всех веществ в воде, органических и минеральных, или «окисляемость с поправкой», если определяется содержание только органических веществ.
В качестве окислителя используют не кислород, а растворы сильных окислителей – перманганата калия или бихромата калия. Полученные результаты пересчитывают и представляют в виде количества кислорода, эквивалентного израсходованному окислителю. В зависимости от применяемого окислителя различают окисляемость перманганатную, бихроматную и др. Выбор метода определения зависит от количества загрязнений в воде и от их природы (органические или минеральные).
Например, для анализа питьевой воды и слабозагрязненных поверхностных вод, окисляемость которых не выше 100 мг О2/л, применяют перманганатный метод.
Для определения общей окисляемости сильнозагрязненных и сточных вод, если окисляемость 100 мг О2/л и более, используют бихроматный метод, т.е. методику для анализа сточных вод с большой концентрацией бихромата калия, а последующее титрование – соответствующим раствором соли Мора.
При использовании кратких модификаций результаты надо периодически проверять унифицированными арбитражными методами.
При определении окисляемости воды, как перманганатной, так и бихроматной, получают условные сведения о качестве воды, указывающие лишь на химическую природу загрязнителей и их косвенное количество по израсходованному окислителю. |
Ответа о качественном составе загрязнителей, присутствующих в воде, окисляемость не дает. Для разных категорий водопользования окисляемость является важным показателем, т.к. дает возможность получить ответ об общем состоянии воды.
Наиболее доступный метод определения окисляемости воды – с помощью титрованного раствора перманганата калия по ГОСТ 4595-49. Титрованный раствор перманганата калия в кислой среде (серная кислота) окисляет органические вещества, переходя в серно-кислый марганец:

Таким образом, окисляемость воды – это то количество кислорода (мг), которое пошло на окисление органических веществ в 1л исследуемой воды. |
Глубоко залегающие подземные воды имеют самую низкую окисляемость – до 1-2 мг О2/л, грунтовые воды – до 2-4 мг О2/л. Воды открытых водоемов сильнее загрязняются органическими веществами, потому их окисляемость может достигать 5-6 и даже 8 мг О2/л. В практике допускается к использованию вода, окисляемость которой достигает 20 мг О2/л, но при условии, что другие показатели соответствуют ГОСТам.
При определении окисляемости воды учитывают наличие в ней хлоридов. Если их в воде менее 300 мг/л, окисляемость устанавливают в кислой среде (серная кислота), если их больше 300 мг/л – в щелочной среде (едкий натр). По нормативам параметры ХПК воды водоемов хозяйственно-питьевого водопользования – 15 мг О2/л, культурно-бытового – 30 мг О2/л.
Бихроматная окисляемость (химическое потребление кислорода – ХПК)
В серно-кислой среде с помощью бихромата калия в присутствии солей серебра (можно взять в качестве катализатора сульфат серебра) при кипячении окисляется большинство органических веществ и часть минеральных. После окисления избыток бихромата находят титрованием раствора соли Мора.
Бихроматную окисляемость называют общей или полной окисляемостью. |
Влияние большого количества хлоридов в анализе можно исключить добавлением в пробу воды сульфата ртути (II).
Если необходимо определить содержание только органических веществ в пробе, то необходимо с помощью других известных методов определить в ней содержание минеральных веществ, а затем эту величину (ее кислородный эквивалент) вычесть из общей окисляемости. Метод позволяет определить окисляемость от 15 мг О2/л и выше при применении 0,1 н. раствора бихромата калия.

Круглодонная колба с обратным холодильником с притертой пробкой.
Колба на 500 мл.
Бюретка.

1. Серная кислота пл. 1,84 г/см3.
2. Сульфат серебра Ag2SO4.
3. Сульфат ртути (II) HgSO4.
4. Бихромат калия, 0,1 н. раствор.
5. Соль Мора, 0,1 н. раствор: 40 г (NH4)2SO4 · FeSO4 · 6H2O растворяют в 20 мл концентрированной серной кислоты. После охлаждения объем раствора осторожно доводят дистиллированной водой до 1 л, вливая раствор с кислотой в воду.
Поправку титра этого раствора устанавливают по титрованному раствору бихромата калия. |
В колбу 500 мл вводят пипеткой 25 мл 0,1 н. титрованного раствора бихромата калия, разбавляют дистиллированной водой до 250 мл, добавляют 20 мл концентрированной серной кислоты пл. 1,84 г/см3 и дают остыть. Добавляют 3-4 капли ферроина или 5-10 капель N-фенилантраниловой кислоты и титруют раствором соли Мора. Раствор бихромата калия 0,25 н. К2Сr2О7 (х. ч.) сушат в чашке Петри в течение 2 ч при 105°С, затем навеску 12,259 г растворяют в 1 л дистиллированной воды. Хранят в емкости из темного стекла без доступа света. Для раствора бихромата калия 0,1 н. К2Сr2О7 пересчитывают навеску, т.е. навеска должна быть в 2,5 раза меньше, чем в первом случае.
6. Индикаторы:
а) ферроин (1,485г 1,10-фенантролина и 0,695 г сульфата железа (II) Fe SO4, 7H2O растворяют в воде и доводят до 100 мл;
б) N-фенилантраниловую кислоту 0,25 г растворяют в 12 мл 0,1 н. гидроксида натрия и разбавляют водой до 250 мл.

Для анализа отбирают 20 мл пробы, помещают ее в круглодонную колбу на 300 мл со шлифом для кипячения. В колбу добавляют 10 мл 0,1 н. раствора бихромата калия и опускают стеклянные шарики. Смесь аккуратно перемешивают и осторожно малыми порциями приливают к ней 30 мл концентрированной серной кислоты. Затем добавляют 0,3-0,4 г сульфата серебра, присоединяют обратный холодильник, нагревают до слабого кипения и кипятят смесь в течение 2 ч.
При этом необходимо следить за цветом кипящего раствора. Если он изменился от золотисто-оранжевого к буро-зеленоватому, то определение необходимо повторить с более разбавленной пробой, т.к. это свидетельствует о недостатке окислителя. Если цвет не изменился, то по истечении указанного времени охлаждают систему, отсоединяют холодильник и приливают в колбу 100 мл дистиллированной воды.
Разогревшуюся смесь вновь охлаждают, обмывают стенки холодильника 25 мл дистиллированной воды. Дают остыть и переносят раствор в коническую колбу на 500 мл. Обмывают первую колбу несколько раз дистиллированной водой, собирая промывные воды в коническую колбу, чтобы объем раствора был около 350 мл. В колбу прибавляют 3-5 капель ферроина или 10-15 капель N-фенилантраниловой кислоты и оттитровывают избыток бихромата калия 0,1 н. раствором соли Мора до перехода окраски в зеленый цвет.
Параллельно проводят опыт с 20 мл дистиллированной воды.
Бихроматную окисляемость ХПК (мг О2/л) рассчитывают по формуле
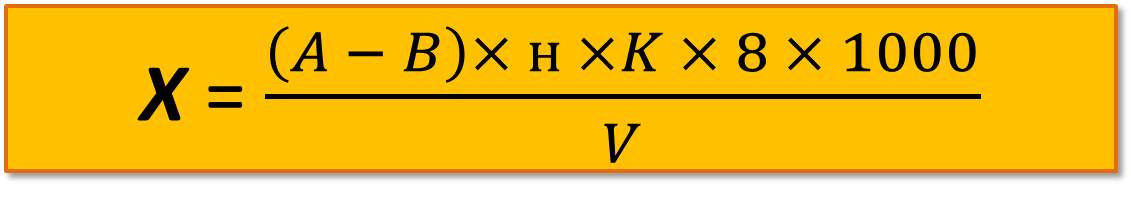
где А – объем раствора соли Мора, израсходованный на титрование пробы, мл;
В – объем раствора соли Мора для титрования холостой пробы, мл;
н – нормальность раствора соли Мора;
К – поправочный коэффициент для раствора соли Мора;
V – объем пробы воды для анализа, мл;
8 – эквивалент кислорода.
Округление результатов производят в зависимости от величины бихроматной окисляемости.
Диапазон ХПК, мг О2/л 100 200 500 1000 2000
Округление с точностью до, мг/л 5 10 15 20 50
Определение окисляемости воды обычных водоемов и очищенных сточных вод
Бихроматную окисляемость всех веществ, ХПК (мг О2/л) малозагрязненных вод проводят, применяя 0,05 или 0,025 н., т.е. меньшую концентрацию бихромата калия, а последующее титрование – соответствующим раствором соли Мора.
Расчет ведут по той же формуле, меняется лишь величина нормальности раствора:
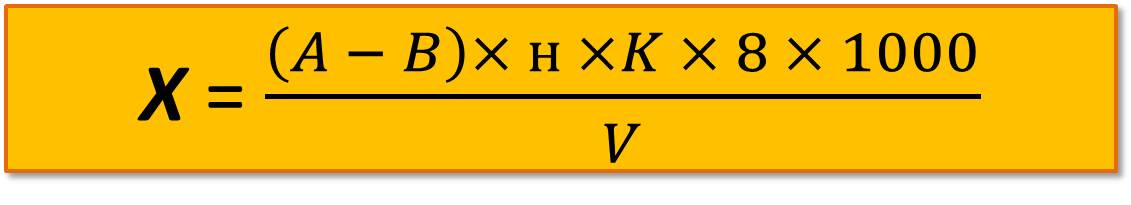
где А – объем раствора соли Мора, израсходованный на титрование пробы, мл;
В – объем раствора соли Мора для титрования холостой пробы, мл;
н – нормальность раствора соли Мора;
К – поправочный коэффициент для раствора соли Мора;
V – объем пробы воды для анализа, мл;
8 – эквивалент кислорода.
Окисление веществ, находящихся в воде в небольших количествах, проводят раствором перманганата калия в серно-кислой среде. |

1. 0,01 н. раствор перманганата калия (КМnО4), молекулярная масса которого 316 (0,316 г КМnО4) доводят дистиллированной водой до 1л, (расчет нормальности перманганата калия см. прил. 18);
2. 0,01 н. раствор щавелевой кислоты (0,63 г ее доводят до 1 л дистиллированной водой;
3. Раствор серной кислоты 1:3 (в колбу со 150 мл дистиллированной воды осторожно по стенкам прибавляют 50 мл концентрированной серной кислоты с удельной массой 1,84).
Реактивы готовят исходя из того, что 1 см3 0,01 н. раствора перманганата калия может выделить 0,08 мг кислорода, в то время как 1 см3 0,01 н. раствора щавелевой кислоты потребует для окисления такого же количества (0,08 мг) кислорода.
Раствор перманганата калия при хранении разлагается и титр его снижается, поэтому перед определением окисляемости воды необходимо предварительно устанавливать его титр.
Для этого в коническую колбу на 250-300 мл наливают 100 мл дистиллированной воды, пипеткой добавляют 5 мл разведенной 1:3 серной кислоты и 8 мл 0,01 н. раствора КМnО4 (из бюретки со стеклянным краном).
Жидкость в колбе кипятят 10 мин, после чего из другой бюретки сразу же вливают точно 10 мл 0,01 н. раствора щавелевой кислоты. Жидкость обесцветится.
Титруют ее 0,01 н. раствором перманганата калия до появления бледно-розового окрашивания. Подсчитывают, сколько миллилитров 0,01 н. раствора КМnО4 пошло на титрование. Количество его, взятое до титрования (8 мл), плюс количество, пошедшее на титрование, и будет соответствовать 10 мл 0,01 н. раствора щавелевой кислоты, на окисление которой расходуется 0,8 мг кислорода.
Пример расчета титра КМnО4
В колбу со 100 мл дистиллированной воды первоначально было влито 8 мл раствора КМnО4. На титрование до появления слабо-розовой окраски пошло еще 2,9 мл КМnО4.
Титр раствора будет равен:
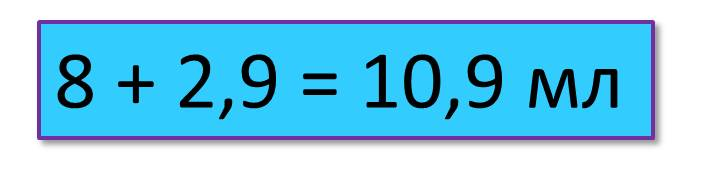
Значит, 10,9 мл 0,01 н. раствора КМnО4 соответствуют 10 мл 0,01н. раствора щавелевой кислоты и выделяют при окислении 0,8 мг кислорода.

Окисляемость воды в кислой среде
В колбу емкостью 250 мл наливают 100 мл исследуемой воды, прибавляют 5 мл разведенной 1:3 серной кислоты в 8 мл 0,01 н. раствора перманганата калия. Можно поместить в колбу стеклянные шарики и колбу закрыть маленькой воронкой.
Раствор кипятят 10 мин от закипания, убирают воронку и сразу же добавляют к нему из бюретки 10 мл 0,01 н. раствора щавелевой кислоты.
В горячем состоянии обесцвеченную смесь титруют 0,01н. раствором КМnО4 до появления бледно-розового окрашивания.
Если цвет становится бурым или происходит обесцвечивание, то воду нужно развести и затем учесть разведение.
Расчет окисляемости воды в кислой среде
Определяют количество раствора КМnО4, израсходованного до кипячения и на титрование после кипячения. Из него находят количество кислорода (мг), пошедшее на окисление 1 л исследуемой воды.

При определении титра 0,01 н. раствора КМnО4 было установлено, что на 10 мл 0,01 н. раствора щавелевой кислоты израсходовано 10,9 мл 0,01 н. раствора КМnО4.
При титровании 100 мл исследуемой воды было израсходовано 14,8 мл (8 + 6,8 мл) 0,01 н. раствора КМnО4.
Таким образом, на окисление органических веществ в 100 мл исследуемой воды пошло 3,9 мл (14,8 – 10,9 = 3,9) 0,01н. раствора КМnО4.
Значит, на титрование 1 л воды пойдет 39 мл 0,01 н. раствора КМnО4.
Рассчитывают количество кислорода, пошедшее на окисление органических веществ в 1 л воды, исходя из того, что 10,9 мл 0,01 н. раствора КМnО4 выделяет 0,8 мг О2, а 39 – х:

В случаях, когда исследуемая вода содержит очень много органических веществ, ее разбавляют дистиллированной водой. Полученный результат умножают на кратность разбавления.
Перманганатная окисляемость методом Кубеля (питьевая вода)
Окисление органических веществ, находящихся в воде, проводят 0,01 н. раствором перманганата калия в сернокислой среде при кипячении. Определяют окисляемость в диапазоне от 0 до 100 мг/л. Без разбавления максимальная определяемая окисляемость составляет 10 мг О2/л.
Определению мешают неорганические соединения (хлориды, сульфиды, нитриты, железо (II)), которые могут окисляться при анализе. Если они присутствуют в анализируемой воде, их количество необходимо определить отдельно и вычесть результат, пересчитанный на окисляемость, из окисляемости пробы воды. 1 мг H2SО4 соответствует 0,47 мг О2; 1 мг NO2 – 0,35 мг О2; 1 мг Fe+2 – 0,14 мг О2. При определении перманганатной окисляемости после реакции должно остаться не менее 40% введенного перманганата калия, так как степень окисления зависит от его концентрации. При большем расходе реагента пробу необходимо разбавлять.

1. Плоскодонные колбы для кипячения вместимостью 250-300 мл, предназначенные только для определения окисляемости. Новые колбы перед употреблением кипятят в кислом растворе перманганата калия.
2. Стеклянные шарики, капилляры или обожженная пемза.

1. Проба анализируемой воды – вода питьевая (отстоенная); проба контрольная – дистиллированная вода.
2. Раствор серной кислоты (1:3): к трем объемам дистиллированной воды добавляют один объем Н2SO4 (х.ч.) (нужно готовить не более 1л). По охлаждении раствора до 40°С к нему прибавляют 0,01н. раствор перманганата калия до слабо-розовой окраски.
3. Перманганат калия 0,1 и 0,01 н. растворы. Основной раствор 0,1 н. готовят, растворяя 3,16 г КМnО4 в 1 л бидистиллята и ставят в темной склянке на 2-3 недели в темное место для отстаивания, изредка перемешивая.
Путем разбавления 0,1 н. раствора в 10 раз готовят 0,01 н. КМnО4.
Берут 100 мл 0,1н. раствора КМnО4 и доводят до 1 л дистиллированной водой. Можно приготовить 0,1н. раствор КМnО4 из фиксанала и развести его в 10 раз. Приготовленный из навески раствор хранят в склянке темного цвета, изредка перемешивая. Используют через 2-3 недели после приготовления. Через несколько дней рабочий раствор титруют для установления титра. Для этого в коническую колбу наливают 100 мл дистиллированной воды, прибавляют 10 мл 0,01н. щавелевой кислоты и 5 мл серной кислоты (1:3).
Можно использовать оттитрованную пробу после определения окисляемости, в этом случае кислоту не прибавляют. Смесь нагревают до кипения и, слегка охладив (до 80-90°С), титруют 0,01н. раствором перманганата калия до появления слабо-розового окрашивания. Если поправка раствора отличается от 1,00 больше чем на 0,05, то раствор соответственно разбавляют или концентрируют.
Нормальность раствора перманганата калия устанавливают в день анализа.
4. Раствор щавелевой кислоты 0,1 н. Для его приготовления кристаллы подсушивают между листами фильтровальной бумаги и оставляют на воздухе на 12 ч. Навеску 6,3024 г щавелевой кислоты (С2Н2О4 + 2Н2О) в литровой колбе растворяют в дистиллированной воде, добавляют 50 мл Н2SO4 (1:3) и общий объем доводят до 1л.
Раствор щавелевой кислоты 0,01 н. готовят, так же как и 0,01 н. раствор КМnО4, путем точного разбавления дистиллированной водой в мерной колбе. 1 мл данного раствора соответствует 0,08 г кислорода.

Для выделения нерастворимых примесей анализируемая вода должна отстояться в течение 2 ч. Затем отбирают 100 мл пробы и помещают в плоскодонную коническую колбу объемом 250 мл, предназначенную только для определения окисляемости, в колбу опускают стеклянные шарики или капилляры.
Новые колбы обрабатывают перед употреблением кипячением в кислом растворе перманганата калия, как это описано при определении поправки раствора перманганата.
Для создания кислой среды приливают 5 мл разбавленной (1:3) серной кислоты, а в качестве окислителя – 10 мл 0,01 н. раствора перманганата калия. Колбу накрывают воронкой и ставят на плитку. Смесь нагревают, она должна закипеть через 5 мин, и кипятят точно 10 мин. При кипении раствора внимательно следят за его окраской.
Если розовое окрашивание перейдет в бурое или раствор обесцветится, это свидетельствует о недостатке окислителя. В таком случае анализ данной пробы прекращается и повторяется сначала, но уже с разбавленной пробой. Если в процессе кипения цвет раствора остается розовым, то по истечении 10 мин колбу снимают с плитки, убирают прикрывающую ее воронку и прибавляют 10 мл 0,01н. раствора щавелевой кислоты. Обесцвеченную горячую (80-90°С) смесь титруют 0,01н. раствором перманганата калия до появления слабо-розового окрашивания.
Для получения точных результатов необходимо, чтобы при титровании концентрированных проб расходовалось не более 7 мл 0,01н. раствора КМnО4, а в случае разбавленных – не менее 2 мл. В противном случае определения рекомендуется повторить, подобрав соответствующие разбавления исследуемой воды. Параллельно проводят холостой опыт со 100 мл дистиллированной воды (разбавляющей), который учитывает поведение окислителя в условиях анализа. При этом расход 0,01 н. раствора перманганата калия не должен превышать 0,2-0,3 мл.
Перманганатную окисляемость (мг О2/л) вычисляют по формуле
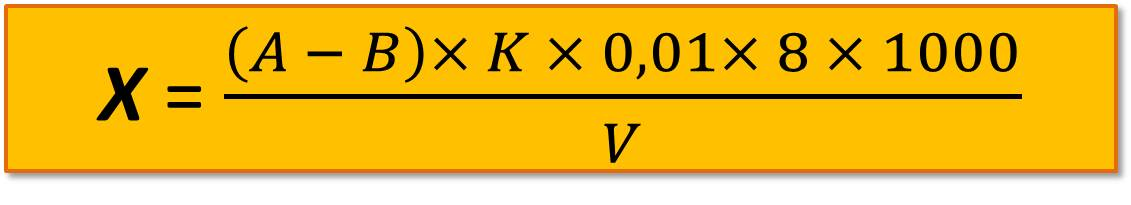
где А – количество 0,01 н. раствора перманганата калия на титрование пробы, мл;
В – количество 0,01 н. раствора перманганата калия на титрование холостой пробы, мл;
К – поправочный коэффициент для раствора перманганата калия (К =1);
V – объем пробы, взятой для анализа, мл;
8 – эквивалент кислорода.
Если поправка к титру перманганата калия имеет значение от 0,995 до 1,005, то при вычислении результатов ее можно не учитывать. |
Результаты определения округляют с точностью до 0,1 мг при значении окисляемости от 0 до 10 мг О2 в 1 л, а от 10 до 100 мг О2 в 1 л – с точностью до 1 мг.
Перманганатная окисляемость с йодометрическим титрованием
Метод основан на окислении присутствующих в воде веществ перманганатом калия в серно-кислой среде с последующим добавлением йодида калия. |
Количество выделившегося йода, эквивалентное непрореагировавшему перманганату калия, титруют тиосульфатом натрия.
После окисления должно остаться около 40% введенного перманганата калия (на титрование должно пойти не более 6 мл 0,01 н. тиосульфата натрия), поскольку степень окисления зависит от его концентрации. При меньшем расходе тиосульфата натрия пробу необходимо разбавлять.
Проведению анализа мешают хлориды (более 300 мг/л), железо, нитриты, сульфиды. При содержании этих ингредиентов меньше 0,1 мг/л их присутствием можно пренебречь. В противном случае их предварительно окисляют при комнатной температуре: к 100 мл исследуемой воды прибавляют 10 мл 0,01 н. перманганата калия, 5 мл серной кислоты (1:3), 0,5 г йодида калия и сразу после растворения йодида титруют выделившийся йод 0,01 н. тиосульфатом натрия. Объем тиосульфата натрия учитывают при расчете окисляемости.

1. Плоскодонные колбы для кипячения вместимостью 250-300 мл, предназначенные только для определения окисляемости. Новые колбы перед употреблением кипятят в кислом растворе перманганата калия.

1. Проба анализируемой воды – вода (отстоенная); контрольная проба – дистиллированная вода.
2. Раствор серной кислоты (1:3): к трем объемам дистиллированной воды добавляют один объем Н2SO4 (х.ч.) (готовить нужно не более 1 л).
3. Перманганат калия 0,1 н. раствор. В 1 л бидистиллята растворяют 3,16 г КМnО4 и ставят в темное место для отстаивания. 0,01 н. КМnО4 готовят путем разбавления 0,1 н. раствора в 10 раз. 100 мл 0,1н. раствора КМnО4 довести до метки 1 л дистиллированной воды.
Можно приготовить 0,1н. раствор КМnО4 из фиксанала и развести его в 10 раз. Приготовленный из навески раствор хранят в склянке темного цвета, изредка перемешивая.
Используют через 2-3 недели после приготовления. Рабочий раствор титруют для установления титра.
4. Тиосульфат натрия, 0,01 н. раствор.
5. Йодид калия кристаллический.
6. Крахмал, 0,5%-й раствор.

В колбу помещают 100 мл исследуемой воды (или меньший объем, разбавленный до 100 мл дистиллированной водой), несколько капилляров, стеклянных шариков или кусочков пемзы, 5 мл разбавленной серной кислоты (1:3), нагревают и в самом начале кипения добавляют 10 мл 0,01 н. перманганата калия, кипятят 10 мин, закрыв маленькой конической воронкой для уменьшения испарения.
Охлаждают, прибавляют 0,5 г йодида калия и выделившийся йод оттитровывают 0,01 н. тиосульфатом натрия да слабо-желтого цвета. В колбу прибавляют 1 мл 0,5%-го крахмала и продолжают, по каплям, титровать раствор до исчезновения синей окраски.
Параллельно проводят определение окисляемости холостой пробы (дистиллированной воды). Величину перманганатной окисляемости (мг О2/л) вычисляют па формуле
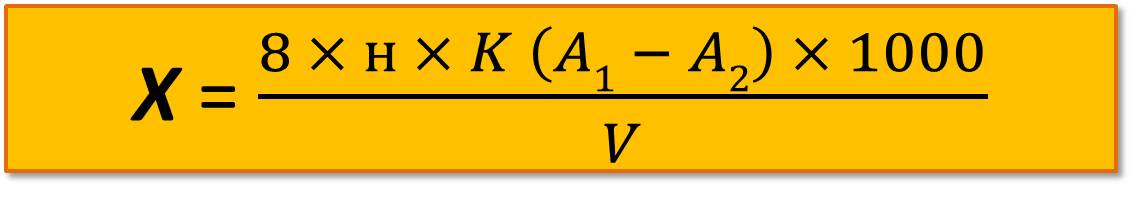
где А1 и А2 – объемы 0,01 н. тиосульфата натрия, израсходованные на титрование холостой и исследуемой пробы, мл;
н – нормальность раствора тиосульфата натрия;
8 – эквивалент кислорода;
V – объем пробы, взятой для определения, мл;
К – поправочный коэффициент к раствору тиосульфата натрия.
