Экологический мониторинг и экологическая экспертиза

3.1. Реакция воды
|
Колориметрическое определение рН воды Количественное определение щелочности или кислотности воды Электрометрическое определение рН |
Природные воды имеют нейтральную реакцию с колебаниями рН в пределах 6-8. Повышенные концентрации гуминовых веществ, свободной углекислоты вызывают кислую реакцию воды, бикарбонатов – щелочную.
При предварительной оценке реакции воды пользуются красной и синей лакмусовыми бумажками. |
Через 5 мин посинение красной лакмусовой бумажки – признак щелочной реакции, покраснение синей – кислой. Если цвет не изменяется, реакция воды нейтральная.
Колориметрическое определение рН воды
Метод основан на том, что при прибавлении к исследуемой воде соответствующего индикатора в зависимости от рН воды он принимает ту или иную окраску, которую сравнивают со шкалой стандартных буферных растворов. Окраску сравнивают в тени или при рассеянном освещении на белом фоне, держа пробирки перед собой на расстоянии 25 см в слегка наклонном положении. Вода часто имеет желтую окраску и мутность, что мешает колориметрическому определению рН. В этом случае нужен компаратор.
В передний ряд компаратора помещают первый буферный раствор с индикатором и исследуемую воду с индикатором, во второй – буферный раствор с индикатором. На задний ряд помещают исследуемую и дистиллированную воду. Окраски просматривают сбоку, через горизонтальные отверстия компаратора.
А. Определение рН воды универсальным индикатором в пределах от 2 до 10

Универсальный индикатор: в 50 мл абсолютного спирта растворяют 0,01 г фенолфталеина, 0,02- метилового красного, 0,03 - диметиламиноазобензола, 0,04 – бромтимолблау и 0,05г тимолблау. Затем в жидкость добавляют 0,1н. раствор NaOH до ясного зеленого окрашивания (от капли до 1 мл).

2 мл воды наливают в пробирку или фарфоровую чашку. Добавляют 2 капли универсального индикатора. При рН 2 вода приобретает красный цвет, при рН 4 – оранжевый, при рН 6 – желтый, при рН 8 – зеленый, при рН 10 – синий.
Б. Определение рН воды универсальным индикатором в пределах от 5 до 8,5

- бромтимоловый синий
- метиловый красный.
Для подщелачивания индикатора готовят гидроксид калия, 0,01 н. раствор.
Универсальный индикатор:
а) отвешивают 0,04 г бромтимолового синего, растирают в агатовой ступке или на часовом стекле стеклянным пестиком с 6 мл 0,01 н. раствора гидроксида калия. Навеску смывают 20 мл этанола в мерную колбу на 100 мл, затем дистиллированной водой ополаскивают ступку или стекло в колбу, доводя объем до 100 мл;
б) отвешивают на аналитических весах 0,01 г метилового красного, растирают с 3,5 мл 0,01 н. раствора гидроксида калия. Навеску смывают в мерную колбу вместимостью 50 мл сначала 10 мл этанола, а затем дистиллированной водой, доводя объем до метки.
Оба раствора сливают вместе. Полученный индикатор пригоден для определения рН в интервале от 5 до 8,5, т. е. в пределах, которые наиболее характерны для большинства природных вод.
Шкала фосфатных буферных растворов
Для приготовления буферных растворов используют бидистиллированную воду, не содержащую углекислоты (свежепрокипяченную и охлажденную).
а) Дигидроортофосфат калия применяют квалификации х. ч. для рН-метрии. КН2РО4 квалификации х. ч. дважды перекристаллизовывают. Растворяют 9,078 г препарата в мерной колбе вместимостью 1 л в дистиллированной воде и доводят объем до метки той же водой.
б) Гидроортофосфат натрия Na2HPО4 квалификации х. ч. дважды перекристаллизовывают. Растворяют 0,472 г препарата в мерной колбе вместимостью 1 л в дистиллированной воде и доводят объем той же водой до метки.
Буферные растворы хранят в плотно закрытых полиэтиленовых склянках в прохладном месте. Необходимые буферные смеси готовят по мере надобности (табл. 5.15).
Таблица 5.15 - Состав буферных растворов
рН буферного раствора при 20°С |
Объем раствора, мл |
рН буферного раствора при 20°С |
Объем раствора, мл |
||
дигидроорто-фосфат тофосфат ккалия |
гидроорто-фосфат натрия |
дигидроорто-фосфат калия |
гидроорто-фосфат натрия |
||
5,29 |
9,75 |
0,25 |
6,81 |
5 |
5 |
5,59 |
9,50 |
0,5 |
6,98 |
4 |
6 |
5,91 |
9 |
1 |
7,17 |
3 |
7 |
6,24 |
8 |
2 |
7,38 |
2 |
8 |
6,47 |
7 |
3 |
7,73 |
1 |
9 |
6,64 |
6 |
4 |
8,04 |
0,5 |
9,5 |
В полевых условиях можно применять также пленочные или нарисованные имитирующие шкалы.

В пробирку наливают 5 мл исследуемой воды, добавляют 0,1 мл универсального индикатора, перемешивают и сравнивают со шкалой буферных растворов, к которым прибавлено также 0,1 мл индикатора на 5 мл раствора. Пробирки просматривают сверху на белом фоне. Приближенное значение рН в соответствии с окраской исследуемой воды:
Розовато-оранжевая – 5
Светло-желтая – 6
Светло-зеленая – 7
Зеленовато-голубая – 8
В. Определение рН с набором индикаторов
Для исследования природных вод рекомендуют следующий набор индикаторов и буферных растворов.

1. Набор индикаторов:
а) Метиловый красный для рН от 4,4 до 6,2. Растворяют 0,1 г препарата при нагревании на водяной бане в 50 мл этанола и доводят объем до 100 мл дистиллированной водой. Переход окраски из красной в желтую.
б) Бромтимоловый синий для рН от 6,0 до 7,6. Растворяют 0,1 г препарата в 50 мл этанола и доводят объем до 100 мл дистиллированной водой. Переход окраски из желтой в синюю.
в) Крезоловый красный для рН от 7,2 до 8,8. Растворяют 0,1 г препарата в 50 мл этанола и доводят объем до 100 мл дистиллированной водой. Переход окраски из желтой в красную.
г) Тимоловый синий для рН от 8 до 9,6. Растворяют 0,1 г препарата в 50 мл этанола при нагревании на водяной бане и по охлаждении доводят объем до 100 мл дистиллированной водой. Переход окраски из желтой в синюю.
Во все индикаторы добавляют 0,1 н. раствор гидроксида натрия или хлористоводородной кислоты до получения окраски переходного цвета.
2. Буферные растворы:
Для их приготовления применяют бидистиллированную воду без углекислоты (свежепрокипяченную и охлажденную). Фосфатные растворы – рН 5,3-8,0. Приготовление см.в прил.17.
3. Борно-щелочные растворы
а) Хлорид калия, 0,1 н. раствор. КСl квалификации х. ч., дважды перекристаллизовывают и высушивают при температуре не выше 120°С. Растворяют 7,456 г препарата в мерной колбе на 1 л в дистиллированной воде и доводят объем до метки этой же водой.
б) Борная кислота квалификации х. ч., дважды перекристаллизованная из кипящей дистиллированной воды, высушенная при температуре не выше 80°С до постоянной массы. Растворяют 6,2 г Н3ВО3 в мерной колбе вместимостью 1 л в 0,1 н. растворе хлорида калия и доводят объем до метки этим же раствором.
в) Гидроксид натрия, 0,1 н. раствор. В мерной колбе вместимостью 1 л в дистиллированной воде растворяют 4 г NaOH квалификации х. ч. и доводят объем до метки той же водой.
Хранят растворы в плотно закрытых склянках в прохладном месте. Борно-щелочные растворы готовят по мере необходимости (табл. 5.16).
Таблица 5.16 - Состав борно-щелочных буферных растворов
рН при 20°С |
Объем растворов, мл |
рН при 20°С |
Объем растворов, мл |
||
борная кислота в 0,1н. |
борная кислота в 0,1н. |
||||
хлориде калия |
гидроксиде натрия |
хлориде калия |
гидроксиде натрия |
||
8,2 |
9,05 |
0,95 |
9,2 |
6,60 |
3,40 |
8,4 |
8,64 |
1,36 |
9,4 |
6,10 |
3,90 |
8,6 |
8,15 |
1,85 |
9,6 |
5,83 |
4,17 |
8,8 |
7,60 |
2,40 |
9,8 |
5,57 |
4,43 |
9,0 |
7,05 |
2,95 |
10,0 |
5,35 |
4,65 |
Приготовление шкалы
В пробирки вносят по 10 мл буферных растворов и по 5 капель индикатора. Пробирки закрывают пробками, можно резиновыми, предварительно прокипяченными. Для каждого индикатора готовят отдельную шкалу буферных растворов в интервале, в котором может работать данный индикатор.
Для полевых исследований можно использовать пробирки меньшего объема, брать 3 мл раствора и прибавлять 3 капли индикатора.
Шкалу хранят в темном месте в деревянном ящике, где имеются гнезда для пустых пробирок и капельницы для индикаторов. Пробирки должны быть одного стекла и одного размера для шкалы и исследуемой воды. К стандартной шкале и исследуемой пробе следует прибавлять индикатор одной и той же партии приготовления и из одной и той же капельницы. Шкала не изменяется в течение нескольких месяцев при хранении в темноте.

Исследуемую воду вносят в пробирку в количестве 10 или 3 мл и прибавляют 5 или 3 капли индикатора, перемешивают и сравнивают со шкалой буферных растворов того интервала, для которого предназначен данный индикатор. Если окраска пробирки выходит за пределы шкалы, то определение повторяют, взяв соседний индикатор. Если окраска исследуемой воды совпадает с окраской одной из пробирок шкалы, то значение ее рН считают рН воды.
Если окраска в пробирке является промежуточной между двумя пробирками шкалы, то значение рН воды находят интерполяцией.
Для санитарных исследований температурные поправки можно не учитывать, а среднюю солевую поправку для вод с минерализацией до 1000 мг/л принимать равной 0,2; 1000-2000 мг/л – 0,1; 2000-3000 мг/л – равной 0. Величину поправки следует прибавлять к найденной рН исследуемой воды.
Количественное определение щелочности или кислотности воды
Под щелочностью понимают способность некоторых компонентов, содержащихся в воде, связывать эквивалентное количество сильной кислоты.
Количество раствора кислоты, необходимое для достижения рН 8,3, эквивалентно свободной щелочности, а для достижения рН 4,5 – общей щелочности. При рН воды меньше 4,5 ее щелочность равна нулю.
Кислотностью называют содержание в воде веществ, вступающих в реакцию с гидроксил-ионами. |
Расход гидроксил-ионов выражает общую кислотность воды, которая зависит от содержания в воде свободного диоксида углерода, а также гуминовых и других слабых органических кислот. В этих случаях рН воды не бывает ниже 4,5. В загрязненных водоемах рН воды может быть ниже 4,5. Часть общей кислотности, снижающей рН ниже 4,5, называется свободной.
Таким образом, количество титрованного раствора, израсходованного до получения рН 4,5, соответствует свободной кислотности; количество же, израсходованное до получения рН 8,3, – общей. Если рН воды больше 8,3, то ее кислотность равна 0.

1. 0,1н. раствор соляной кислоты (3,65 г НСl, до 1 л дистиллированной воды).
2. Раствор 0,1 н. едкого натра (4,0008г NaOH до 1л дистиллированной воды).
3. Фенолфталеин, 0,5%-й раствор. В 50 мл 96%-го этанола растворяют 0,5 г фенолфталеина и разбавляют 50 мл дистиллированной воды, добавляют по каплям 0,01 н. гидроксид натрия до появления заметной розовой окраски.
4. Метиловый оранжевый индикатор, 0,05%-й раствор.
5. Смешанный индикатор. В 150 мл 96%-го этанола растворяют 0,03 г метилового красного и 0,2 г бромкрезолового зеленого и рН раствора устанавливают так, чтобы индикатор имел грязно-серую окраску.

Для более точного определения рН воду нужно профильтровать.
Свободная щелочность
В химический стакан наливают 100 мл исследуемой воды, добавляют 0,1 мл (2 капли) индикатора 0,5%-го фенолфталеина и титруют на белом фоне 0,1 н. раствором соляной кислоты до полного обесцвечивания.
Общая щелочность
К 100 мл воды прибавляют 0,15 мл (3 капли) смешанного индикатора или 0,1мл (2 капли) метилового оранжевого, затем продувают воздух в течение 2-3 мин и титруют 0,1 н. соляной кислотой до момента, когда зеленая окраска смешанного индикатора перейдет в грязно-серую (или до начала перехода окраски метилового оранжевого из желтой в оранжевую), вновь продувают воздух в течение 2-3 мин, и если возвращается первоначальная окраска, то раствор дотитровывают. Расчет свободной (Р) и общей (М) щелочности (мг-экв/л) проводят по формулам
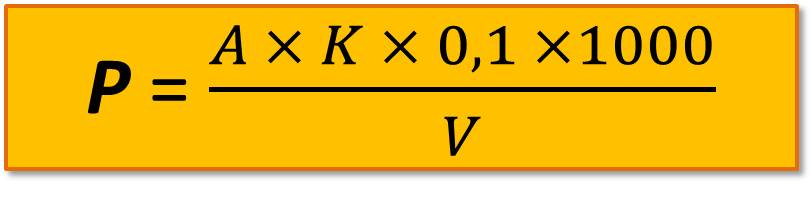
или
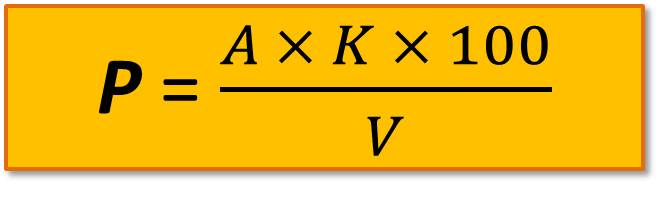 ;
;
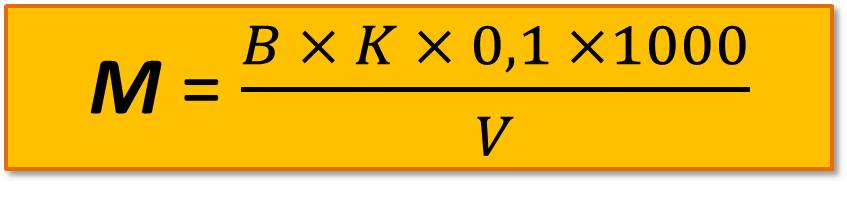
или

где А – объем 0,1 н. хлористоводородной кислоты, израсходованной на титрование по фенолфталеину, мл;
В – то же по смешанному индикатору или метиловому оранжевому, мл;
К – поправочный коэффициент к 0,1 н. раствору хлористоводородной кислоты;
V – объем пробы, взятой для определения, мл.
Свободная кислотность
Определяется, если рН пробы менее 4,5 (кислая реакция по метиловому оранжевому), т.е. проба содержит свободную кислоту. Свободная кислота не определяется, если проба содержит гидролизованные соли сильных кислот и слабых гидроксидов.
К 100 мл пробы добавляют 0,1 мл (2 капли) метилового оранжевого и титруют на белом фоне 0,1 н. раствором гидроксида натрия до появления желтой окраски индикатора.
Общая кислотность
К 100 мл пробы добавляют 0,15 мл (3 капли) фенолфталеина и титруют на белом фоне 0,1 н. раствором гидроксида натрия до появления розовой окраски индикатора. Расчет свободной (С и общей (О) кислотности (мг-экв/л) проводят по формулам
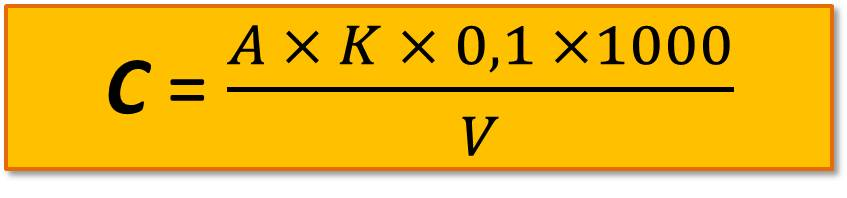
или
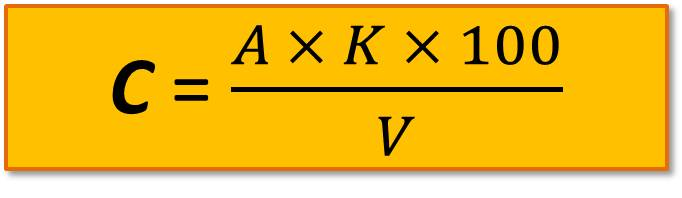 ;
;
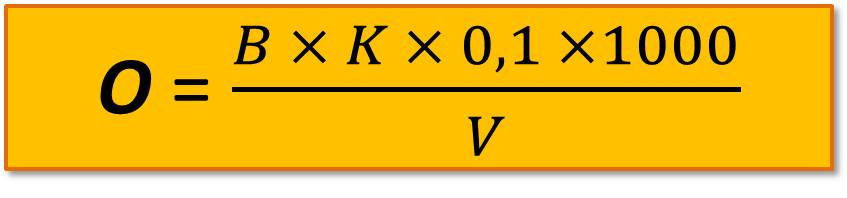
или

где А – объем 0,1 н. гидроксида натрия, израсходованного на титрование по метиловому оранжевому, мл;
В – то же по фенолфталеину, мл;
К – поправочный коэффициент к 0,1 н. раствору гидроксида натрия;
V – объем пробы, взятой для определения, мл.
Электрометрическое определение рН
Электрометрический (потенциометрический) метод определения рН воды отличается большой точностью (до 0,02). Определению не мешают окраска, мутность, свободный хлор, окислители, восстановители, повышенное содержание солей. Влияние температуры воды компенсируется специальным устройством, вмонтированным в прибор.
При анализе сильно загрязненных вод могут мешать жиры, минеральные масла, смолы, оседающие на поверхности электрода. В этом случае электроды следует промывать ватным тампоном, смоченным диэтиловым эфиром, затем раствором моющего средства, после этого несколько раз ополоснуть дистиллированной водой.

Потенциометры (рН-метры) любой модели со стеклянным и хлорсеребряным электродом.
Стеклянный электрод перед работой выдерживают 8 ч в 0,01 н. растворе хлористоводородной кислоты. Перед измерением его несколько раз ополаскивают дистиллированной водой. Стеклянный электрод должен быть прокалиброван по буферным растворам (прил. 12).

Включают pН-метр, после прогрева корректируют «электрический нуль». Затем проверяют по 2-3 буферным растворам крутизну электродной функции. Измеряют рН буферного раствора, спустя 2-5 мин повторяют измерение. Значения рН буферных растворов для корректировки шкалы приведены в табл. 5.17.
Таблица 5.17 - рН буферных растворов при различной температуре
Температура, °С |
рН буферных растворов |
||
бифталатного |
фосфатного |
тетраборатного |
|
0 |
4,01 |
6,98 |
6,46 |
5 |
4,00 |
6,95 |
6,39 |
10 |
4,00 |
6,92 |
9,53 |
15 |
4,00 |
6,90 |
9,27 |
20 |
4,00 |
6,88 |
9,22 |
25 |
4,01 |
6,86 |
9,18 |
30 |
4,01 |
6,85 |
9,14 |
35 |
4,02 |
6,84 |
9,10 |
Если оба значения совпадают, то потенциал электрода считают установившимся и приступают к коррекции шкалы в соответствии с инструкцией. Аналогично поступают с другими буферными растворами. Электрод между измерениями ополаскивают дистиллированной водой, снимают капли ее чистой фильтровальной бумагой и ополаскивают небольшими порциями нового буферного раствора. После проверки и корректировки прибора электроды, термометр и стаканчик ополаскивают дистиллированной водой. Наливают в стакан анализируемую воду и измеряют рН 2-3 раза с интервалом 2-3 мин. Последние два показания прибора должны быть одинаковыми. Если исследуемая вода имеет низкую температуру (около 0°С), то она должна быть нагрета до комнатной, иначе стрелка pН-метра будет плыть, пока не установится комнатная температура.
