Работа 10.21
Определение удельной электрической проводимости
Международный стандарт ИСО-1126 устанавливает определение удельной электрической проводимости водного экстракта почвы следующим методом.
Сущность метода заключается в экстрагировании воздушно-сухой пробы почвы водой с последующим определением удельной электрической проводимости профильтрованного экстракта.
Приборы и оборудование: прибор для измерения удельной электрической проводимости, оборудованный ячейкой с регулированием температуры, который должен обеспечивать точность измерения 1 мСм/м, и иметь устройство для корректирования постоянной ячейки; аналитические весы с точностью взвешивания не менее 0,01 г; механический встряхиватель для приготовления суспензии почвы в воде (рекомендуется применять встряхиватель, делающий около 180 циклов в минуту с ходом около 5 см); термометр с точностью измерения до 0,01°С; плотный беззольный фильтр.
Реактивы. При определении используют дистиллированную воду и реактивы только аналитического качества:
1) раствор хлорида калия I, с (КСl)=0,1 моль/л. Растворяют в воде 7,456 г хлорида калия, высушенного 24 ч при 220±10°С, и доводят водой до 1 л при 20°С. Удельная электрическая проводимость раствора при 25°С должна составлять 1290 мСм/м;
2) раствор хлорида калия II, с (КСl)=0,0200 моль/л. 200 мл раствора хлорида калия 1 помещают в мерную колбу на I л и доводят водой до I л при 20 °С. Удельная электрическая проводимость раствора при 25 °С должна составлять 277 мСм/м;
3) раствор хлорида калия III, с (КСl) = 0,0100 моль/л. 100 мл раствора хлорида калия 1 помещают в мерную колбу объемом 1 л и доводят водой до I л при 20°С. Удельная электрическая проводимость раствора при 25°С должна составлять 141 мСм/м.
Bсe растворы хлорида калия, используемые для калибровки, хранят в плотно закрытых сосудах, материал которых не влияет на электропроводность указанных pacтворов.
Методика определения. Для определения используют воздушно-сухую пробу почвы с размером частиц менее 2 мм после предварительной обработки по ИСО 11464.
Навеску 20,0 г полученной пробы помещают в полиэтиленовую колбу объемом 250 мл (или в колбу из боросиликатного стекла), добавляют 100 мл воды при температуре 20±1 °С. Колбу закрывают, помещают в горизонтальном положении на механический встряхиватель и включают прибор на 30 мин. Затем полученную суспензию фильтруют через плотный беззольный фильтр. Аналогично проводят холостой опыт. Удельная электрическая проводимость фильтрата холостой пробы не должна превышать 1 мСм/м. Если полученная удельная электрическая проводимость холостой пробы превышает указанную величину, экстракцию пробы почвы водой повторяют.
Примечания:
1. Полученный объем фильтрата должен быть достаточен для проведения определения удельной электрической проводимости.
2. Соотношение объема пробы почвы к объему воды 1 : 5 выбрано для получения достаточного объема экстракта из всех видов почв, включая почвы с высоким содержанием органического вещества.
3. При проведении экстракции поддерживают температуру 20±1 °С, так как растворимость солей зависит от температуры.
4. После фильтрования измерения удельной электропроводности проводят при температуре до 25°С.
5. Энергия встряхивания на механическом встряхивателе должна быть достаточной для образования суспензии. Чрезмерная сила встряхивания может привести к сильному диспергированию частиц глины, ухудшению процесса фильтрации и отрицательному влиянию на результат определения.
В соответствии с инструкциями изготовителя прибора проводят проверку постоянной ячейки с применением стандартных растворов хлорида калия.
Для каждого раствора хлорида калия рассчитывают постоянную ячейки по уравнению:
![]() ,
,
где К - постоянная ячейки, м -1;
СS - удельная электрическая проводимость раствора хлорида калия, мСм/м;
Сm - измеренная электрическая проводимость того же раствора хлорида калия, мСм/л.
В качестве постоянной ячейки используют среднюю величину всех определений со стандартными растворами хлорида калия. Полученная величина не должна отличаться более чем на 5% от значения постоянной ячейки, указанной изготовителем прибора.
Затем измеряют электрическую проводимость фильтратов (Сm) при 25°С в соответствии с инструкциями изготовителя прибора и записывают полученный результат с точностью до одного десятичного знака.
Кондуктометрическое титрование. Большое распространение в аналитической практике получил метод кондуктометрического титрования. Как и в химическом титрометрическом анализе, здесь присутствуют все типы реакции: кислотно-основное и окислительно-восстановительное взаимодействие, реакции осаждения и комплексообразования. При титровании электропроводность АР изменяется. Причиной этого является связывание определяемых ионов в малодиссоциирующие молекулы, в труднорастворимые электролиты или в комплексные ионы. Например, при кислотно-основном титровании образуются молекулы воды. По мере добавления титранта уменьшается концентрация ионов Н+ (титрование кислоты щелочью) или концентрация ионов ОН- (титрование щелочи кислотой) и удельная электропроводность АР падает.
Но по достижении точки эквивалентности при дальнейшем приливании титранта удельная электропроводность возрастает, так как в АР вновь появляются свободные ионы ОН- (титрование щелочью) или Н+ (титрование кислотой) (рис. 65).
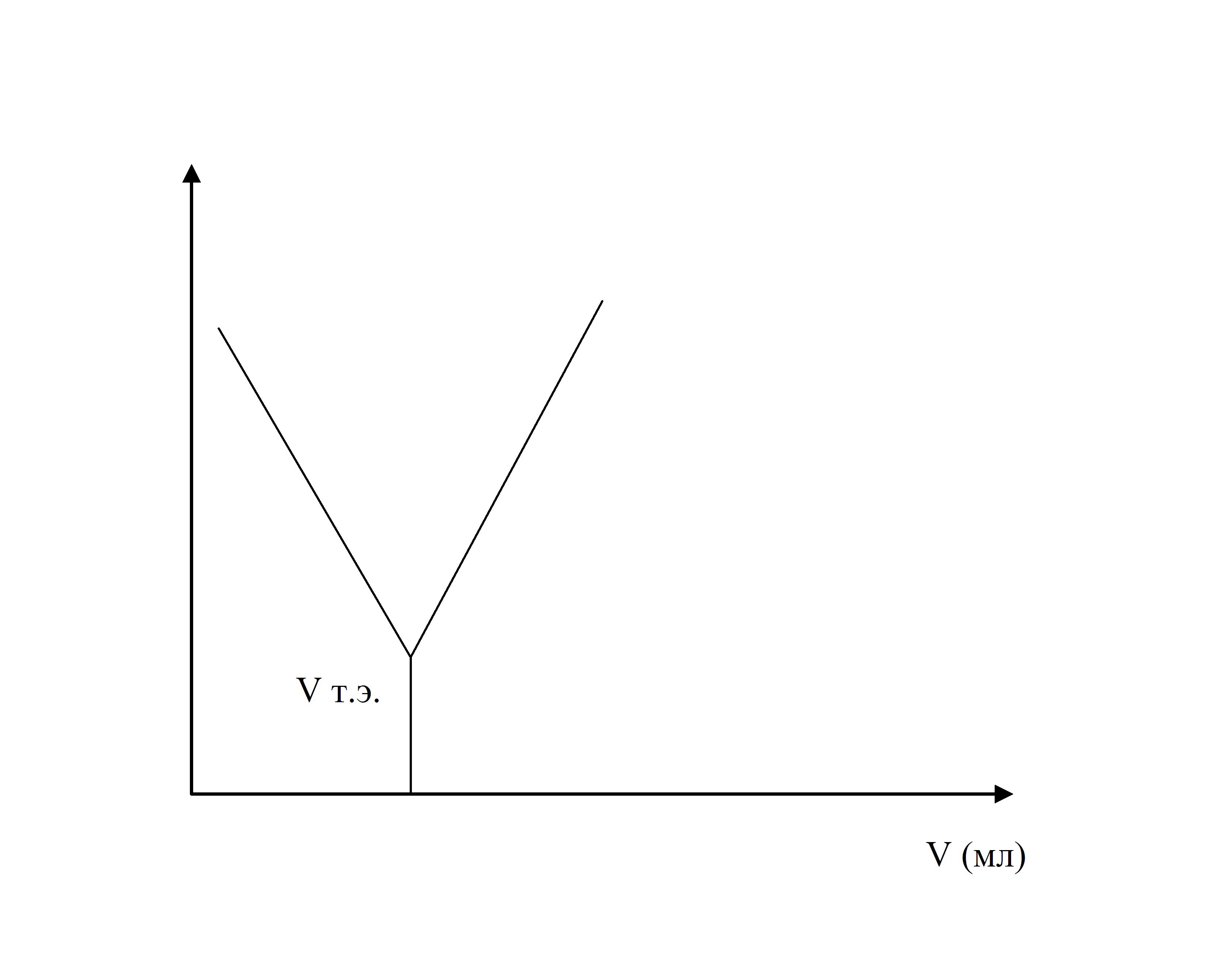
Рис. 65. Кривая титрования с изломом в точке эквивалентности
Если процесс нейтрализации изобразить графически, то получается кривая с изломом в точке эквивалентности, по которому находят объем титранта, пошедшего на титрование АР.
Кондуктометрическое титрование обладает рядом достоинств: возможность анализа смесей кислот и смесей оснований, титрование мутных и окрашенных растворов и др.
Нижний предел определяемых концентраций – 10-4 моль/л с погрешностью анализа 2%. При концентрациях выше 10-4 моль/л метод кондуктометрического титрования, как и прямая кондуктометрия, неизбирателен.
Техника кондуктомегрического титрования. За ходом реакции следят по электрической проводимости титруемой среды между двумя инертными (например, платиновыми) электродами, вычерчивают кривую зависимости электрической проводимости от объема прибавленного титранта.
При титровании определяемого вещества раствором реактива получаются малодиссоциирующие или малорастворимые соединения, вследствие чего электрическая проводимость титруемого раствора заметно понижается. При этом минимум электрической проводимости на кривой наблюдается в конце титрования и соответствует точке эквивалентности. Добавление же небольшого избытка реактива вызывает при титровании сильных электролитов новое увеличение электрической проводимости, которое и считают признаком конечной точки титрования.
Это позволяет определить точку эквивалентности по резкому увеличению электрической проводимости анализируемого раствора.
Например, в количественном анализе при работе по методу нейтрализации, при титровании гидроксида калия хлороводородной кислотой
К+ + ОН– + Н+ + Сl– →К+ + Сl– + Н2О
концентрация щелочи в растворе постепенно уменьшается.
Поскольку электрическая проводимость раствора хлорида калия гораздо ниже электрической проводимости раствора гидроксида калия и хлороводородной кислоты, то по мере нейтрализации будет наблюдаться уменьшение электрической проводимости. В точке эквивалентности титрования она будет наименьшей, а при добавлении избытка кислоты снова увеличится. Это и позволяет определить конечную точку титрования.