Экологический мониторинг и экологическая экспертиза

3.6. Фотометрическое определение железа в природных и сточных водах
Железо в воде присутствует в виде закисного (Fe+2) и окисного (Fe+3).
Содержание этих форм лимитируется величиной рН. Окисное железо менее устойчиво, более устойчиво железо в коллоидном состоянии. Оно характерно для поверхностных вод, тогда как закисное – для подземных вод.
ПДК железа в водных объектах рыбохозяйственного назначения составляет 0,1 мг/л, в водоемах хозяйстенно-питьевого и культурно-бытового назначения – 0,5 мг/л. Содержание железа в природных и сточных водах определяют фотометрически.
Метод основан на образовании окрашенных соединений железа с салициловой или сульфосалициловой кислотой и колориметрировании комплекса при λ = 425 нм.
Диапазон измерения концентраций железа без разбавления пробы 0,1-2,0 мг/л. Проведению анализа мешают медь при концентрации более 0,25 мг/л и алюминий более 2 мг/л. В слабокислом растворе при рН 2-4 в реакцию вступает одна молекула салициловой кислоты и образуется комплекс фиолетовой окраски:
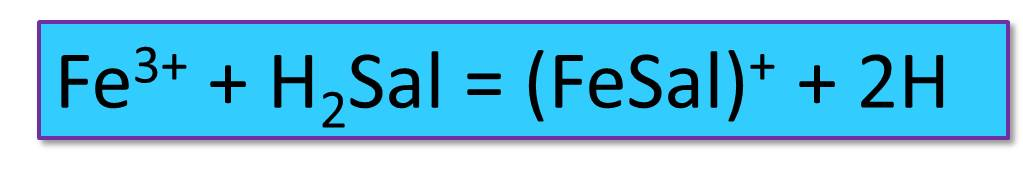 ,
,
где Sal – сокращенное обозначение остатка салициловой кислоты или сульфосалициловой кислоты.
В более кислой среде при рН<2 реакция смещается влево, и вследствие разрушения комплекса (FeSal)2 уменьшается интенсивность окраски раствора.
При уменьшении кислотности раствора (рН>4) в реакцию вступает вторая молекула салициловой кислоты, и раствор приобретает красную окраску за счет образования комплекса (FeSal2):
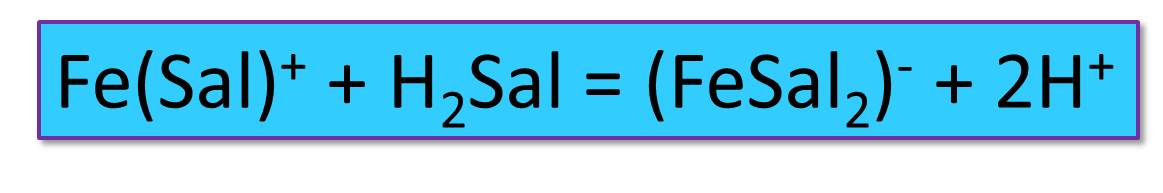
Комплекс (FeSal2)- устойчив при рН 4-8 и имеет более интенсивную окраску, поэтому удобен для колориметрирования.
В щелочной среде при рН 8-10 возникает третий комплекс желтого цвета:
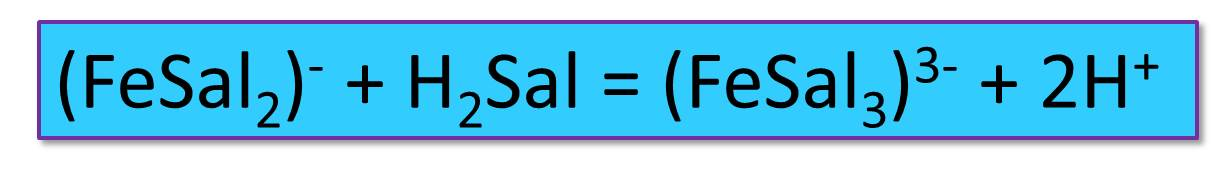
Подобные комплексы дает и сульфосалициловая кислота.
 – красного цвета при рН 1,8 – 2,5;
– красного цвета при рН 1,8 – 2,5;
 – бурого цвета при рН 4-8;
– бурого цвета при рН 4-8;
 – желтого цвета при рН 8-11,5.
– желтого цвета при рН 8-11,5.
Поскольку салициловая кислота имеет небольшую растворимость в воде (0,18 г в 100 мл воды), для колориметрирования удобнее применять хорошо растворимую сульфосалициловую кислоту.
Окраска исследуемого раствора при прибавлении реактива возникает не сразу, поэтому колориметрировать надо через 10 мин.

1. Хлорид аммония, 2 н. раствор (растворяют 107 г NH4Cl в мерной колбе вместимостью 1 л в небольшом количестве дистиллированной воды и доводят объем до метки дистиллированной водой).
2. Раствор сульфосалициловой кислоты 20%-й (или насыщенный раствор салициловой кислоты).
3. Аммиак, 10%-й или 25%-й раствор.
4. Стандартный раствор, содержащий 0,1 г железа в 1 л. Готовят его в мерной колбе, растворяя 0,7020 г соли Мора (FeSO4 + (NH4)2SO4 + 6H2O) в дистиллированной воде с добавлением 5 мл концентрированной серной кислоты.
В этом растворе в 1 мл содержится 0,1 мг железа. Из этого раствора готовят рабочий раствор разведением стандартного раствора в 20 раз. В 1мл свежеприготовленного рабочего раствора содержится 0,005 мг железа.

1. Фотоэлектроколориметр.
2. Кюветы с толщиной оптического слоя 2-5 см.

Отбирают 25 мл (или меньший объем, содержащий не более 0,1 мг железа) или берут пробу после минерализации, доводят 10%-м аммиаком рН до 6-8, контролируя по универсальной индикаторной бумаге, приливают 1мл 2 н. хлорида аммония, 1 мл 20% - й сульфосалициловой кислоты, 1 мл 10%-го аммиака.
После добавления каждого реактива перемешивают, доводят объем до метки дистиллированной водой, перемешивают и через 15 мин фотометрируют при фиолетовом светофильтре (λ = 425 нм ) в кюветах с толщиной оптического слоя 2-5 см по отношению к дистиллированной воде, обработанной как проба.
Содержание железа (мкг) находят по калибровочному графику или визуально по интенсивности окраски пробы и шкалы стандартных растворов.
Калибровочный график.
Для получения калибровочного графика в колбы на 50 мл вносят 0 – 1 – 3 – 5 – 10 мл рабочего стандартного раствора, что соответствует содержанию железа 0 – 5 – 15 – 25 – 50 мкг.
Доводят объем до 25-30 мл дистиллированной водой и проводят анализ как исследуемой воды.
Калибровочный график строят в координатах "оптическая плотность – содержание железа (мкг)".
Концентрацию железа (мг/л) рассчитывают по формуле
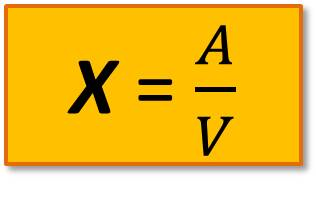 ,
,
где А – содержание железа, найденное по калибровочному графику или визуально по шкале стандартных растворов, мкг;
V – объем пробы, взятой для анализа, мл.
