ФИЗИКА
Задача 2. В сосуде объёмом 2 м3 находится смесь 4 кг гелия и 2 кг водорода при температуре 27°С. Определить давление и молярную массу газа.
Дано: V = 2 м3; т1 = 4 кг; М1 = 4 ⋅ 10-3 кг/моль; т2 = 2 кг; М2 = 2 ⋅ 10-3 кг/моль; Т = 300 К
Найти: p, M.

Запишем уравнения Клайперона-Менделеева для гелия и водорода:
(2.2.1)
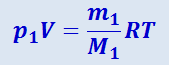 ,
,
(2.2.2)
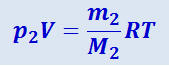 ,
,
где р1 - парциальное давление гелия;
т1 - масса гелия;
М1 - молярная масса гелия;
V – объём сосуда;
Т – температура газа;
R = 8,31 Дж/моль⋅К - молярная газовая постоянная;
р2 - парциальное давление воздуха;
т2 - масса водорода;
М2 - молярная масса водорода.
По закону Дальтона
(2.2.3)
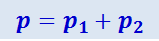 .
.
Из (2.2.1) и (2.2.2) выразим р1 и р2, и подставим в (2.2.3):
(2.2.4)
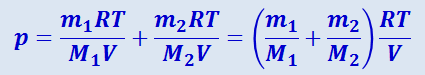 .
.
Определим молярную массу смеси газов по формуле
(2.2.5)
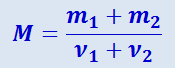 ,
,
где ν1 и ν2 - число молей гелия и водорода соответственно
(2.2.6)
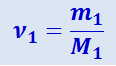 ,
,
(2.2.7)
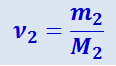 .
.
Подставив (2.2.6) и (2.2.7) в (2.2.5), найдём
(2.2.8)
 .
.
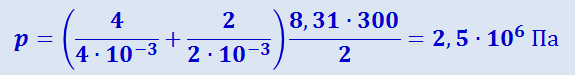 ,
,
 .
.
к к к
