ФИЗИКА
2.3.7. Второе начало термодинамики.
Замечания о первом и втором началах термодинамики.
Формулировки, выражающие второе начало термодинамики
Первое начало термодинамики не даёт никаких указаний относительно направления, в котором могут происходить процессы в природе. Для изолированной системы, например, первое начало требует только, чтобы во всех процессах энергия системы оставалась постоянной. Если 1 и 2 – два состояния такой системы, то первое начало ничего не может сказать, будет ли система переходить из состояния 1 в состояние 2, или из состояния 2 в состояние 1. Вообще, на основании первого начала нельзя выяснить, будут ли в изолированной системе происходить какие-либо процессы.
Второе начало термодинамики наоборот, позволяет судить о направлении процессов, которые могут происходить в действительности. Но этим значение второго начала не исчерпывается. Второе начало позволяет вполне удовлетворительно решить вопрос о количественной мере температуры и построить рациональную температурную шкалу, не зависимую от произвола выбора термометрического тела и устройства термометра.
Чтобы прийти к формулировке постулата второго начала термодинамики, рассмотрим схематически работу тепловой машины. В цилиндре машины (рис. 2.3.10) помещается газ или какое-либо вещество, называемое рабочим телом. Для определённости будем считать, что рабочим телом является газ.
Рис. 2.3.10 |
Пусть на диаграмме pV начальное состояние рабочего тела изображается точкой 1. Приведём дно цилиндра в тепловой контакт с нагревателем, т.е. телом, температура которого выше температуры газа в цилиндре. Газ будет нагреваться и расширяться – этот процесс изображён кривой 1 а 2. Рабочее вещество получит от нагревателя тепло Q1 и совершит положительную работу A1. По первому началу,
(2.3.31)
 .
.
Теперь надо вернуть поршень в исходное положение, т.е. сжать газ. Это надо сделать так, чтобы работа A2, затраченная на сжатие, была меньше A1. С этой целью приведём дно цилиндра в тепловой контакт с холодильником, т.е. телом, температура которого ниже температуры газа в цилиндре, и сожмём газ по пути 2 б 1. В результате газ вернётся в исходное состояние 1. При этом он отдаст холодильнику тепло Q2. По первому началу,
(2.3.32)
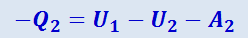 .
.
Сложим (2.3.31) и (2.3.32):
(2.3.33)
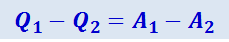 .
.
Таким образом, тепловая машина совершила круговой процесс, в результате которого нагреватель отдал тепло Q1, холодильник получил тепло Q2, тепло Q = Q1 - Q2 пошло на производство работы A1 - A2. Отношение
(2.3.34)
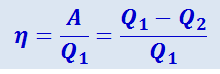
называется коэффициентом полезного действия тепловой машины.
Возникает вопрос, нельзя ли построить периодически действующую тепловую машину без холодильника, т.е. добиться того, чтобы Q2 = 0, и следовательно, η = 1? Такая машина могла бы превращать в работу всю теплоту, заимствованную от одного теплового резервуара. Возможность её построения не противоречит закону сохранения энергии. По своему практическому значению она почти не уступала бы перпетуум-мобиле, так как с её помощью можно было бы производить работу за счёт практически неисчерпаемых запасов внутренней энергии, содержащихся в воде океанов и морей, воздушной атмосфере и недрах Земли. Такую машину Оствальд назвал перпетуум-мобиле второго рода.
Опытные факты говорят против возможности построения перпетуум-мобиле второго рода. Поэтому невозможность построения такого вечного двигателя была возведена в постулат. Он называется постулатом второго начала термодинамики и является обобщением опытных фактов. Доказательством этого постулата является согласие всех вытекающих из него следствий с опытом. До сих пор, применяя этот постулат к макроскопическим системам, размеры которых не очень малы, физика нигде не натолкнулась на противоречия. Приведём две точных формулировки постулата.
Согласно Томсону (лорд Кельвин), невозможен круговой процесс, единственным результатом которого было бы производство работы за счёт уменьшения внутренней энергии теплового резервуара.
Напомним, что под тепловым резервуаром понимают тело или систему тел, находящуюся в состоянии термодинамического равновесия и обладающую запасом внутренней энергии.
Клаузиус дал существенно иную формулировку основного постулата: «Теплота не может самопроизвольно переходить от тела, менее нагретого к телу более нагретому».
Содержание этого постулата состоит в том, что невозможно каким бы то ни было способом забрать тепло от тела менее нагретого, целиком передать его телу, более нагретому и притом так, чтобы в природе больше не произошло никаких изменений. Любой воображаемый процесс, в котором осуществляется такая передача тепла, называется процессом Клаузиуса. Таким образом, постулат утверждает, что процесс Клаузиуса невозможен.
Но постулат Клаузиуса не утверждает, что передача тепла от тела менее нагретого к телу более нагретому вообще невозможна. Она невозможна при условии, что во всех остальных телах никаких изменений не должно произойти. В этом смысл слова «самопроизвольно», употреблённого при формулировке второго начала термодинамики. Если же допустить другие процессы, то передача тепла от тела менее нагретого к телу более нагретому становится возможной.
Такие процессы называются компенсирующими или, короче, компенсациями. Так, в холодильных машинах тепло, заимствованное от менее нагретого тела, передаётся более нагретому телу. Это не противоречит постулату Клаузиуса, так как такой переход происходит здесь не самопроизвольно, а сопровождается работой электрического мотора. Электрический холодильник перестаёт действовать, если выключить питающий его ток. Простейшая тепловая машина, о которой говорилось в начале (рис. 2.3.10), может работать как холодильная машина. Для этого расширение рабочего вещества следует производить по кривой 1 б 2, а сжатие – по кривой 2 а 1, лежащей выше. Совершая расширение 1 б 2, машина будет заимствовать от холодильника тепло Q2; при сжатии по кривой 2 а 1 она передаст нагревателю тепло Q1 > Q2. При этом над машиной будет произведена положительная работа A' = Q1 - Q2. Производство этой работы и является здесь компенсирующим процессом.
Нетрудно показать, что постулаты Клаузиуса и Томсона эквивалентны.
к к к