ФИЗИКА
2.2.6. Барометрическая формула. Распределение Больцмана
Известно, что атмосферное давление убывает с высотой. Найдём функцию p(h), описывающую зависимость давления от высоты.
Выделим мысленно в атмосфере вертикальный столб с площадью поперечного сечения S, равной единице (рис. 2.2.9).
Рис. 2.2.9 |
Атмосферное давление на высоте h обусловлено весом столба воздуха, простирающегося от сечения, расположенного на данной высоте, до внешней границы атмосферы. Поэтому убыль давления -dp при переходе от высоты h к высоте h + dh равна весу воздуха, заключённого в элементе столба высоты dh:
(2.2.31)
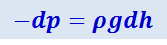 ,
,
где ρ - плотность воздуха на высоте h.
При условиях, близких к нормальным (т.е. при давлениях порядка атмосферного и температурах, близких к 0°С), воздух довольно хорошо подчиняется уравнению состояния идеального газа (2.2.18). Из (2.18) следует:
(2.2.32)
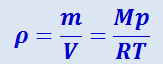 .
.
Подставим (2.2.32) в (2.2.31). Тогда получим:
(2.2.33)
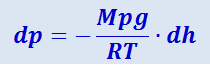 .
.
Здесь под М подразумевается молярная масса воздуха. Разделив в (2.2.33) переменные, придём дифференциальному уравнению
(2.2.34)
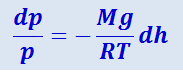 .
.
Полагая T = const, получим:
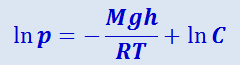 .
.
Потенцируя это выражение, придём к формуле
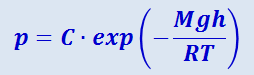 .
.
Положив h = 0, получим, что C = p0, где p0 - атмосферное давление на высоте, принятой за начало отсчёта.
Таким образом, для изотермической атмосферы зависимость давления от высоты описывается формулой
(2.2.35)
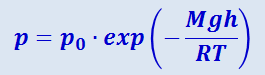 ,
,
которая называется барометрической формулой.
На самом деле температура атмосферы заметно изменяется с высотой, достигая на высоте 10 км значений, на несколько десятков кельвинов меньших, чем на поверхности Земли. Однако относительное (по сравнению с температурой, равной примерно 300 K) изменение температуры с высотой не очень велико, вследствие чего формула (2.2.35) позволяет определять довольно точно высоту, измеряя давление. Предназначенный для этой цели, проградуированный в значениях высоты барометр называется альтиметром. Такие высотомеры устанавливаются, в частности, на самолётах.
Заменим в формуле (2.2.35) отношение  равным ему отношением
равным ему отношением 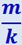 (т – масса молекулы, k – постоянная Больцмана). Кроме того, представим р в виде nkT. Тогда получим:
(т – масса молекулы, k – постоянная Больцмана). Кроме того, представим р в виде nkT. Тогда получим:
(2.2.36)
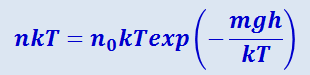 .
.
Формула (2.2.35) получена для изотермической атмосферы. Поэтому значение Т в обеих частях равенства (2.2.36) одно и то же. С учётом этого
(2.2.37)
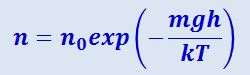 .
.
Здесь n0 - концентрация молекул при h = 0, n - концентрация молекул на высоте h.
Формула (2.2.37) описывает распределение молекул по высоте в изотермической атмосфере. Из неё следует, что с понижением температуры концентрация молекул на высотах, отличных от нуля, убывает, обращаясь в нуль при T = 0. Это означает, что при абсолютном нуле все молекулы расположились бы на поверхности Земли. С повышением температуры зависимость n от h cтановится всё более слабой, так что молекулы оказываются распределёнными по высоте почти равномерно. Такое поведение функции при изменении температуры объясняется тем, что она отражает «противоборство» двух тенденций:
- притяжение молекул к Земле (характеризуемое силой mg) стремится расположить их на поверхности Земли;
- тепловое движение (характеризуемое энергией kT) стремится разбросать молекулы равномерно по всем высотам.
При каждом значении Т обе тенденции уравновешивают друг друга.
Выражение mgh представляет собой потенциальную энергию молекулы εp. Поэтому формулу (2.2.37) можно написать следующим образом:
(2.2.38)
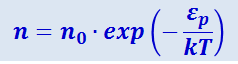 .
.
Здесь n0 - концентрация молекул в том месте, для которого εp принята равной нулю, n - концентрация молекул в том месте, где потенциальная энергия молекулы равна εp.
Больцман доказал, что формула (2.2.38) справедлива в случае потенциального силового поля любой природы для совокупности любых одинаковых частиц, находящихся в состоянии хаотического теплового движения. В связи с этим функцию (2.2.38) называют распределением Больцмана.
Между распределениями Больцмана и Максвелла имеется большое сходство: и в том и в другом случае основным множителем является экспонента, под знаком которой стоит отношение энергии молекулы (в одном случае потенциальной, в другом кинетической) к величине kT, определяющей среднюю энергию теплового движения молекул.
Возьмём элементарный объём dV = dxdydz, расположенный в точке с координатами x, y, z. Согласно (2.38), в пределах этого объёма находится число молекул
(2.2.39)
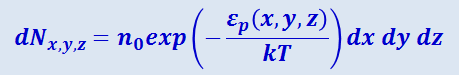 .
.
Эта формула обнаруживает ещё большее сходство с распределением Максвелла, которое можно представить в виде
(2.2.40)
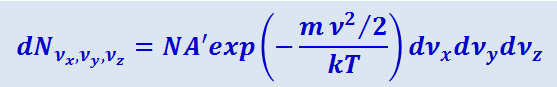 .
.
Распределения (2.2.39) и (2.2.40) можно объединить в один закон Максвелла-Больцмана, согласно которому число молекул, компоненты скоростей которых лежат в пределах от νx, νy, νz до νx + dνx, νy + dνy, νz + dνz , а координаты – в пределах от x, y, z до x + dx, y + dy, z + dz, равно
(2.2.41)
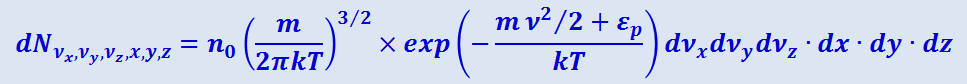 .
.
к к к