Глава 13
Дыхательная система включает два отдела: воздухоносные пути и респираторный отдел. В состав органов дыхания также входят дыхательные мышцы, плевральные полости, собственный нервный аппарат, эндокринные клетки, иммунокомпетентные клетки, чувствительные и двигательные нервные окончания, образованные отростками нейронов собственного нервного аппарата и нейронов симпатического и парасимпатического отделов. Дыхательная система имеет мощную иммунологическую защиту.
Регуляция развития
Как начальные, так и поздние стадии развития органов дыхания регулируют гены семейства Hox. В развитии и морфогенезе органов дыхания участвуют различные транскрипционные факторы и факторы роста: Notch, TGFb, BMP, Shh, Wnt, FGF, EGF.
Развитие трахеи и бронхов находится под индукционным влиянием окружающей спланхнической мезодермы. Мезодерму можно разделить на две части: окружающая трахею — индуцирует рост трахеи в длину, но подавляет ветвление; окружающая бронхи — стимулирует ветвление бронхов. Мезенхима не только предопределяет ветвление бронхов, но и контролирует дифференцировку альвеолярного эпителия.
В регулирующем влиянии мезенхимы на ветвление бронхов участвуют компоненты сигнальной системы FGF. На самых ранних стадиях формирования бронхиальных почек, особенно в дистальной мезенхиме, окружающей верхушки энтодермальных почек, экспрессируется FGF10, регулирующий формирование почек и направленную миграцию клеток. Компоненты сигнальной системы EGF участвуют в более поздних этапах развития лёгких, а именно в образовании альвеол. EGF регулирует дифференцировку пневмоцитов типа II. BMP4 экспрессируется в вентральной мезенхиме передней кишки и первичных бронхиальных почек. По мере развития экспрессия BMP4 становится максимальной у верхушек дистальных почек. BMP4 участвует в ветвлении бронхов, регулирует дифференцировку эпителия, противодействуя, в то же время, стимулирующему влиянию FGF10 на пролиферацию эпителия.
Shh экспрессируется всей энтодермой развивающихся лёгких, максимально — на верхушках дистальных почек. Рецепторы Shh (Patched) экспрессируются главным образом в клетках дистальной мезенхимы. Shh имеет важное значение во взаимодействии энтодермы с мезенхимой, регулирует пролиферативный потенциал мезенхимы, влияет на экспрессию мезенхимных генов.
Пренатальное развитие
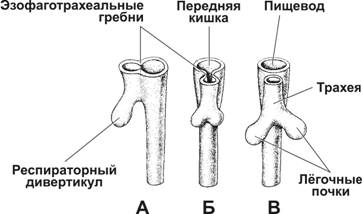
Развитие дыхательной системы начинается на 4-й неделе. На 26-й день в каудальной части первичной глотки (позади 4-й пары глоточных карманов) по срединной линии дна глотки появляется гортанно-трахейная (ларинготрахеальная) борозда. Борозда тянется каудально по срединной линии вентральной части передней кишки и быстро углубляется. Затем дорсальные края борозды — пищеводно-трахейные (эзофаготрахеальные) гребни — смыкаются с образованием пищеводно-трахейной (эзофаготрахеальной) перегородки. Перегородка разделяет зачаток пищевода (первоначально — короткий суженный участок передней кишки) и зачаток трахеи. Смыкание краёв гортанно-трахейной борозды происходит на всём её протяжении, за исключением краниального (гортанного) конца, где сохраняется (в виде отверстия) связь зачатка трахеи с первичным пищеводом. Отверстие, которое остаётся между гортанным концом зачатка трахеи и первичным пищеводом, — голосовая щель.
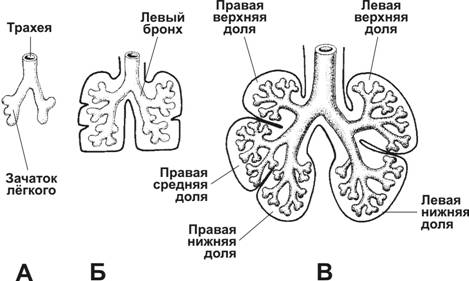
Одновременно с углублением гортанно-трахейной борозды на наружной поверхности первичной глотки образуется выпячивание, а стенки борозды утолщаются. Таким образом вентральнее первичной глотки формируется трубчатый вырост — гортанно-трахейный (респираторный) дивертикул (рис. 13-1). На каудальном конце удлиняющегося дивертикула формируется мешковидное выпячивание — лёгочная почка, которая затем подразделяется на две бронхиальные почки, растущие латерально в перикардиоперитонеальный канал (зачаток плевральной полости). Во время роста бронхиальных почек окружающая их спланхническая мезодерма сдвигается вентрально и из неё начинает формироваться плевра. Бронхиальные почки дифференцируются на левый и правый первичные бронхи (рис. 13-2). При этом правый бронх несколько больше левого и ориентирован более вертикально. Это соотношение сохраняется и на всех последующих стадиях развития, поэтому чужеродные тела легче попадают в правый бронх. Первичные бронхи подразделяются на вторичные. Справа верхний вторичный бронх даёт начало верхней доле лёгкого, тогда как нижний вторичный бронх подразделяется на два бронха, один для средней доли, а другой для нижней доли лёгкого. Слева два вторичных бронха вступают в верхнюю и нижнюю доли лёгкого. Далее формируется бронхиальное дерево лёгких; к концу 6-го месяца плодного периода насчитывают 17 ветвлений. Позднее происходит ещё 6 дополнительных ветвлений, процесс ветвления заканчивается после рождения.
Эмбриональные источники
Энтодерма, выстилающая гортанно-трахейную борозду, даёт начало эпителию и железам гортани, трахеи, бронхов и лёгочной эпителиальной выстилке. Соединительная ткань, хрящи, ГМК развиваются из спланхнической мезодермы, окружающей первичную кишку.
Клеточные компартменты
В лёгком клетки многочисленных герминативных линий взаимодействуют между собой как в ходе морфогенеза, так и для поддержания структур сформированного лёгкого. В рамках одного зародышевого листка клетки обособляются в отдельные клеточные компартменты. Так, энтодерма формирует по крайней мере 4 отдельных эпителиальных региона, каждый — со своим специфическим клеточным составом. Первый компартмент содержит многорядный мерцательный эпителий и подслизистые железы трахеи и крупных бронхов, второй компартмент — многорядный мерцательный эпителий меньших бронхов, третий — цилиндрический эпителий и бронхиолярные экзокриноциты бронхиол, четвёртый — альвеолярный эпителий. Всё это затрудняет выделение стволовой клетки эпителия лёгких. Считают, что в качестве стволовых клеток выступают базальные клетки и бронхиолярные экзокриноциты эпителия воздухоносных путей и пневмоциты типа II.
Развитие гортани
Каудальнее голосовой щели гортанно-трахейная трубка несколько расширена. Этот расширенный участок — будущая гортань. Отверстие гортанно-трахейной трубки в глотку становится входом в гортань (aditus laryngis). На краниальном конце гортанно-трахейной трубки мезенхима образует два черпаловидных бугорка. Из гипобранхиального возвышения (eminentia hypobranchialis) образуется надгортанное утолщение в результате пролиферации мезенхимы вентральных частей 3-й и 4-й глоточных дуг. Затем из этого утолщения формируется надгортанник. Эпителий гортани быстро пролиферирует и временно закрывает просвет гортани. Эпителий, выстилающий гортань, происходит из энтодермы краниального конца гортанно-трахейного дивертикула. Хрящи гортани происходят из хрящей 4-й и 6-й пар глоточных дуг.
Рис. 13-1. Начальные стадии развития органов дыхания. В конце 3-й–начале 4-й недели в стенке передней кишки образуется выпячивание (респираторный дивертикул). По обе стороны от выпячивания формируются вдающиеся в просвет первичной кишки продольные валики — эзофаготрахеальные гребни, которые затем сближаются и смыкаются. Так образуется перегородка, отделяющая первичную кишку (будущий пищевод) от респираторного дивертикула. Последний даёт начало трахее, заканчивающейся на каудальном конце двумя мешковидными образованиями — лёгочными почками. А — в конце 3‑й недели, Б и В — на 4‑й неделе. [17]
Рис. 13-2. Развитие бронхов и лёгких. На 5‑й неделе начинается закладка бронхов. Левая лёгочная почка образует два, правая — три выпячивания. Из выпячиваний развиваются главные бронхи. В дальнейшем происходит ветвление главных бронхов с формированием бронхиального дерева. А — 5 недель, Б — 6 недель, В — 8 недель. [17]
Стадии развития лёгких
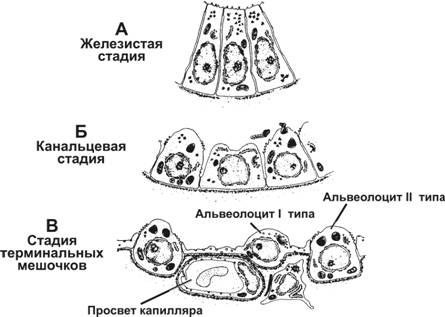
Дифференцировка лёгких проходит следующие стадии: железистую, канальцевую и альвеолярную (рис. 13-3).
Железистая стадия
Железистая стадия (5–15 недель) характеризуется дальнейшим ветвлением воздухоносных путей (лёгкие приобретают вид железы), развитием хрящей трахеи и бронхов, появлением бронхиальных артерий. Эпителий, выстилающий респираторный зачаток, состоит из цилиндрических клеток. На 10-й неделе среди клеток цилиндрического эпителия воздухоносных путей появляются бокаловидные клетки. К 15-й неделе формируются первые капилляры будущего респираторного отдела.
Рис. 13-3. Развитие лёгких. По мере формирования бронхиального дерева лёгкие приобретают сходство с разветвлённой железой (железистая стадия развития). К концу 4‑го месяца однослойный эпителий, выстилающий бронхи и бронхиолы, остаётся недифференцированным и имеет цилиндрическую форму. В дальнейшем ветвление продолжается, и к концу 6‑го месяца бронхи и бронхиолы формируют канальцы (канальцевая стадия). Эпителий, выстилающий канальцы, становится кубическим. В течение 7‑го месяца канальцы приобретают вид мешочков — первичных альвеол (стадия терминальных мешочков). При этом происходит дифференцировка эпителиальных клеток, и к концу 7‑го месяца большинство из них уплощается (пневмоциты типа I). Небольшое количество эпителиальных клеток сохраняет кубическую форму (пневмоциты типа II). А — с 4‑й недели по 4‑й месяц; Б — с 4‑го по 6‑й месяц; В — с начала 7‑го месяца до рождения. [17]
Канальцевая стадия
Канальцевая стадия (16–25 недель) характеризуется появлением выстланных кубическим эпителием респираторных и терминальных бронхиол, а также канальцев (прообразов альвеолярных мешочков) и подрастанием к ним капилляров.
стадия терминальных мешочков
Альвеолярная, или стадия терминальных мешочков (26–40 недель), характеризуется массовым преобразованием канальцев в мешочки (первичные альвеолы), увеличением числа альвеолярных мешочков, дифференцировкой пневмоцитов типов I и II и появлением сурфактанта. К концу 7-го месяца значительная часть клеток кубического эпителия респираторных бронхиол дифференцируется в плоские клетки (пневмоциты типа I), тесно связанные с кровеносными и лимфатическими капиллярами, и становится возможным газообмен. Остальные клетки сохраняют кубическую форму (пневмоциты типа II) и начинают вырабатывать сурфактант. Синтез и секреция сурфактанта пневмоцитами типа II — важное событие внутриутробного развития лёгких. Функции сурфактанта — снижение сил поверхностного натяжения альвеол и повышение эластичности лёгочной ткани. Сурфактант предотвращает спадение альвеол в конце выдоха и позволяет раскрываться альвеолам при пониженном внутригрудном давлении. Из фосфолипидов, входящих в состав сурфактанта, крайне важен лецитин. Отношение содержания лецитина к содержанию сфингомиелина в амниотической жидкости косвенно характеризует количество внутриальвеолярного сурфактанта и степень зрелости лёгких. Показатель 2:1 или выше — признак функциональной зрелости лёгких.
В течение последних двух месяцев пренатальной и нескольких лет постнатальной жизни число терминальных мешочков постоянно увеличивается. Зрелые альвеолы до рождения отсутствуют.
Лёгочная жидкость
К рождению лёгкие заполнены жидкостью, в большом количестве содержащей хлориды, белок, некоторое количество слизи, поступающей из бронхиальных желёз, и сурфактант. После рождения лёгочная жидкость быстро резорбируется кровеносными и лимфатическими капиллярами, а небольшое её количество удаляется через бронхи и трахею. Сурфактант остаётся в виде тонкой плёнки на поверхности альвеолярного эпителия.
Болезнь гиалиновых мембран (респираторный дистресс-синдром новорождённых) — дыхательное расстройство, поражающее в первую очередь недоношенных детей, родившихся до полного биохимического созревания лёгких. Вследствие недостатка сурфактанта лёгкие плохо расправляются, что приводит к развитию дыхательной недостаточности.
Постнатальная дифференцировка
Рост лёгких после рождения происходит в основном за счёт нарастания числа респираторных бронхиол и образования новых первичных альвеол, а не за счёт увеличения их размера. К рождению лёгкие содержат около 60 млн. первичных альвеол, их количество интенсивно увеличивается в первые два года жизни. Затем скорость роста замедляется, и к 8–12 годам количество альвеол достигает приблизительно 375 млн., что соответствует количеству альвеол у взрослых.
Пороки развития
Трахеопищеводный свищ возникает в результате неполного расщепления первичной кишки на пищевод и трахею.
Врождённая долевая эмфизема — увеличение объёма доли, реже сегмента лёгкого вследствие повышения давления в респираторном отделе. Возникновение данной патологии связывают с недоразвитием хрящей субсегментарных бронхов или с недостаточностью эластических волокон альвеол.
Гипоплазия лёгких — патология развития, когда долевые бронхи оканчиваются морфологически недоразвитой (вследствие редукции ветвления бронхов, уменьшения размеров и количества ацинусов) и, следовательно, функционально несовершенной лёгочной тканью. Гипоплазия лёгких — наиболее часто встречающееся врождённое нарушение; в подавляющем большинстве случаев проявляется в связи с другими врождёнными аномалиями. К гипоплазии лёгких приводят два главных фактора: компрессия (сдавление) лёгкого, вызванная различными причинами, и олигогидрамнион (уменьшенный объём амниотической жидкости).
Лёгочная секвестрация — образование дополнительной доли или кистообразных скоплений нефункционирующей лёгочной ткани, не сообщающихся с бронхиальным деревом. Секвестры могут располагаться внутри долей (интралобарный секвестр), внутри грудной клетки вне лёгких (экстралобарный секвестр).
Принципы организации дыхательной системы
Просвет воздухоносных путей и альвеол лёгкого — внешняя среда
Везде — в воздухоносных путях и на поверхности альвеол — расположен пласт эпителия. Эпителий воздухоносных путей осуществляет защитную функцию, которая выполняется, с одной стороны, самим фактом присутствия пласта эпителия; с другой стороны, за счёт секреции защитного материала — слизи. Её продуцируют присутствующие в составе эпителия бокаловидные клетки. Кроме того, под эпителием находятся железы, также секретирующие слизь; выводные протоки этих желёз открываются на поверхность эпителия.
Воздухоносные пути функционируют как установка для кондиционирования воздуха
Характеристики внешнего воздуха (температура, влажность, загрязнённость частицами разного сорта, наличие микроорганизмов) варьируют весьма значительно. Но в респираторный отдел должен поступать воздух, отвечающий определённым требованиям. Функцию доведения воздуха до необходимых кондиций и выполняют воздухоносные пути.
Очистка воздуха. Посторонние частицы осаждаются в находящейся на поверхности эпителия слизистой плёнке. Далее загрязнённая слизь удаляется из воздухоносных путей при её постоянном перемещении по направлению к выходу из дыхательной системы с последующим откашливанием. Такое постоянное движение слизистой плёнки обеспечивается за счёт направленных к выходу из воздухоносных путей синхронных и волнообразных колебаний ресничек, находящихся на поверхности эпителиальных клеток. Кроме того, перемещением слизи к выходу предупреждается её попадание на поверхность альвеолярных клеток, через которые происходит диффузия газов.
Поддержание температуры и влажности. Кондиционирование температуры и влажности вдыхаемого воздуха осуществляется при помощи крови, находящейся в сосудистом русле стенки воздухоносных путей. Этот процесс происходит главным образом в начальных отделах, а именно в носовых ходах.
Слизистая оболочка воздухоносных путей участвует в защитных реакциях
В составе эпителия слизистой оболочки присутствуют внутриэпителиальные дендроциты, тогда как собственный слой содержит значительное количество различных иммунокомпетентных клеток (T- и B–лимфоциты; плазматические клетки, синтезирующие и секретирующие IgG, IgA, IgE; макрофаги, дендритные клетки).
Тучные клетки весьма многочисленны в собственном слое слизистой оболочки воздухоносных путей. Гистамин тучных клеток вызывает бронхоспазм, вазодилатацию, гиперсекрецию слизи из желёз и отёк слизистой оболочки (как результат вазодилатации и увеличения проницаемости стенки посткапиллярных венул). Кроме гистамина, тучные клетки, наряду с эозинофилами и другими клетками воспаления, выделяют ряд медиаторов; действие которых приводит к воспалению и отёку слизистой оболочки, повреждению эпителия, сокращению ГМК и сужению просвета воздухоносных путей. Все вышеперечисленные эффекты характерны для бронхиальной астмы.
Воздухоносные пути не спадаются
Более того, их просвет постоянно изменяется и регулируется в связи с реальной ситуацией. Спадение просвета воздухоносных путей предотвращает присутствие в их стенке структур, образованных в начальных отделах костной, а далее — хрящевой тканью. Изменение величины просвета воздухоносных путей обеспечивают складки слизистой оболочки, активность ГМК и эластические структуры стенки.
Регуляция тонуса ГМК. Тонус ГМК воздухоносных путей регулируют нейромедиаторы, гормоны, метаболиты арахидоновой кислоты. Эффекты зависят от присутствия соответствующих рецепторов в ГМК. ГМК стенки воздухоносных путей имеют м-холинорецепторы, рецепторы гистамина, a- и b-адренорецепторы и др. Нейромедиаторы секретируются из терминалей нервных окончаний (для блуждающего нерва — ацетилхолин; для нейронов симпатического ствола — норадреналин).
· ГМК бронхов. Бронхоконстрикцию вызывают ацетилхолин, вещество P, нейрокинин A, гистамин, простагландин PGD2, тромбоксан TXA2, лейкотриены LTC4, LTD4, LTE4. Бронходилатацию вызывают VIP, адреналин, брадикинин, простагландин PGE2.
· ГМК сосудов. Сокращение ГМК сосудов (вазоконстрикцию) вызывают: адреналин, лейкотриены LTC4, LTD4, LTE4, ангиотензин II. Расслабляющий эффект на ГМК сосудов бронхов (вазодилатация) оказывают гистамин, брадикинин, VIP, простагландин PGD2, тромбоксан TXA2.
Поступающий в дыхательные пути воздух подвергается химической экспертизе
Её осуществляют обонятельный эпителий и хеморецепторы в стенке воздухоносных путей. К таким хеморецепторам относятся чувствительные нервные окончания и специализированные хемочувствительные клетки в составе эпителия слизистой оболочки.
Воздухоносные пути — носовые ходы с обонятельным эпителием, носоглотка, гортань, трахея, бронхи разных калибров, бронхиолы. Функция воздухоносных путей — проведение воздуха к респираторному отделу; они же выполняют функцию голосообразования и обоняния. Стенка воздухоносных путей в типичном случае состоит из четырёх оболочек: слизистой, подслизистой, фиброзно-хрящевой и адвентициальной. В стенке воздухоносных путей также присутствуют кровеносные и лимфатические сосуды, нейроны собственного нервного аппарата, чувствительные нервные окончания, нервные окончания вегетативной нервной системы.
Слизистая оболочка
Слизистую оболочку образуют однослойный многорядный мерцательный эпителий, собственный слой и мышечный слой. Мышечный слой отсутствует в верхних отделах, но появляется в нижних. Собственный слой представлен рыхлой соединительной тканью со значительным количеством ретикулиновых и эластических волокон. Здесь присутствуют тучные клетки, фибробласты, макрофаги, дендритные клетки, T- и B–лимфоциты, плазматические клетки. Эпителий содержит реснитчатые, бокаловидные, базальные, нейроэндокринные, щёточные (каёмчатые), хеморецепторные клетки, бронхиолярные экзокриноциты (в терминальном отделе воздухоносных путей), внутриэпителиальные дендроциты (рис. 13-6).
Реснитчатые клетки
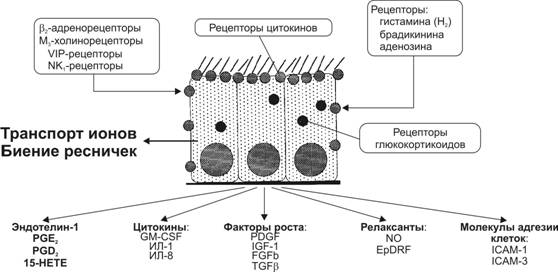
Основную массу эпителия воздухоносных путей составляют реснитчатые клетки, содержат до 250 ресничек на апикальной поверхности. Эти клетки имеют рецепторы для многих веществ (табл. 13–1, рис. 13-4). В зависимости от вида активированных рецепторов реакция реснитчатых клеток может быть различной.
Функции реснитчатых клеток
1. Транспорт ионов и продвижение слизи. Ряд агентов стимулирует активный ионный транспорт через эпителиальные клетки, а именно секрецию ионов Cl– и абсорбцию ионов Na+, соответственно увеличивая или уменьшая транспорт воды через эпителий, а также может изменять частоту биения ресничек эпителиальных клеток, что влияет на эффективность продвижения слизи, т.е. на уровень очистки вдыхаемого воздуха (табл. 13-1).
Таблица 13-1. Рецепторы эпителиальных клеток воздухоносных путей
|
Вид рецептора |
Эффект активации |
|
b2‑Адренергический |
Увеличение ионного транспорта, частоты биения ресничек |
|
м3‑Холинергический |
Увеличение ионного транспорта, частоты биения ресничек |
|
VIP |
Увеличение ионного транспорта, частоты биения ресничек |
|
NK1 (тахикининов) |
Увеличение ионного транспорта, частоты биения ресничек, увеличение экспрессии молекул адгезии клеток |
|
Относящегося к кальцитониновому гену пептида (CGRP) |
Увеличение ионного транспорта, частоты биения ресничек |
|
H2‑гистаминовый |
Выделение NO, бронходилататора PGE2, эпителиального расслабляющего фактора |
|
PAF |
Увеличение трансэпителиального транспорта |
|
Брадикинина |
Выделение PGE2, эпителиального расслабляющего фактора, увеличение ионного транспорта |
|
TNFa, ИЛ1, g‑ИФН |
Увеличение синтеза и секреции цитокинов. Индукция NO-синтетазы |
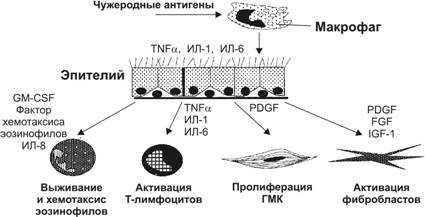
2. Синтез и секреция биологически активных веществ. На функцию эпителия воздухоносных путей влияют цитокины, действуя через соответствующие рецепторы (рис. 13-4, рис. 13-5). TNFa, ИЛ1, g-ИФН, выделяемые, например, активированными макрофагами воздухоносных путей, могут индуцировать секрецию реснитчатыми клетками ряда медиаторов воспаления. TNFa, ИЛ1 стимулируют выработку в эпителиальных клетках колониестимулирующего фактора гранулоцитов и макрофагов (GM-CSF), ИЛ8 и фактора хемотаксиса эозинофилов (ECF), усиливают экспрессию молекул адгезии реснитчатыми клетками и совместно с g-ИФН стимулируют выработку бронхо- и вазодилататора NO в эпителии. Возможно, именно действием указанных цитокинов объясняется значительное возрастание уровня NO в выдыхаемом воздухе у больных бронхиальной астмой. Эпителиальные клетки при активации соответствующих рецепторов синтезируют и секретируют эндотелин-1 (бронхо- и вазоконстриктор), ИЛ1, ИЛ6, фактор роста из тромбоцитов (PDGF), факторы роста фибробластов (FGF), инсулиноподобные факторы роста (IGF), простагландин E2, нейтральную эндопептидазу (разрушающую тахикинины), брадикинин.
Рецепторы глюкокортикоидов. Эпителиальные клетки воздухоносных путей содержат многочисленные рецепторы глюкокортикоидов. Через этот рецепторный вход реализуются различные эффекты:
Ú ингибирование синтеза цитокинов эпителиальными клетками;
Ú снижение образования NO-синтетазы, а следовательно, и уровня NO в выдыхаемом воздухе;
Ú уменьшение экспрессии молекул адгезии клеток и выработки эндотелина-1;
Ú ингибирование вызванного цитокинами синтеза простагландинов в эпителиальных клетках.
Рис. 13-4. Рецепторы реснитчатых клеток воздухоносных путей. Активация рецепторов вызывает усиление секреции медиаторов, факторов роста, цитокинов, релаксантов, экспрессии молекул адгезии, а также влияет на транспорт ионов и частоту биения ресничек. PGE2, PGD2 — простагландины PGE2 и PGD2; 15-HETE — 15-эйкозатетраноевая кислота; GM-CSF — колониестимулирующий фактор гранулоцитов и макрофагов; PDGF — тромбоцитарный фактор роста; IGF-1 — инсулиноподобный фактор роста 1; bFGF — щелочной фактор роста фибробластов; TGFb — трансформирующий фактор роста b; EpDRF — эпителиальный расслабляющий фактор. [17]
Рис. 13-5. Влияние эпителиальных клеток на другие клеточные типы в воздухоносных путях. Активированные эпителиальные клетки выделяют цитокины, которые действуют на соответствующие мишени. FGF — фактор роста фибробластов; GM-CSF — колониестимулирующий фактор гранулоцитов и макрофагов; IGF-1 — инсулиноподобный фактор роста 1; ИЛ — интерлейкины; PDGF — тромбоцитарный фактор роста; TNFa — фактор некроза опухоли a. [17]
3. Регуляция подвижности клеток. Под воздействием определённых стимулов эпителиальные клетки экспрессируют молекулы адгезии клеток, благодаря чему регулируется подвижность клеток (нейтрофилы, эозинофилы), участвующих в воспалительных реакциях.
Бокаловидные клетки
Бокаловидные клетки (бокаловидные экзокриноциты, мукоциты) составляют до 30% клеток эпителия воздухоносных путей. Клетки расположены поодиночке, содержат вакуоли со слизистым секретом в расширенной апикальной части, а в суженной базальной — выраженные комплекс Гольджи и гранулярную эндоплазматическую сеть, многочисленные митохондрии. В латеральных участках апикальной поверхности клетки имеются микроворсинки. После выделения слизи микроворсинки бокаловидных клеток становятся заметнее, вследствие чего такие клетки получили название щёточных (каёмчатых). Выделение слизи из клеток, происходящее циклически, стимулируют внешние факторы (температура, влажность). Муцины (известно 18 генов MUC) — высоко гликозилированные (содержат до 50% углеводов) макромолекулы в составе слизи, секретируемой бокаловидными клетками. Молекула муцина характеризуется многочисленными тандемными повторами, содержащими пролин, богата сериновыми и/или треониновыми остатками. Секреторные или связанные с мембраной муцины — часть мукоцилиарного защитного механизма воздухоносных путей. Различные медиаторы воспаления, секретируемые, например, при астме, хронических обструктивных заболеваниях лёгких, кистозном фиброзе (муковисцидозе) активируют гены MUC и стимулируют гиперсекрецию слизи, а также гиперплазию бокаловидных клеток. Гиперпродукция муцина и гиперплазия бокаловидных клеток могут быть следствием активации различных сигнальных путей и путей регуляции активности генов.
Базальные клетки
Базальные клетки (30% общей популяции клеток эпителия) имеют небольшие размеры, апикальная часть клетки не достигает поверхности эпителия. Эти малодифференцированные клетки способны делиться и составляют стволовую популяцию для эпителия.
Нейроэндокринные клетки
Нейроэндокринные клетки (мелкозернистые клетки) составляют до 8% общей популяции эпителия воздухоносных путей и располагаются поодиночке или группами (в составе нейроэпителиальных телец). Эти клетки содержат электроноплотные гранулы, синтезируют и накапливают бомбезин, кальцитонин, относящийся к кальцитониновому гену пептид (CGRP, кокальцигенин), серотонин, холецистокининоподобный пептид. Высокое содержание бомбезина в лёгких отмечено сразу после рождения с последующим снижением его уровня и количества нейроэндокринных клеток. Карциноидные опухоли и некоторые мелкоклеточные карциномы лёгких характеризуются высоким содержанием этого пептида.
Нейроэпителиальные тельца расположены в местах ветвления воздухоносных путей. Тельце состоит из 4–25 клеток, снабжённых микроворсинками и контактирующих с чувствительными нервными терминалями. Клетки телец содержат сенсорную систему, регистрирующую содержание О2. Снижение концентрации О2 ведёт к деполяризации плазмолеммы и возбуждении клетки тельца с последующей секрецией серотонина. Серотонин вызывает расширение воздухоносных путей.
Каёмчатые клетки
Каёмчатые (щёточные) клетки — гетерогенная популяция клеток, имеющих многочисленные микроворсинки в апикальной части. К щёточным клеткам относят освободившиеся от секрета бокаловидные клетки, хеморецепторные клетки, а также дифференцирующиеся реснитчатые клетки.
Хеморецепторные клетки
Гранулосодержащие клетки с микроворсинками, связаны с афферентными нервными терминалями.
Вегетативные нервные терминали
В собственном слое слизистой оболочки присутствуют терминали нервных волокон вегетативного отдела нервной системы, секретирующие нейромедиаторы: для блуждающего нерва — ацетилхолин; для нейронов симпатического ствола — норадреналин. Симпатические нервные волокна проводят импульсы, вызывающие расширение бронхов и сужение кровеносных сосудов; импульсы, проходящие по парасимпатическим нервным волокнам, оказывают эффект бронхоконстрикции и вазодилатации.
· Норадреналин, активируя b2-адренорецепторы реснитчатых клеток эпителия, усиливает транспорт ионов через эпителий и увеличивает частоту биения ресничек; последнее способствует более быстрому удалению слизи из просвета воздухоносных путей.
· Ацетилхолин, активируя м3-холинорецепторы, стимулирует транспорт ионов через эпителий, а также увеличивает частоту биения ресничек у реснитчатых клеток.
· Секреция нейропептидов. В собственном слое присутствуют немиелинизированные волокна С-типа и миелинизированные волокна А-типа. Часть нервных волокон проникает в эпителий, часть контактирует с ГМК. Волокна секретируют ряд нейропептидов, влияющих на функции клеток эпителия и ГМК сосудов и мышечного слоя слизистой оболочки. Некоторые нейропептиды генерируют и поддерживают воспалительный процесс, называемый «нейрогенным».
à Парасимпатические нервные терминали секретируют VIP, действующий аналогично агонистам b2-адренорецепторов реснитчатых клеток. VIP способствует ионному транспорту через эпителиальные клетки, а также является бронхо- и вазодилататором.
à Чувствительные нервные терминали (С-афференты) секретируют тахикинины — вещество P и нейрокинин А. Активация тахикининами NK1-рецепторов реснитчатых клеток приводит к увеличению ионного транспорта и частоты биения ресничек. Вещество P и нейрокинин А вызывают бронхоконстрикцию и вазодилатацию, увеличивают проницаемость сосудистой стенки; последнее может привести к развитию нейрогенного воспаления. Вещество P и нейрокинин А способствуют высвобождению из тучных клеток и лейкоцитов простагландина Е2, цитокинов (ИЛ, TNFa) и биогенных аминов, которые, воздействуя на мембрану нервных окончаний, запускают метаболические процессы, повышающие возбудимость ноцицептивных афферентов и снижающие болевой порог.
à Чувствительные нервные окончания секретируют относящийся к кальцитониновому гену пептид (CGRP, кокальцигенин), его действие на реснитчатые клетки эпителия аналогично действию агонистов b2-адренорецепторов и VIP. Кокальцигенин регулирует пролиферацию эпителиальных клеток.
Рецепторные нервные окончания
Рецепторные нервные окончания воздухоносных путей и респираторного отдела регистрируют изменения объёмов лёгких, наличие посторонних частиц и раздражающих веществ и проводят информацию по нервным волокнам блуждающего и языкоглоточного (от верхних отделов воздухоносных путей) нервов к нейронам ЦНС. К рецепторам этой группы относятся медленно адаптирующиеся рецепторы растяжения, быстро адаптирующиеся ирритантные рецепторы и J–рецепторы.
Медленно адаптирующиеся рецепторы растяжения расположены среди ГМК мышечного слоя слизистой оболочки, регистрируют растяжение стенки воздухоносных путей и проводят импульсы по миелинизированным нервным волокнам A-типа. При возбуждении рецепторы запускают рефлекс Херинга–Бройера (подавление длительности вдоха и увеличение продолжительности выдоха). При обструктивных заболеваниях увеличенный объём лёгкого постоянно стимулирует рецепторы растяжения, что приводит к отсрочке следующего вдоха на фоне длительного затруднённого выдоха.
Быстро адаптирующиеся ирритантные (раздражающие) рецепторы (миелинизированные нервные волокна A-типа) расположены между эпителиальными клетками слизистой оболочки крупных воздухоносных путей. Рецепторы главным образом реагируют на действие поступающих при вдохе раздражающих агентов (например, аммиака, табачного дыма, пыли, холодного воздуха), а также на наличие в стенке воздухоносных путей гистамина, простагландинов и брадикинина. При возбуждении ирритантных рецепторов увеличивается сопротивление воздухоносных путей, рефлекторно возникает задержка дыхания и кашель.
J–рецепторы (от англ. juxtacapillary — околокапиллярные) (безмиелиновые волокна C-типа) расположены в межальвеолярных перегородках, являются как хемо– так и механорецепторами. J–рецепторы возбуждаются при перерастяжении ткани лёгкого, а также при воздействии различных экзо- и эндогенных химических соединений (капсаицин, гистамин, брадикинин, серотонин, простагландины). Стимуляция J-рецепторов приводит к рефлекторной задержке дыхания с последующим появлением частого и поверхностного дыхания, сужению просвета воздухоносных путей (бронхоконстрикции), увеличению секреции слизи, а также к падению АД и брадикардии. J–рецепторы реагируют на переполнение кровью лёгочных капилляров и увеличение объёма интерстициальной жидкости альвеол, что возможно при левожелудочковой недостаточности и приводит к появлению диспноэ (одышки).
Бронхиолярные экзокриноциты
Бронхиолярные экзокриноциты расположены в терминальных бронхиолах между реснитчатыми клетками и формируют дистальные (безреснитчатые) участки бронхиального эпителия. Для этих клеток характерны куполообразная форма, отсутствие ресничек, локализация митохондрий и гладкой эндоплазматической сети в базальной части клетки, а в апикальной — электронно-плотных гранул. Гранулы содержат специфический для бронхиолярных экзокриноцитов белок CC10. В цитоплазме также присутствуют гранулярная эндоплазматическая сеть, комплекс Гольджи, множество пузырьков и мультивезикулярных телец.
Бронхиолярные экзокриноциты выполняют ряд функций:
· секретируют гликозаминогликаны, определяющие консистенцию секрета бронхиол. Полагают, что клетки служат источником липопротеинов сурфактанта терминальных бронхиол;
· модулируют воспалительные реакции в дистальных воздухоносных путях, что опосредовано белком CC10;
· содержат неспецифические эстеразы и участвуют в работе детоксикационной системы лёгких. Неспецифические эстеразы также присутствуют в пневмоцитах типа II, в альвеолярных макрофагах, в клетках эндотелия. Бронхиолярные экзокриноциты участвуют в инактивации поступающих с вдыхаемым воздухом токсинов при помощи холестерол монооксигеназы (цитохром P450) — фермента, в большом количестве содержащегося в цистернах эндоплазматической сети.
Подслизистая оболочка
Подслизистая оболочка содержит слизистые и белково-слизистые железы. По мере уменьшения калибра бронхов количество желёз уменьшается.
Фиброзно-хрящевая оболочка
Фиброзно-хрящевая оболочка представлена гиалиновым хрящом, образующим кольца в трахее и главных бронхах, пластинки и небольшие островки вплоть до мелких бронхов. В бронхах малого калибра и бронхиолах фиброзно-хрящевая оболочка отсутствует.
Наружная оболочка
Наружная (адвентициальная) оболочка образована волокнистой соединительной тканью, в дистальных отделах связанная с междолевой, междольковой и внутридольковой соединительной тканью лёгких.
Носовая полость
Носовая полость включает в себя преддверие и собственно носовую (дыхательную) полость. Преддверие выстлано тонкой кожей, содержащей сальные, потовые железы и волосяные фолликулы. Дыхательная полость выстлана слизистой оболочкой, сменившей тонкую кожу; здесь эпидермис переходит в многорядный мерцательный эпителий, содержащий бокаловидные, базальные клетки и клетки с микроворсинками. Собственный слой слизистой оболочки содержит коллагеновые и эластические волокна, а также слизистые и белковые железы, вырабатывающие большое количество слизи.
Сосуды
В собственном слое в значительном количестве присутствуют тонкостенные полости, выстланные эндотелием и окружённые циркулярно и продольно направленными ГМК. Обычно полости находятся в спавшемся состоянии, но способны, растягиваясь, накапливать значительное количество крови, что увеличивает толщину слизистой оболочки. Кровь поступает по артериолам, имеющим сфинктеры и регулирующим приток, а оттекает по венулам с большим количеством циркулярно ориентированных ГМК (сфинктеры, регулирующие отток). В зависимости от реальной ситуации (терморецепторы регистрируют температуру воздуха), к артериолам и венулам поступают по двигательным нервным окончаниям вегетативного отдела нервной системы импульсы, регулирующие степень сокращения ГМК этих сосудов.
Гортань
Гортань — верхний отдел воздухоносных путей; основная функция, помимо проведения воздуха, — голосообразование. Отделена от глотки надгортанником, а в нижней части ограничена первым хрящевым полукольцом трахеи. Имеет слизистую, фиброзно-хрящевую и адвентициальную оболочки. В состав фиброзно-хрящевой оболочки гортани входят 4 хряща — надгортанный, щитовидный, черпаловидный, перстневидный. Эпителий слизистой оболочки (за исключением голосовых связок) — многорядный мерцательный. Собственный слой передней поверхности гортани содержит смешанные белково-слизистые железы, скопления лимфатических фолликулов.
Голосовые связки
Голосовые связки — верхние и нижние складки слизистой оболочки в средней части органа, образующие соответственно ложные и истинные голосовые связки. Пространство между истинными голосовыми связками — голосовая щель. Область расширения просвета гортани между двумя рядами связок — желудочек гортани. Основу ложных голосовых связок составляет рыхлая соединительная ткань, содержащая белково-слизистые железы. Такие железы имеются также выше и ниже истинных голосовых связок. Истинные голосовые связки содержат пучки поперечнополосатых мышечных волокон; железы отсутствуют. Оба типа голосовых связок, как и передняя поверхность надгортанника, покрыты многослойным плоским неороговевающим эпителием.
Трахея
Стенка трахеи (рис. 13-6) образована слизистой, подслизистой, фиброзно-хрящевой и адвентициальной оболочками.
Слизистая оболочка
Слизистая оболочка состоит из однослойного многорядного мерцательного эпителия и тонкого собственного слоя. Мышечный слой отсутствует. Собственный слой слизистой оболочки содержит многочисленные эластические волокна и немного слизистых желёз. Здесь встречаются отдельные лимфоциты и лимфатические фолликулы.
Эпителий трахеи содержит различные типы клеток (рис.13-6А). Реснитчатые клетки составляют основную часть эпителия. Среди реснитчатых рассеяны бокаловидные, базальные, щёточные (каёмчатые), нейроэндокринные, хеморецепторные клетки.
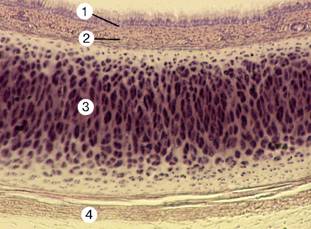
Рис. 13-6. Трахея. Стенка образована четырьмя оболочками. Слизистая оболочка (1) состоит из многорядного мерцательного эпителия и собственного слоя. Для подслизистой оболочки (2) характерны многочисленные слизистые и белково-слизистые железы. Фиброзно-хрящевая оболочка (3) представлена незамкнутыми кольцами гиалинового хряща. Адвентициальная оболочка (4) образована волокнистой соединительной тканью. Окраска гематоксилином и эозином.
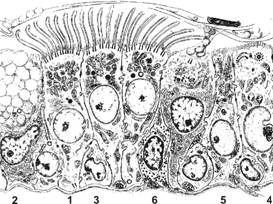
Рис. 13-6А. Многорядный эпителий слизистой оболочки трахеи. В состав эпителия входят различные типы клеток. Первый (основной) тип (1) — реснитчатые клетки, имеющие на апикальной поверхности более 200 ресничек. Второй тип (2) — высокие бокаловидные клетки, содержащие вакуоли со слизистым секретом в апикальной части, а в базальной — ядро и различные органеллы. Третий тип (3) — базальные (стволовые) клетки, имеющие небольшие размеры. Четвёртый тип (4) — щёточные (каёмчатые) клетки. Пятый тип (5) — хеморецепторные клетки, содержащие мелкую зернистость и образующие контакт с афферентными терминалями. Шестой тип (6) — нейроэндокринные клетки с многочисленными мелкими гранулами. [17]
Подслизистая оболочка
Границей между слизистой и подслизистой оболочками служит уплотнённая пластинка переплетённых эластических волокон. В подслизистой оболочке расположено множество кровеносных сосудов и секреторных отделов слизистых и белково-слизистых желёз.
Фиброзно-хрящевая оболочка
Фиброзно-хрящевая оболочка представлена пластинками в виде незамкнутых колец гиалинового хряща, окружённого тонкой фиброзной оболочкой — надхрящницей. Концы колец соединены пучками соединительнотканных волокон и ГМК. Соседние кольца соединяет между собой плотная соединительная ткань (переплетённые коллагеновые и отдельные эластические волокна), переходящая в надхрящницу колец.
Бронхи
Строение бронхов (рис. 13-6Б) сходно со строением трахеи, но имеются и определённые различия.
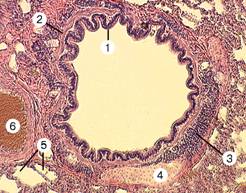
Рис. 13-6Б. Бронх среднего калибра. Слизистая оболочка выстлана многорядным цилиндрическим мерцательным эпителием (1), имеет мышечный слой (2). В подслизистой оболочке присутствуют слизистые железы (3). Фиброзно-хрящевая оболочка содержит пластины гиалинового хряща (4). Вокруг бронха видны альвеолы (5), в соединительнотканных перегородках паренхимы лёгкого проходят кровеносные сосуды (6). Окраска гематоксилином и эозином.
Слизистая оболочка
Слизистая оболочка бронхов, в отличие от трахеи, обладает мышечным слоем. Этот слой состоит из ГМК, расположенных в виде двух противоположно направленных (по часовой и против часовой стрелки) спиралей. Сокращение ГМК приводит к образованию продольных складок слизистой оболочки бронха. Собственный слой слизистой оболочки содержит множество эластических волокон, организованных в виде нескольких длинных лент, идущих параллельно. Ленты переходят в эластические компоненты терминальных бронхиол. Эпителий слизистой оболочки бронхов — однослойный многорядный цилиндрический мерцательный, в нём имеются реснитчатые, бокаловидные, каёмчатые, эндокринные и базальные клетки.
Подслизистая оболочка
Подслизистая оболочка содержит слизистые и белково-слизистые железы. Железы располагаются группами, особенно в тех участках, где отсутствует хрящ. В бронхах малого калибра железы отсутствуют. Образование слизи секреторными клетками желёз (а также бокаловидными клетками эпителия) и её вязкость регулируется трансмембранными Na+-каналами и Cl–-каналами CFTR (Cystic Fibrosis Transmembrane conductance Regulator) (рис. 13-7). Клетка секретирует ионы Cl– через каналы CFTR; ионы Na+ через Na+-каналы поступают в клетку и далее в подлежащую соединительную ткань, вслед за Na+ следует вода. Мутация гена CFTR ведёт к нарушению или блокаде секреции Cl– и чрезмерной абсорбции Na+ и воды Это вызывает повышение вязкости секрета бокаловидных клеток и секреторных клеток бронхиальных желёз и закупорку выводных протоков (муковисцидоз).
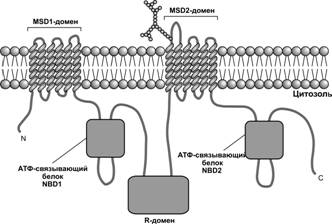
· CFTR — гликопротеин 170 кД, относится к надсемейству АТФ-связывающих кассетных белков (ABC–белков, ATP-binding cassette), функционирует как апикальный Cl–-канал. Молекула содержит два трансмембранных домена (MSD1 и MSD2), состоящих из 6 сегментов каждый, два АТФ-связывающих домена (NBD1 и NBD2) и цитоплазматический регуляторный R-домен, разделяющий две половины молекулы (рис. 13-7). Канал активируется при фосфорилировании R-домена протеинкиназой А, а также при взаимодействии АТФ с NBD1 и NBD2. Гидролиз АТФ в домене NBD2 приводит к закрытию канала. Дефосфорилирование R-домена возвращает канал в покоящееся состояние. Приблизительно у 80% больных муковисцидозом зарегистрированы мутации CFTR, приводящие к нарушению транспорта CFTR из эндоплазматической сети и встраивания его в плазматическую мембрану эпителиальных клеток. Наиболее часто встречается мутация DF508 (отсутствие фенилаланина в позиции 508 домена NBD1) канала; DF508-CFTR не достигают плазмолеммы.
· Амилорид-чувствительный натриевый канал ENaC. Найден во всех эпителиях, содержащих CFTR. Участвует в транспорте Na+ и воды в эпителиальных клетках почек, лёгких, толстой кишки. Современные подходы в лечении муковисцидоза предполагают попытки заблокировать этот канал.
Рис. 13-7. Структура Cl–-канала CFTR. Молекула включает цитоплазматический регуляторный R-домен, два АТФ-связывающих домена, NBD1 и NBD2, и два мембранных домена MSD1 и MSD2, каждый из которых содержит 6 трансмембранных сегментов. [114]
Фиброзно-хрящевая оболочка
Хрящи в виде незамкнутых колец, присутствующие в главных бронхах, в крупных внутрилёгочных бронхах сменяются хрящевыми пластинками неправильной формы, а затем островками хрящевой ткани (бронхи среднего калибра). Пространства между хрящами заполнены соединительной тканью, переходящей в надхрящницу. В бронхах малого калибра хрящевой ткани нет.
Наружная оболочка
Адвентициальная оболочка — соединительная ткань, переходящая в междолевую и междольковую соединительную ткань паренхимы лёгкого.
Бронхиолы
Бронхиолы отличаются от бронхов по ряду признаков: их диаметр значительно меньше и составляет от 0,5 до 1 мм. Эпителий слизистой оболочки — однорядный цилиндрический мерцательный; его высота меньше, чем в бронхах. В эпителии более крупных бронхиол преобладают реснитчатые клетки, между которыми расположены бронхиолярные экзокриноциты. В стенке бронхиол отсутствуют хрящи и железы. Таким образом, стенка бронхиол состоит из следующих элементов: однорядного цилиндрического (кубического) эпителия, тонкого и эластичного собственного слоя, мышечного слоя слизистой оболочки и наружной соединительной ткани. Всего образуется 20 генераций бронхиол, мельчайшими из которых являются терминальные бронхиолы.
Изменения стенки бронхов по мере уменьшения их калибра
Снижение высоты эпителиального пласта слизистой (от многорядного цилиндрического до двухрядного, а затем — однорядного в бронхах малого калибра и однорядного кубического в терминальных бронхиолах) с постепенным снижением количества, а затем и исчезновением бокаловидных клеток. В дистальных участках терминальных бронхиол реснитчатые клетки отсутствуют, но имеются бронхиолярные экзокриноциты.
Уменьшение толщины слизистой оболочки.
Возрастание количества эластических волокон.
Возрастание количества ГМК, так что с уменьшением калибра бронхов мышечный слой слизистой оболочки становится более выраженным.
Уменьшение размеров пластинок и островков хрящевой ткани с последующим её исчезновением.
Уменьшение количества слизистых желёз с их исчезновением в бронхах малого калибра и в бронхиолах.
Респираторный отдел лёгкого осуществляет функцию внешнего дыхания — газообмен между двумя средами — внешней и внутренней. С понятием респираторный отдел связаны представления об ацинусе и лёгочной дольке.
Ацинус
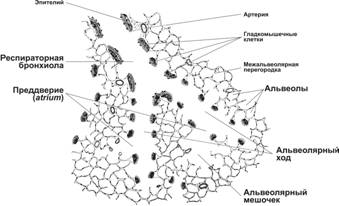
Респираторный отдел представляет собой совокупность ацинусов (рис. 13-8). Ацинус начинается респираторной бронхиолой первого порядка, которая дихотомически делится на респираторные бронхиолы второго, а затем третьего порядков. Каждая респираторная бронхиола третьего порядка, в свою очередь, подразделяется на альвеолярные ходы, переходящие в преддверие и далее — в альвеолярные мешочки. В просвет респираторной бронхиолы и альвеолярных ходов открываются альвеолы. Преддверие и альвеолярные мешочки фактически являются пустотами, образованными альвеолами.
Рис. 13-8. Лёгочный ацинус. Лёгочные ацинусы составляют респираторный отдел лёгких. От терминальных бронхиол отходят респираторные бронхиолы первого порядка, которые дают начало ацинусам. Бронхиолы делятся на респираторные бронхиолы второго и третьего порядка. Каждая из последних разделяется на два альвеолярных хода. Каждый альвеолярный ход через преддверие переходит в два альвеолярных мешочка. В стенках респираторных бронхиол и альвеолярных ходов имеются мешковидные выпячивания — альвеолы. Альвеолы образуют преддверия и альвеолярные мешочки. Между ацинусами имеются тонкие прослойки соединительной ткани. В состав лёгочной дольки входит 12–18 ацинусов. [17]
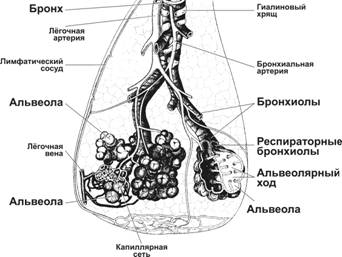
Лёгочная долька
Лёгочная долька (рис. 13-9) состоит из 12–18 ацинусов, разделённых тонкими прослойками соединительной ткани. Неполные фиброзные междольковые перегородки отделяют друг от друга соседние дольки.
Рис. 13-9. Лёгочная долька. Дольки лёгкого имеют форму пирамид с вершиной, через которую входит кровеносный сосуд и терминальная бронхиола. Основание дольки обращено наружу, к поверхности лёгкого. Бронхиола, проникая в дольку, ветвится и даёт начало респираторным бронхиолам, являющимся частью лёгочных ацинусов. Последние также имеют форму пирамид, обращённых основанием наружу. [17]
Альвеолы
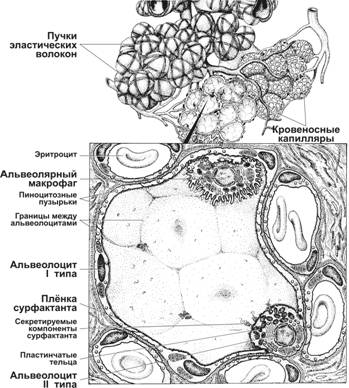
Альвеолы (рис. 13-10) выстланы однослойным эпителием, расположенным на базальной мембране. Клеточный состав эпителия — пневмоциты типов I и II. Клетки образуют между собой плотные контакты. Альвеолярная поверхность покрыта тонким слоем воды и сурфактанта.
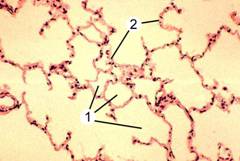
Рис. 13-10. Альвеолы — мешковидные пустоты, разделённые тонкими перегородками. Снаружи к альвеолам вплотную примыкают кровеносные капилляры, образующие густую сеть. Капилляры окружены эластическими волокнами, оплетающими альвеолы в виде пучков. Альвеола выстлана однослойным эпителием (см. врезку). Цитоплазма большинства эпителиальных клеток максимально уплощена (пневмоциты типа I). В ней присутствует множество пиноцитозных пузырьков. Пиноцитозные пузырьки в изобилии имеются также в плоских эндотелиальных клетках капилляров. Между пневмоцитами типа I располагаются клетки кубической формы — пневмоциты типа II. Для них характерно наличие в цитоплазме пластинчатых телец, содержащих сурфактант. Сурфактант секретируется в полость альвеолы и образует на поверхности тонкого слоя воды, покрывающего альвеолярный эпителий, мономолекулярную плёнку. Из межальвеолярных перегородок в просвет альвеол могут мигрировать макрофаги. Перемещаясь по поверхности альвеолы, они образуют многочисленные цитоплазматические отростки, с помощью которых захватывают посторонние частицы, поступающие с воздухом. [17]
Пневмоциты типа I
Пневмоциты типа I (респираторные пневмоциты) покрывают почти 95% альвеолярной поверхности. Это плоские клетки с уплощёнными выростами; выросты соседних клеток перекрывают друг друга, смещаясь при вдохе и выдохе. По периферии цитоплазмы имеется много пиноцитозных пузырьков. Клетки не способны делиться. Функция пневмоцитов типа I — участие в газообмене. Эти клетки входят в состав аэрогематического барьера.
Пневмоциты типа II
Пневмоциты типа II вырабатывают, накапливают и секретируют компоненты поверхностноактивного вещества — сурфактанта. Клетки имеют кубическую форму. Они встроены между пневмоцитами типа I, возвышаясь над последними; изредка образуют группы из 2–3 клеток. На апикальной поверхности пневмоциты типа II имеют микроворсинки. Особенностью этих клеток является присутствие в цитоплазме пластинчатых телец диаметром 0,2–2 мкм. Окружённые мембраной тельца состоят из концентрических слоёв липидов и белков. Пластинчатые тельца пневмоцитов типа II относят к лизосомоподобным органеллам, накапливающим вновь синтезированные и рециклированные компоненты сурфактанта. В ограничивающей пластинчатые тельца мембране присутствует белок ABCA3 семейства кассетных АТФ-связывающих белков (ABC–белков), участвующий в накоплении фосфолипидов сурфактанта в пластинчатых тельцах. При дыхательной недостаточности новорождённых образование дефектных пластинчатых телец связано с аномалиями белка ABCA3. Мутации гена ABCA3 ассоциированы с недостаточностью фосфатидилхолина сурфактанта, что приводит к фатально сниженной функции сурфактанта у младенцев. Для формирования структуры пластинчатого тельца важно также присутствие белка сурфактанта SP-B. При недостаточности SP-B формируются дефектные пластинчатые тельца.
Пластинчатые тельца подвергаются созреванию и регулируемой секреции в альвеолярное пространство. Каждый час в нормальном лёгком секретируется в альвеолярное пространство примерно 10% материала, накопленного в пластинчатых тельцах. Секреция происходит по нескольким сигнальным путям: активация аденилатциклазы, протеинкиназы C, цАМФ-зависимой протеинкиназы и Ca2+-регулируемая активация Ca2+-кальмодулин-зависимой протеинкиназы. Экзоцитоз телец происходит с участием аннексина II и a-SNAP/NSF; содержимое пластинчатых телец высвобождается через поры, формируемые при слиянии мембран тельца и пневмоцита.
Гигантские пластинчатые тельца и пенистые пневмоциты типа II наблюдаются при синдроме Хермански-Пудлак (нарушение обмена ароматических аминокислот). Одно из проявлений синдрома — развитие лёгочного фиброза как следствие накопления цероидного липофусцина в лизосомах.
Межальвеолярная перегородка
Межальвеолярная перегородка (рис. 13-10А) содержит капилляры, заключённые в сеть эластических волокон, окружающих альвеолы. Эндотелий альвеолярного капилляра — уплощённые клетки, содержащие в цитоплазме пиноцитозные пузырьки. В межальвеолярных перегородках имеются небольшие отверстия — альвеолярные поры. Эти поры создают возможность для проникновения воздуха из одной альвеолы в другую, что облегчает воздухообмен. Через поры в межальвеолярных перегородках происходит также миграция альвеолярных макрофагов.
Рис. 13-10А. Паренхима лёгкого имеет губчатый вид из-за наличия множества альвеол (1), разделённых тонкими межальвеолярными перегородками (2). Окраска гематоксилином и эозином.
Аэрогематический барьер
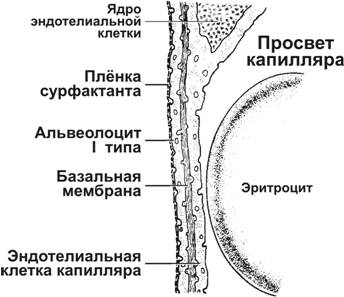
Между полостью альвеолы и просветом капилляра происходит газообмен путём простой диффузии газов в соответствии с их концентрациями в капиллярах и альвеолах (рис. 13-11). Следовательно, чем меньше структур между полостью альвеолы и просветом капилляра, тем эффективнее диффузия. Уменьшение пути диффузии достигается за счёт уплощения клеток — пневмоцитов типа I и эндотелия капилляра, а также за счёт слияния базальных мембран эндотелия капилляра и пневмоцита типа I и формирования одной общей мембраны. Таким образом, аэрогематический барьер образуют: альвеолярные клетки типа I (0,2 мкм), общая базальная мембрана (0,1 мкм), уплощённая часть эндотелиальной клетки капилляра (0,2 мкм). В сумме это составляет около 0,5 мкм.
Респираторный обмен CO2 (см. также главу 6 и рис. 6-2). СО2 транспортируется кровью преимущественно в виде иона бикарбоната НСО3– в составе плазмы. В лёгких, где pО2 = 100 мм рт.ст., комплекс дезоксигемоглобин–Н+ эритроцитов крови, поступаемой в альвеолярные капилляры от тканей, диссоциирует. HCO3– транспортируется из плазмы в эритроциты в обмен на внутриклеточный Cl– при помощи специального анионообменника (белка полосы 3) и соединяется с ионами Н+, образуя СО2 ± Н2О; дезоксигемоглобин эритроцита связывает O2, образуя оксигемоглобин. СО2 выделяется в просвет альвеол.
Рис. 13-11. Аэрогематический барьер — совокупность структур, через которые диффундируют газы в лёгких. Газообмен происходит через уплощённую цитоплазму пневмоцитов типа I и эндотелиальных клеток капилляров. В состав барьера также входят базальная мембрана, общая для эпителия альвеолы и эндотелия капилляра. [17]
Интерстициальное пространство
Утолщённый участок стенки альвеолы, где не происходит слияния базальных мембран эндотелия капилляра и альвеолярного эпителия (так называемая «толстая сторона» альвеолярного капилляра) состоит из соединительной ткани и содержит коллагеновые и эластические волокна, создающие структурный каркас альвеолярной стенки, протеогликаны, фибробласты, липофибробласты и миофибробласты, тучные клетки, макрофаги, лимфоциты. Такие участки называют интерстициальным пространством (интерстицием).
Диффузия жидкости в лёгких
В отличие от альвеолярного эпителия, между эндотелиальными клетками альвеолярных капилляров, а также прекапиллярных артериол и посткапиллярных венул, нет плотных контактов, что позволяет воде и растворённым в ней низкомолекулярным веществам, мелким белкам плазмы пассивно перемещаться из просвета сосуда сквозь стыки между клетками эндотелия в интерстиций. Поскольку клетки альвеолярного эпителия соединены плотными контактами, в нормальном лёгком не происходит пассивного перемещения растворимых соединений из интерстиция в воздушное пространство альвеол. Микрососудистый фильтрат по градиенту гидростатического давления направляется от альвеолярных стенок к терминальным лимфатическим сосудам, составляя часть лимфы, и прокачивается под действием перистальтики к лимфатическим сосудам корней лёгких, далее — по средостенным лимфатическим сосудам, через лимфатические узлы в грудной проток, после чего возвращается в кровь.
Удаление воды из альвеолярных пространств. Альвеолярный эпителий покрыт тонким слоем воды. В апикальной мембране пневмоцитов типа II присутствуют Na+-каналы. Na+ поступает в клетку через каналы по градиенту концентрации, а затем перекачивается в интерстиций с помощью Na+, K+-АТФазы базолатеральной мембраны клетки. Этот транспорт Na+ создаёт осмотический градиент, который функционирует для реабсорбции воды из альвеолярных пространств. Опосредованное цАМФ удаление воды через альвеолярный эпителий может происходить с участием как Na+-каналов, так и CFTR.
Отёк лёгких — накопление жидкости в лёгочном интерстиции и альвеолярных пространствах. Отёк лёгких возникает в ситуации, когда жидкость выходит из микрососудистого русла в интерстициальное пространство быстрее, чем оттекает из последнего по лимфатическим сосудам.
Сурфактант
Общее количество сурфактанта в лёгких крайне невелико. На 1 м2 альвеолярной поверхности приходится около 50 мм3 сурфактанта. Толщина его плёнки составляет 3% общей толщины аэрогематического барьера. Основное количество сурфактанта вырабатывается у плода после 32-й недели беременности, достигая максимального количества к 35-й неделе. До рождения образуется избыток сурфактанта. После рождения этот избыток удаляется альвеолярными макрофагами. Удаление сурфактанта из альвеол происходит несколькими путями: через бронхиальную систему, через лимфатическую систему и при помощи альвеолярных макрофагов. Для гомеостаза и рециклирования сурфактанта необходим GM-CSF, рецепторы которого присутствуют на поверхности пневмоцитов типа II и макрофагов.
После секреции на тонкий слой воды, покрывающий альвеолярный эпителий, сурфактант подвергается структурным перестройкам: в водном слое сурфактант приобретает сетчатую форму, известную как тубулярный миелин, богатый апопротеинами; затем сурфактант перестраивается в непрерывный монослой.
Сурфактант регулярно инактивируется и конвертируется в мелкие поверхностно-неактивные агрегаты. Примерно 70–80% таких агрегатов захватывается пневмоцитами типа II, заключается в фаголизосомы, а затем катаболизируется или используется вновь. Альвеолярные макрофаги фагоцитируют остальной пул мелких агрегатов сурфактанта, и этот процесс зависит от GM-CSF. Нарушение GM-CSF-сигнального пути в альвеолярном макрофаге приводит к неспособности фагоцита катаболизировать сурфактант. В результате в макрофаге формируются и накапливаются окружённые мембраной пластинчатые агрегаты сурфактанта («пенистый» макрофаг). Одновременно происходит прогрессирующее накопление внеклеточного сурфактанта и клеточных обломков в альвеолярном пространстве, возможности для газообмена уменьшаются, развивается клинический синдром альвеолярного протеиноза.
Мутации гена, кодирующего bc-цепи рецептора GM-CSF, — одна из причин развития врождённой формы альвеолярного протеиноза. Приобретённый (идиопатический) альвеолярный протеиноз — аутоиммунное заболевание, связанное с образованием аутоантител к GM-CSF.
Состав
Лёгочный сурфактант — эмульсия фосфолипидов, белков и углеводов; 80% составляют глицерофосфолипиды, 10% — холестерин и 10% — белки. Главный поверхностно-активный компонент — дипальмитоилфосфатидилхолин (дипальмитоиллецитин), — ненасыщенный фосфолипид (содержащий две цепи полностью насыщенных жирных кислот — пальмитаты), составляющий более 50% фосфолипидов сурфактанта. Сурфактант также содержит большое количество фосфатидилхолина, в молекуле которого присутствуют цепи ненасыщенных жирных кислот и фосфатидилглицерол (около 11% липидов).
Примерно половину белков сурфактанта составляют белки плазмы (преимущественно альбумины) и IgA. Сурфактант содержит ряд уникальных белков, способствующих адсорбции дипальмитоилфосфатидилхолина на границе двух фаз. Среди белков сурфактанта выделяют апопротеины SP-A, SP-B, SP-C, SP-D.
SP-A и SP-D — водорастворимые апопротеины, молекулы которых содержат коллагеноподобные домены. SP-A и SP-D относятся к семейству белков, известных как коллектины (коллагеноподобные лектины), имеющие первичную структуру из 4-х доменов: дисульфид-формирующий NH2-конец, коллагеноподобный участок (хвост молекулы), извитой шеечный участок и COOH–концевой распознающий углеводы домен (глобулярная головка) (рис. 13-12Б). SP-A и SP-D связываются через свои распознающие углевод домены с сахарами и гликолипидами на поверхности микроорганизмов. SP-A и SP-D формируют тримеры и олигомеры, что значительно увеличивает эффективность связывания патогенов. Таким образом, SP-A и SP-D вносят вклад во врождённый иммунитет, действуя как опсонины, способствуя таким образом фагоцитозу бактерий и вирусов альвеолярными макрофагами. SP-A участвует в формировании тубулярного миелина, а также важен в осуществлении обратной связи контроля секреции сурфактанта.
SP-B и SP-C — гидрофобные апопротеины, увеличивающие степень поступления сурфактанта на границу «вода–воздух» и ускоряющие его распределение в виде поверхностного монослоя. SP-B и SP-C ответственны за уменьшение поверхностного натяжения. SP-B важен для формирования пластинчатых телец в пневмоцитах типа II. SP-B, как и SP-A, участвует в формировании тубулярного миелина. Врождённое отсутствие SP-B приводит к респираторному дистресс-синдрому.
Врождённый альвеолярный протеиноз возникает вследствие дефекта в образовании белков сурфактанта, а именно отсутствия сурфактантного белка B (SP-B) и его мРНК, а также заметного увеличения содержания сурфактантного белка C (SP-C). Дети умирают в течение первого года жизни, несмотря на интенсивную терапию.
Регуляция выработки сурфактанта
Образованию компонентов сурфактанта у плода способствуют глюкокортикоиды, пролактин, гормоны щитовидной железы, эстрогены, андрогены, факторы роста, инсулин, b-адренергические агонисты, цAMФ. Глюкокортикоиды усиливают синтез SP-A, SP-B и SP-C в лёгких плода. У взрослых продукцию сурфактанта регулируют ацетилхолин и простагландины.
Функции сурфактанта
Сурфактант имеет важное значение при первом вдохе ребёнка. Поверхностное натяжение максимально в лёгких, пока альвеолы ещё не расправлены. Если младенец родится ранее 35-й недели беременности, то трудно ожидать, что альвеолярная система откроется без терапевтической стимуляции пневмоцитов типа II. Степень дифференцировки альвеолярного эпителия и его способность формировать сурфактант, таким образом, рассматривается как важный признак зрелости лёгких недоношенных детей. Недостаточная выработка компонентов сурфактанта приводит к слипанию альвеол.
Респираторный дистресс-синдром новорождённых развивается у недоношенных детей вследствие незрелости пневмоцитов типа II. Из-за недостаточного количества сурфактанта, выделяемого этими клетками на поверхность альвеол, последние оказываются нерасправленными (ателектаз). В результате развивается дыхательная недостаточность. Из-за ателектаза альвеол газообмен осуществляется через эпителий альвеолярных ходов и респираторных бронхиол, что ведёт к их повреждению.
Снижение поверхностного натяжения
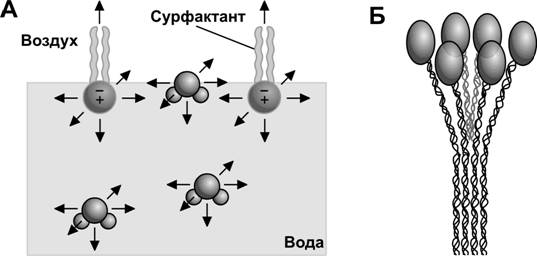
Снижение поверхностного натяжения на границе «вода–воздух» — главная функция сурфактанта. Молекулы фосфолипидов монослоя сурфактанта встраиваются между поверхностными молекулами воды; при этом гидрофобные хвосты тянут молекулы фосфолипидов вверх, в сторону просвета альвеолы, а гидрофильные полярные головки направлены к водному слою, покрывающему альвеолярный эпителий, и притягивают поверхностные молекулы воды (рис. 13-12А). Таким образом, плотность молекул воды на границе «вода–воздух» снижается. Поскольку сурфактант уменьшает поверхностное натяжение, это увеличивает податливость лёгких, облегчая их расширение при вдохе. В отсутствие сурфактанта повышенное поверхностное натяжение увеличивает тенденцию образования воздушных пузырьков и их слияния внутри альвеолы (эффект «вскипания»), что способствует поступлению воды из интерстиция в альвеолярное пространство. В результате расстояние между воздухом и кровью увеличивается, что нарушает диффузию газов.
Сурфактант способствует поддержанию относительно одинаковых размеров альвеол в ходе респираторного цикла, что важно для нормального газообмена.
Рис. 13-12. Сурфактант. А —сурфактант снижает поверхностное натяжение на границе «вода–воздух», уменьшая количество молекул воды в поверхностном слое; Б — структура белка сурфактанта SP-A. [114]
Сурфактант — компонент защитной системы лёгких
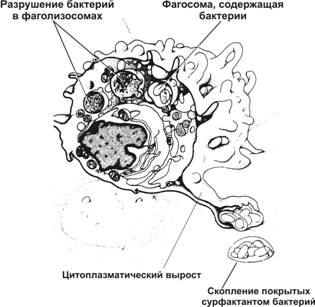
Сурфактант предотвращает непосредственный контакт пневмоцитов с вредными частицами и инфекционными агентами, попадающими в альвеолы с вдыхаемым воздухом. Циклические изменения поверхностного натяжения, происходящие при вдохе и выдохе, обеспечивают зависимый от дыхания механизм очистки. Обволакиваемые сурфактантом пылевые частицы транспортируются из альвеол в бронхиальную систему, из которой они удаляются со слизью. Сурфактант регулирует количество макрофагов, мигрирующих в альвеолы из межальвеолярных перегородок, стимулируя активность этих клеток. Бактерии, проникающие в альвеолы с воздухом, опсонизируются сурфактантом, что облегчает их фагоцитоз альвеолярными макрофагами (рис. 13-13).
Рис. 13-13. Альвеолярный макрофаг. Бактерии в альвеолярном пространстве покрываются плёнкой сурфактанта, что активизирует макрофаг. Клетка образует цитоплазматические выросты, с помощью которых фагоцитирует опсонизированные сурфактантом бактерии. [17]
Сурфактант в бронхиолах
Сурфактант присутствует в бронхиальном секрете, покрывая бронхиолярные экзокриноциты и реснитчатые клетки, и имеет тот же химический состав, что и альвеолярный сурфактант. Очевидно, сурфактант необходим для стабилизации дистальных воздухоносных путей.
Антигенпредставляющие клетки
Дендритные клетки и внутриэпителиальные дендроциты (рис. 13-14) относятся к системе мононуклеарных фагоцитов, именно они являются главными Аг-представляющими клетками лёгкого. Дендритные клетки и внутриэпителиальные дендроциты наиболее многочисленны в верхних дыхательных путях и трахее. С уменьшением калибра бронхов число этих клеток уменьшается. Как Аг-представляющие, лёгочные внутриэпителиальные дендроциты и дендритные клетки. экспрессируют молекулы MHC I и MHC II. Эти клетки имеют рецепторы Fc–фрагмента IgG, фрагмента C3bi комплемента, ИЛ2; синтезируют ряд цитокинов, включая ИЛ1, ИЛ6, фактор некроза опухоли a (TNFa); стимулируют T–лимфоциты, проявляя повышенную активность в отношении Аг, впервые оказавшихся в организме.
Дендритные клетки
Дендритные клетки находятся в плевре, межальвеолярных перегородках, перибронхиальной соединительной ткани, в лимфоидной ткани бронхов. Дендритные клетки, дифференцируясь из моноцитов, довольно подвижны и могут мигрировать в межклеточном веществе соединительной ткани. В лёгких они появляются перед рождением. Важное свойство дендритных клеток — их способность стимулировать пролиферацию лимфоцитов. Дендритные клетки имеют удлинённую форму и многочисленные длинные отростки, неправильной формы ядро и в изобилии — типичные клеточные органеллы. Фагосомы отсутствуют, поскольку дендритные клетки практически не обладают фагоцитарной активностью.
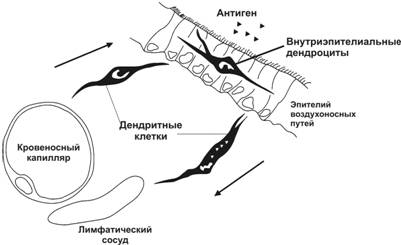
Рис. 13-14. Антигенпредставляющие клетки в лёгком. Дендритные клетки в паренхиму лёгких поступают с кровью. Часть из них мигрирует в эпителий внутрилёгочных воздухоносных путей и дифференцируется во внутриэпителиальные дендроциты. Последние захватывают Аг и переносят его в региональную лимфоидную ткань. Эти процессы контролируют цитокины. [17]
Внутриэпителиальные дендроциты
Внутриэпителиальные дендроциты присутствуют только в эпителии воздухоносных путей и отсутствуют в альвеолярном эпителии. Эти клетки дифференцируются из дендритных клеток., причём такая дифференцировка возможна только в присутствии эпителиальных клеток. Соединяясь цитоплазматическими отростками, проникающими между эпителиоцитами, внутриэпителиальные дендроциты образуют хорошо развитую внутриэпителиальную сеть. Внутриэпителиальные дендроциты морфологически сходны с дендритными клетками. Характерной чертой внутриэпителиальных дендроцитов является наличие в цитоплазме специфических электронно-плотных гранул в форме теннисной ракетки, имеющих пластинчатую структуру. Эти гранулы участвуют в захвате Аг клеткой для последующего его процессирования.
Макрофаги
Макрофаги составляют 10–15% всех клеток в альвеолярных перегородках. На поверхности макрофагов присутствует множество микроскладок (рис. 13-10, рис. 13-13). Клетки формируют довольно длинные цитоплазматические отростки, которые позволяют макрофагам мигрировать через межальвеолярные поры. Терминальную дифференцировку альвеолярных макрофагов стимулирует GM-CSF, повышая уровень транскрипционного фактора PU.1. Находясь внутри альвеолы, макрофаг с помощью отростков может прикрепляться к поверхности альвеолы и захватывать частицы. Альвеолярные макрофаги секретируют a1-антитрипсин — гликопротеин из семейства сериновых протеаз, защищающий эластин альвеол от расщепления эластазой лейкоцитов. Мутация гена a1-антитрипсина — причина врождённой эмфиземы лёгких (поражение эластического каркаса альвеол).
Пути миграции макрофагов
Нагруженные фагоцитированным материалом клетки могут мигрировать в различных направлениях: вверх по отделам ацинуса и в бронхиолы, где макрофаги попадают в слизистую плёнку, постоянно смещающуюся по поверхности эпителия по направлению к выходу из воздухоносных путей; внутрь — во внутреннюю среду организма, т.е. в межальвеолярные перегородки.
Функция
Макрофаги фагоцитируют микроорганизмы и пылевые частицы, попадающие с вдыхаемым воздухом, обладают антимикробной и противоопухолевой активностью, опосредованной кислородными радикалами, протеазами и цитокинами. У макрофагов лёгких антиген-представляющая функция выражена слабо. Более того, эти клетки вырабатывают факторы, ингибирующие функцию T–лимфоцитов, что снижает иммунный ответ.
В лёгких метаболизирует ряд биологически активных веществ.
Активация. Активация известна только в отношении ангиотензина I (обладает слабой сосудосуживающей активностью), который конвертируется в мощный вазоконстриктор — ангиотензин II. Конверсию катализирует ангиотензин-конвертирующий фермент, локализованный в эндотелиальных клетках капилляров альвеол.
Инактивация. Многие биологически активные вещества частично или полностью инактивируются в лёгких. Так, брадикинин инактивируется на 80% (при помощи ангиотензин-конвертирующего фермента). В лёгких инактивируются серотонин, простагландины PGE1, PGE2, PGE2a и норадреналин.
Плевра — серозная оболочка, выстилающая грудную полость (париетальная плевра) и покрывающая лёгкие (висцеральная плевра). Поверхность висцеральной и париетальной плевры выстлана мезотелием, расположенным на соединительнотканном слое. Последний представлен рыхлой соединительной тканью и содержит коллагеновые и эластические волокна, кровеносные и лимфатические сосуды, нервные волокна. Мезотелий покрыт тонким слоем жидкости общим объёмом 10–20 mл, сходной по составу с плазмой, но содержащей меньше белка. Жидкость поступает из капилляров плевры и удаляется через эпителий висцеральной плевры и лимфатические сосуды.
Кровоснабжение лёгких
Кровеносные сосуды лёгких относятся к малому и большому кругу кровообращения. Лёгочные сосуды составляют малый круг кровообращения и выполняют функцию газообмена между кровью и воздухом. Система бронхиальных сосудов обеспечивает питание лёгких и принадлежит большому кругу кровообращения. От правого предсердия отходит расположенный внутриперикардиально лёгочный ствол, делящийся на правую и левую лёгочные артерии, каждая из которых направляется к корню соответствующего лёгкого. Лёгочные артерии в лёгких делятся на долевые и сегментарные ветви. Последние дихотомически ветвятся и повторяют ветвления бронхиального дерева. Ветвь лёгочной артерии и бронх образуют бронхососудистый пучок. Артерии переходят в артериолы, которые распадаются на капилляры, оплетающие альвеолы. Через стенку этих капилляров происходит газообмен. Обогащённая кислородом кровь собирается в систему лёгочных вен.
Артерии
У взрослого человека в связи с низким сопротивлением току крови стенка артерий малого круга значительно тоньше, а просвет артерий, капилляров и вен шире, чем у аналогичного порядка сосудов большого круга. Артерии, вплоть до сосудов малого калибра (диаметром 0,5–1 мм), относятся к эластическому типу. Дистальнее они сменяются более мелкими артериями мышечного типа.
Венозная система
Венозная система отличается сложностью и большей вариабельностью, чем артериальная, причём вены не сопровождают все разветвления бронхиального дерева. Из сегментарных вен, часто расположенных между сегментами, формируются долевые вены, а затем — верхние и нижние лёгочные вены, раздельно впадающие в левое предсердие. Стенка вен тоньше стенки артерий и состоит из неупорядоченных эластических мембран и ГМК. У большинства вен — тонкие растяжимые стенки.
В лёгких имеется две сети лимфатических сосудов. Сосуды поверхностной сети лежат в висцеральной плевре. Самые крупные сосуды повторяют ход линий соединения междольковых перегородок с плеврой, мелкие образуют густую сеть. Глубокая сеть состоит из трёх групп сосудов: лежащие в стенках бронхов и бронхиол; сопровождающие ветви лёгочной артерии и анастомозирующие с сосудами первой группы; идущие в междольковых перегородках. В местах соединения висцеральной плевры и междольковых перегородок сосуды глубокой сети сообщаются с сосудами плевры. В целом отток лимфы по сосудам глубокой и поверхностной сетей осуществляется с периферии (от терминальных лимфатических сосудов, расположенных в окружающей бронхососудистые пучки рыхлой соединительной ткани) к центру, к корню лёгкого, в регионарные лимфатические узлы. В межальвеолярных перегородках лимфатические узлы отсутствуют.
Лёгкие иннервируются ветвями блуждающего нерва, грудных симпатических ганглиев и диафрагмального нерва, формирующими в воротах лёгких лёгочное сплетение. Последнее разделяется на переднее и заднее. Переднее лёгочное сплетение расположено на передней поверхности корня лёгкого. Ветви заднего лёгочного сплетения проходят вдоль задней стенки главных бронхов и задней поверхности корней лёгких. Ветви сплетений, вступая в сегменты лёгкого, формируют перибронхиальные и перивазальные сплетения, осуществляющие двигательную и чувствительную иннервацию. По ходу сплетений располагаются небольшие парасимпатические ганглии. Лёгочные нервные сплетения образуют связи с сердечным нервным сплетением: отходящие от них ветви участвуют в иннервации сердца.