Глава 4
Со времён Кёлликера и Лейдига (пятидесятые годы XIX века) ткани организма человека принято делить на четыре типа: эпителиальная, внутренней среды, мышечная, нервная. Структурно-функциональные единицы, образующие ткани, — гистологические элементы. Клетка — главная тканеобразующая единица и главный гистологический элемент. Другие гистологические элементы — симпласт, синцитий, компоненты межклеточного вещества — производные клетки.
Гистологические элементы — структурно-функциональные единицы, образующие ткани, органы и организм в целом (своего рода разные строительные кирпичики, из которых и конструируется организм человека). Таким образом, гистологические элементы — основные категории, которыми оперирует предмет гистология. Ткань, орган, система органов, организм — не механическая сумма гистологических элементов. Исходя из определения понятия ткань (“..система гистологических элементов, объединённых общей структурой, функцией и происхождением”), система гистологических элементов конструируется, обновляется и функционирует лишь при условии их взаимного узнавания, образования контактов между ними и информационных взаимоотношений, т.е. множества процессов, объединяемых термином межклеточные взаимодействия (термин межклеточные взаимодействия подразумевает взаимодействия между гистологическими элементами, а не только между клетками. Ещё точнее, взаимодействия между конкретными молекулами разных гистологических элементов). Гистологические элементы подразделяют на две основные категории — клеточные (клетка, симпласт, синцитий) и неклеточные (компоненты межклеточного вещества).
Клетка
Клетка — главный гистологический элемент. Главенствующее положение клеток среди гистологических элементов очевидно. Два других гистологических элемента клеточного типа — симпласт и синцитий — образуются из отдельных клеток. Разнообразные гистологические элементы неклеточного типа конструируются из макромолекул, синтезированных в клетках и секретированных в межклеточное вещество.
Симпласт
Симпласт — многоядерная структура, образованная при слиянии однотипных клеток. Примеры симпластов: поперечнополосатое мышечное волокно скелетной мускулатуры, остеокласт, гигантские клетки инородных тел.
Синцитий
Синцитий — структура, состоящая из клеток, соединённых цитоплазматическими мостиками.
· Синцитиотрофобласт — высокоплоидная многоядерная структура, образующаяся из клеток цитотрофобласта (см. рис. 3-22).
· Синцитий в сперматогенном эпителии формируют предшественники сперматозоидов, связанные между собой цитоплазматическими мостиками.
· Функциональный синцитий. Этот термин применяют по отношению к клеткам (например, рабочим кардиомиоцитам), связанным щелевыми контактами, что позволяет всей совокупности клеток функционировать как единое целое.
Тканевый матрикс
Тканевый матрикс (межклеточное вещество) состоит из основного вещества и содержащихся в нём волокон (коллагеновые, эластические и ретикулиновые). Структуры тканевого матрикса построены из молекул, вырабатываемых и секретируемых клетками. В свою очередь компоненты внеклеточного матрикса влияют на клетки (например, контролируют их пролиферацию и дифференцировку).
Жидкость
Организм человека в основном состоит из воды. Её содержание в общей массе тела постепенно уменьшается от 75% у новорождённых до 55% у пожилых людей.
Внутриклеточная жидкость (55% всей воды организма) содержит в низкой концентрации Na+, Cl–, HCO3–, в высокой концентрации K+, органические фосфаты (например, АТФ) и белок. Низкая концентрация Na+ и высокая концентрация K+ обусловлены работой Na+,K+-АТФазы, выкачивающей Na+ из клетки в обмен на K+.
Внеклеточная жидкость (45% всей воды организма).
· Интерстициальная жидкость (20% всей воды организма) в межклеточном пространстве тканей.
· Плазма (7,5% всей воды организма). Химический состав сходен с интерстициальной жидкостью (преобладающий катион — Na+, преобладающие анионы — Cl–, HCO3–), но концентрация белка в плазме выше.
· Кристаллизационная вода кости и хряща (15% всей воды организма).
· Трансклеточная жидкость (2,5% всей воды организма) содержится в пищеварительном тракте, жёлчи, мочевыделительной системе, внутриглазной и цереброспинальной жидкостях, а также в жидкости серозных полостей (плевра, брюшина, перикард).
Популяция клеток
По Джилберту и Лайта [154], популяция — группа клеток одного или нескольких типов, которая может быть охарактеризована в понятиях пространства и времени. Термин «клеточная популяция» применяют, по крайней мере, в двух значениях — в расширительном понимании и по отношению к популяциям по Леблону [57].
Клеточный тип
Эта концепция включает понятие клеточные фенотипы, а также пластичность и границы нормы клеточного типа. В организме человека насчитывают более 200 клеточных типов.
Определение. На первый взгляд, понятие клеточный тип очевидно. Ясно, что эритроциты, кардиомиоциты, нейроны и макрофаги относятся к разным типам клеток. Можно сказать, что клетки одинаковой морфофизиологической характеристики относятся к одному клеточному типу. В медицине всё чаще применяют понятие маркёр клеточного типа [в том числе в онкологии (например, маркёры лейкозов, рака предстательной и молочной желёз)] — отсюда следует необходимость строгого определения понятия клеточный тип. Клетки с идентичным набором разрешённых к экспрессии генов (вне зависимости от того, транскрибируются ли они) относятся к одному клеточному типу.
Дифферон
Дифферон (гистогенетический ряд) — совокупность клеточных форм, составляющих ту или иную линию дифференцировки.
Состав
В диффероне последовательно различают: стволовые клетки ® клетки–предшественницы ® зрелые клетки, достигшие состояния окончательной (терминальной) дифференцировки.
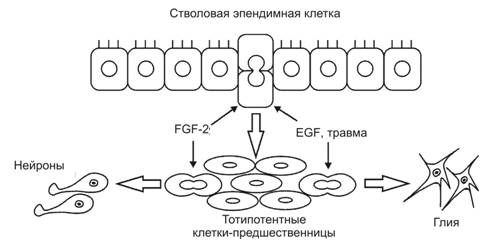
· Стволовые клетки — самоподдерживающаяся популяция клеток, способных дифференцироваться в нескольких направлениях и формировать различные клеточные типы. Так, стволовые эпендимные клетки ЦНС (рис. 4-1) дают начало разным нейронам и глиоцитам. Стволовые клетки обладают высокими пролиферативными потенциями, но, как правило, делятся редко.
Рис. 4-1. Стволовые эпендимные клетки делятся очень редко с образованием быстро пролиферирующих предшественников, которые мигрируют в субвентрикулярную зону и дифференцируются в нейроны и глию. Фактор роста фибробластов 2 (FGF2), фактор роста эпидермиса (EGF) и повреждение ткани стимулируют митозы стволовой нейральной клетки и её мультипотентных потомков. [17]
· Клетки–предшественницы. По мере дифференцировки их пролиферативные потенции постепенно уменьшаются. Выделяют наиболее раннюю стадию клеток–предшественниц — коммитированные, или полустволовые клетки.
· Зрелые клетки. Ими заканчивается гистогенетический ряд
Характеристика
Ограничение проспективных потенций. По мере дифференцировки происходит ограничение потенций клеток дифференцироваться в различных направлениях. Например, если клетка–предшественница может дифференцироваться в трёх направлениях, т.е. участвовать в образовании трёх клеточных типов, то её непосредственный потомок может дифференцироваться только в двух направлениях и т.д.
· Уровень дифференцировки. В диффероне уровень специализации клеток нарастает.
· Необратимость дифференцировки. В нормальных условиях переход от более дифференцированного состояния к менее дифференцированному невозможен, т.е. соблюдается принцип необратимости дифференцировки. Это свойство дифферона часто нарушается при новообразованиях (неоплазиях) — патологических разрастаниях клеток с нарушением контроля размножения и способности к построению тканевых и органных многоклеточных структур.
Стволовые клетки
Стволовыми клетками эмбриона, плода или взрослого организма считаются клетки, которые при определённых условиях способны длительное время воспроизводить себе подобные клетки и в течение жизни давать начало специализированным клеткам, образующих ткани и органы тела. Тотипотентная (лат. totus — целый, полный) клетка обладает потенциалом давать начало всем специализированным клеткам, формирующим ткани эмбриона. Например, зигота и бластомеры по всем признакам относятся к тотипотентным клеткам. Плюрипотентные (лат. plures — несколько, много) клетки дифференцируются в разные полипотентные клетки всех трёх зародышевых листков — экто-, энто- и мезодермы. Клетки внутренней клеточной массы бластоцисты относятся к плюрипотентным клеткам. Экспрессия Oct-4 (Octamer binding gene) в клетках внутренней клеточной массы и эпибласта поддерживает пролиферацию и препятствует дифференцировке клеток. При этом в трофобласте и образовавшихся во время гаструляции первичных зародышевых листках Oct-4 функционально не активен. Oct-4 принадлежит к семейству факторов экспрессии класса 5 POU (Pit, Oct и Unc), прямо взаимодействующих с промотором или энхансером гена-мишени, регулируя его транскрипцию. Oct-4 считается надёжным маркёром эмбриональных стволовых клеток. Поверхностно-клеточные антигены SSEA (Stage Specific Embryonic Antigen), TRA (tumor rejection antigen), Sca-1 (Stem cell antigen), CD34 и многие другие тканеспецифические клеточные маркёры (табл. 4-1) применяются на практике для идентификации и сортировки стволовых клеток, полученных из эмбриона или тканей взрослого организма, с помощью лазерного сортера.
Стволовые клетки эмбриона
Эмбриональная стволовая клетка
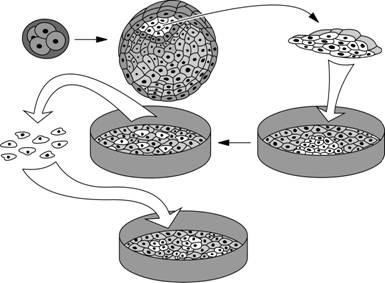
Из бластоцисты на 4–5 сутки развития методом иммунохирургии (при помощи антител, вызывающих повреждение клеток трофобласта) внутреннюю клеточную массу отделяют от трофэктодермы (рис. 4-2). Полученные клетки культивируют in vitro, с целью выделения чистой клеточной линии, способной формировать шарообразные скопления — эмбриоидные тела. С помощью специфических факторов роста можно направлять дифференцировку диссоциированных клеток эмбриоидных тел. Фактор роста гепатоцитов (HGF) и фактор роста нервов (NGF) стимулируют дифференцировку клеток всех трёх зародышевых листков. Ретиноевая кислота, фактор роста эпидермиса (EGF), морфогенетический белок кости 4 (BMP4) и щелочной фактор роста фибробластов (bFGF) индуцируют дифференцировку клеток, образующихся из эктодермы. Производные мезодермы можно получить путём воздействия на стволовые клетки трансформирующим фактором роста b1 (TGFb1) и активином-А.
Рис. 4-2. Получение эмбриональных стволовых клеток. Оплодотворённую in vitro яйцеклетку культивируют до стадии бластоцисты, образованной примерно 200–250 клетками, 30–34 из которых относятся к внутренней клеточной массе. Далее методом иммунохирургии трофэктодерму отделяют от внутренней клеточной массы. Полученные клетки выращивают на подложке из облучённых фибробластов эмбрионов мыши в культуральной среде, содержащей бычью сыворотку. Через серию многократных пассажей размножающихся клеток получают чистые клеточные линии, способные формировать шарообразные структуры — эмбриоидные тела. [143]
Эмбриональная половая клетка
Эмбриональные половые клетки выделяют из эмбриоидных тел, которые формируются при культивировании примордиальных половых клеток, полученных из половых валиков эмбриона на 5–9-й неделе развития. С помощью различных факторов роста из эмбриональных половых клеток получены специализированные клетки — производные всех трёх зародышевых листков.
Таблица 4-1. Стволовые клетки, полученные из эмбриона
|
Клеточный тип |
Маркёры |
Источник |
Потенциал |
|
Эмбриональная стволовая клетка |
SSEA-3 |
Внутренняя клеточная масса |
Плюрипотентная |
|
Эмбриональная половая клетка |
SSEA-1 |
Половые валики |
Плюрипотентная |
Клиническое применение. В будущем технология эмбриональных стволовых клеток может быть применена для лечения таких заболеваний, как инсулин-зависимый сахарный диабет (тип I, юношеский диабет), болезнь Паркинсона, несовершенный остеогенез, мышечная дистрофия Дюшенна, повреждения спинного мозга, сердечная недостаточность и др.
Для безопасной трансплантации стволовых клеток необходимо исключить любое возможное негативное воздействие трансплантированных клеток на организм реципиента. Подготовленные для трансплантации стволовые клетки должны иметь предсказуемые и воспроизводимые характеристики:
Ú активно размножаться с образованием достаточного количества клеток для восстановления утраченной ткани;
Ú дифференцироваться в требуемые клеточные типы;
Ú сохранять жизнеспособность;
Ú интегрироваться с клетками органа-реципиента;
Ú выполнять свойственные для органа-реципиента функции.
Стволовые клетки взрослого организма
Стволовые клетки взрослого организма выделены из красного костного мозга, периферической крови, пульпы зуба, спинного и головного мозга, кровеносных сосудов, скелетной мышцы, эпителия кожи и пищеварительной системы, роговицы и сетчатки глаза, печени и поджелудочной железы (табл. 4-2). Это полипотентные клетки, потомки которых дают начало ограниченному количеству типов коммитированных (унипотентных) клеток–предшественниц. К настоящему времени плюрипотентная стволовая клетка взрослого организма, способная дать начало всем клеточным типам организма, не обнаружена. Стволовые клетки трудно отличать от дифференцированных клеток в составе зрелых тканей. Стволовые клетки сложно идентифицировать и изолировать, а в культуре они имеют ограниченное количество митозов.
Пластичность (трансдифференцировка) стволовых клеток
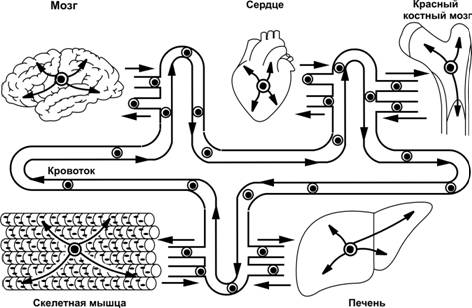
Стволовые клетки, полученные из одной ткани, могут давать начало специализированным клеткам других тканей. Так, стволовая кроветворная клетка может выходить из красного костного мозга, находиться в общем кровотоке и заселять разные органы, например, сердце, головной мозг, печень, скелетные мышцы (рис. 4-3). В зависимости от микроокружения стволовая кроветворная клетка может дифференцироваться в миобласты скелетной и сердечной мышечной ткани, гепатоциты, эндотелиальные клетки сосудов, нейроны, олигодендроциты, астроциты. Стволовая нейральная клетка, в свою очередь, может стать родоначальницей всех клеток крови и миобластов скелетной мышцы. Стволовая мезенхимная клетка красного костного мозга способна дифференцироваться в сердечные и скелетные мышечные клетки. Способность стволовых клеток к трансдифференцировке интенсивно изучается с целью их использования для восполнения дефектов тканей и органов. Не случайно поэтому открытие стволовых клеток признано третьим по значимости событием в биологии после расшифровки двойной спирали ДНК и программы "Геном человека".
Рис. 4-3. Пути миграций стволовых клеток взрослого организма. Тканеспецифические стволовые клетки в присущем микроокружении дифференцируются в клетки данной ткани. Но при этом стволовые клетки сохраняют способность к миграции. Они могут выходить в общий кровоток, после чего, стволовые клетки, либо возвращаются в исходное место, либо выселяются в другие ткани, где трансдифференцируются в специфичные для этой ткани стволовые клетки. [153]
Таблица 4-2. Стволовые клетки взрослого организма
|
Клеточный тип |
Маркёры |
Локализация/Источник |
Образуемые типы клеток |
|
Стволовая кроветворная клетка |
CD34, CD31, CD59, Sca-1, Thy1, Oct-4, Nanog, SOX2, FGF4 |
Красный костный мозг. В среднем удаётся
выделить одну стволовую кроветворную клетку на каждые 100 000 полученных
аспирацией клеток Пуповинная кровь и плацента. Возможно получить несколько миллионов стволовых кроветворных клеток, что недостаточно для трансплантации взрослому (требуется от 7 до 10 миллионов клеток на 1 кг массы тела), но может быть адекватным для трансплантации детям |
Эритроциты, лейкоциты (нейтрофилы, эозинофилы, базофилы, лимфоциты, моноциты), тромбоциты |
|
Стволовая мезенхимная клетка |
CD34, CD105, CD90, CD29, Sca-1, Thy-1, BMPR, SH3, SH4 |
Красный костный мозг |
Хондроциты, остеоциты, адипоциты, кардиомиоциты, скелетные мышечные волокна |
|
Стволовая нейрональная клетка |
CD133, ноггин, нестин |
Субвентрикулярная зона, зубчатая извилина гиппокампа |
Нейроны, астроциты, олигодендроциты |
|
Стволовая эндотелиальная клетка |
CD34, GATA2, Flk-1 |
Эндотелий сосудов |
Эндотелиальные клетки, кардиомиоциты |
|
Стволовая клетка скелетной мышцы (клетка-сателлит) |
М-кадгерин, Pax7, NCAM, c-Met |
Между базальной мембраной и плазмолеммой мышечных волокон |
Скелетные мышечные волокна |
|
Стволовая клетка эпидермиса |
b1–СЕ интегрина, цитокератины 5 и 14 |
Волосяной фолликул |
Кератиноциты эпидермиса, волосяного фолликула и волоса |
|
Стволовая клетка поджелудочной железы |
Нестин, ABCG2 (ATP-binding cassette transporter), c-kit |
Выводные протоки железы |
Эндокринные клетки островков Лангерханса |
|
Овальные клетки печени |
Thy-1, a-фетопротеин, g-глутамил транспептидаза, цитокератин 19, OC.2, OV-6 |
Жёлчные протоки |
Гепатоциты, эпителий жёлчных протоков |
Клиническое применение. Трансплантация стволовых кроветворных клеток производится при лечении ряда врождённых заболеваний крови (апластическая анемия, b-талассемия, серповидноклеточная анемия, лимфопролиферативный синдром, связанный с Х-хромосомой и др.) и гемобластозов (лимфом и лейкемий), при химиотерапии рака для поддержания пула полипотентных кроветворных клеток красного костного мозга.
клеточные популяции по Леблону
На основании способности к клеточному обновлению (в т.ч. путём пролиферации) Леблон выделил четыре категории клеточных популяций [57]: эмбриональная, статическая, растущая и обновляющаяся. Образующие популяцию клетки могут находиться на различных стадиях дифференцировки, фазах клеточного цикла, в различном функциональном состоянии.
Статическая популяция. Её составляет гомогенная группа клеток, не проявляющих митотической активности (например, нейроны).
Растущая популяция. В растущей популяции клетки делятся, митотическая активность постепенно затухает (например, гепатоциты, эпителий почки).
Обновляющаяся популяция. Обновляющаяся клеточная популяция характеризуется множественными митозами и быстрой гибелью клеток. При этом количество вновь образованных клеток слегка превышает клеточные потери (эпидермис, эпителий кишки, клетки тканей внутренней среды). При неоплазиях клеточная продукция намного превосходит гибель клеток, что обеспечивает быстрый рост опухоли.
Клеточный клон
Клеточный клон — группа клеток, происходящая от одной родоначальной клетки–предшественницы. Представление о клоне возникло в иммунологии. При попадании в организм Аг одна иммунокомпетентная клетка усиленно размножается, и образуется большое количество одинаковых клеток (клон), способных синтезировать АТ против этого Аг. Согласно клональной теории развития, структуры зародыша формируются из ограниченного количества клонов. Наконец, опухоли также развиваются как клоны, происходящие от одной трансформированной клетки.
При формировании ткани и в ходе её функционирования важную роль играют процессы межклеточной коммуникации — узнавание и адгезия.
Узнавание — специфическое взаимодействие клетки с другой клеткой или внеклеточным матриксом. В результате узнавания неизбежно развиваются следующие процессы: прекращение миграции клеток ® адгезия клеток ® образование адгезионных и специализированных межклеточных контактов ® формирование клеточных ансамблей (морфогенез) ® взаимодействие клеток между собой в ансамбле, с клетками других структур и молекулами внеклеточного матрикса.
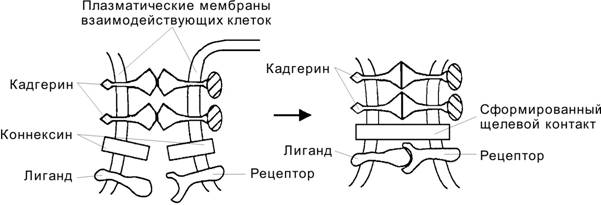
Адгезия — одновременно и следствие процесса клеточного узнавания, и механизм его реализации — процесс взаимодействия специфических гликопротеинов соприкасающихся плазматических мембран распознавших друг друга клеточных партнёров (рис. 4-4) или специфических гликопротеинов плазматической мембраны и внеклеточного матрикса. Если специальные гликопротеины плазматических мембран взаимодействующих клеток образуют связи, то это и означает, что клетки узнали друг друга. Если специальные гликопротеины плазматических мембран узнавших друг друга клеток остаются в связанном состоянии, то это поддерживает слипание клеток — клеточную адгезию.
Рис. 4-4. Молекулы адгезии в межклеточной коммуникации. Взаимодействие трансмембранных молекул адгезии (кадгерины) обеспечивает узнавание клеточных партнёров и их прикрепление друг к другу (адгезию), что позволяет клеткам-партнёрам формировать щелевые контакты, а также передавать сигналы от клетки к клетке не только при помощи диффундирующих молекул, но и путём взаимодействия встроенных в мембрану лигандов со своими рецепторами в мембране клетки-партнёра. [17]
Адгезия
Адгезия — способность клеток избирательно прикрепляться друг к другу или к компонентам внеклеточного матрикса. Клеточную адгезию реализуют специальные гликопротеины — молекулы адгезии. Исчезновение молекул адгезии из плазматических мембран и разборка адгезионных контактов позволяет клеткам начать миграцию. Узнавание мигрирующими клетками молекул адгезии на поверхности других клеток или во внеклеточном матриксе обеспечивает направленную (адресную) миграцию клеток. Иными словами, в ходе гистогенеза клеточная адгезия контролирует начало, ход и конец миграции клеток и образование клеточных сообществ; адгезия — необходимое условие поддержания тканевой структуры. Прикрепление клеток к компонентам внеклеточного матрикса осуществляют точечные (фокальные) адгезионные контакты, а прикрепление клеток друг к другу — межклеточные контакты.
Гистогенез и поддержание тканевой структуры
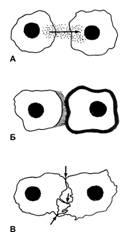
При образовании тканевых структур, а также в дифференцированных тканях клетки обмениваются информацией. Для этой цели существует несколько путей (рис. 4-5).
Рис. 4-5. Пути межклеточных информационных взаимодействий. А — при помощи диффундирующих молекулярных сигналов, Б — через внеклеточный матрикс, В — через щелевые контакты. [17]
Клеточная адгезия важна для образования клеточных сообществ практически всех типов тканей. Молекулы адгезии специфичны для каждого типа ткани. Так, E-кадгерин связывает клетки эмбриональных тканей, P-кадгерин — клетки плаценты и эпидермиса, N–CAM — клетки нервной системы и т.д. Адгезия позволяет клеточным партнёрам обмениваться информацией через сигнальные молекулы плазматических мембран и щелевые контакты. Удержание в соприкосновении при помощи трансмембранных молекул адгезии взаимодействующих клеток позволяет другим мембранным молекулам связываться между собой для передачи межклеточных сигналов.
Молекулы адгезии
Различают несколько групп молекул адгезии.
Кадгерины — трансмембранные гликопротеины, в присутствии Ca2+ обеспечивают межклеточную адгезию гомофильного типа (гомофильный вариант адгезии, предполагает взаимодействие клеток при помощи одинаковых молекул, встроенных в их клеточные мембраны).
Надсемейство иммуноглобулинов включает несколько форм молекул адгезии нервных клеток — (N–CAM), молекулы адгезии L1, нейрофасцин и другие. Они экспрессируются преимущественно в нервной ткани.
Макромолекулы внеклеточного матрикса: ламинин, фибронектин, витронектин и другие.
Точечный адгезионный контакт
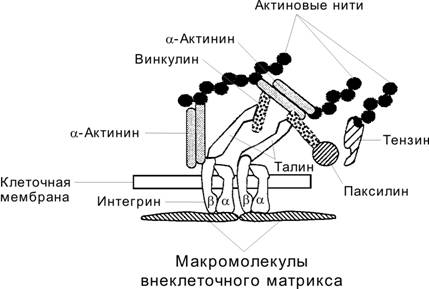
Прикрепление клеток к молекулам адгезии внеклеточного матрикса реализуют точечные (фокальные) адгезионные контакты (рис. 4-6). В образовании контакта участвуют трансмембранные рецепторы — интегрины, объединяющие внеклеточные и внутриклеточные структуры. Фокальный контакт содержит также винкулин, a–актинин, талин и другие белки. Характер распределения макромолекул адгезии во внеклеточном матриксе (фибронектин, витронектин) определяет место окончательной локализации клетки в формирующейся ткани.
Рис. 4-6. Адгезионный контакт. С белковыми макромолекулами внеклеточного матрикса (фибронектин, витронектин) взаимодействует трансмембранный белок-рецептор интегрин, состоящий из a- и b-цепей. На цитоплазматической стороне клеточной мембраны b–СЕ интегрина связывается с талином, взаимодействующим с винкулином. Последний связывается с a–актинином, образующим поперечные связи между актиновыми нитями. Кроме того, a–актинин взаимодействует с цитоплазматической частью b–СЕ интегрина. Подобным образом в единую систему объединяются макромолекулы внеклеточного матрикса, клеточная мембрана и элементы цитоскелета. [17]
Нарушения клеточной адгезии. Клетки способны к перемещению только после дезинтеграции адгезионных контактов. Подобную картину наблюдают при выселении злокачественных (трансформированных) клеток из опухоли и при их метастазировании, когда отдельные трансформированные клетки отделяются от опухоли, мигрируют и образуют новые опухолевые очаги (метастазы). Причиной этих осложнений служат дефекты генов, кодирующих гликопротеины клеточной адгезии. Например, метастазы и разрастания карцином желудка, эндометрия и яичника возникают вследствие нарушения адгезии опухолевых клеток, содержащих мутантный ген E-кадгерина, и экспрессии его дефектного продукта.
Межклеточные контакты — специализированные клеточные структуры, скрепляющие клетки для формирования тканей, создающие барьеры проницаемости и служащие для межклеточной коммуникации. Межклеточные контакты подразделяют на следующие функциональные типы: замыкающий, адгезионные, коммуникационные (проводящие).
Адгезионные межклеточные контакты механически скрепляют клетки между собой. К адгезионным относятся промежуточный контакт (опоясывающая десмосома, zonula adherens), десмосома (macula adherens), полудесмосома.
Промежуточный контакт
Мембраны соседних клеток разделены промежутком шириной 10-20 нм, заполненным аморфным или фибриллярным материалом. Электроноплотная пластинка на цитоплазматической стороне клеточной мембраны в пределах контакта содержит белки плакоглобин, винкулин, a–актинин и радиксин. В пластинку вплетены концы актинсодержащих микрофиламентов. В образовании контакта участвуют трансмембранные белки адгезии из семейства кадгерина.
Цепь молекулярных взаимодействий выглядит следующим образом: актин (примембранные микрофиламенты) — a-актинин — винкулин — Е-кадгерин (трансмембранный гликопротеин адгезии). Е-кадгерин в присутствии Ca2+ прочно связывает мембраны соседних клеток. Цепь молекулярных взаимодействий в промежуточном контакте, начиная с актина микрофиламентов и до винкулина включительно, аналогична таковой в точечном (фокальном) адгезионном контакте. Если винкулин фокального контакта взаимодействует с трансмембранными белками-рецепторами (интегрины), то в промежуточном контакте он связывается с E-кадгерином.
В промежуточном контакте E-кадгерин связан с актиновым цитоскелетом через периферические мембранные белки, в том числе a-, b- и g–катенины, a–актинин и винкулин. b-Катенин взаимодействует с цитоплазматическим участком E-кадгерина и связывает E-кадгерин с a–катенином, который связан непосредственно с F–актином. a–Актинин и винкулин — также F–актин связывающие белки, прямо связанные с a–катенином. Связь E-кадгерина с актиновым цитоскелетом через эти мембранные белки усиливает межклеточную адгезионную активность E-кадгерина.
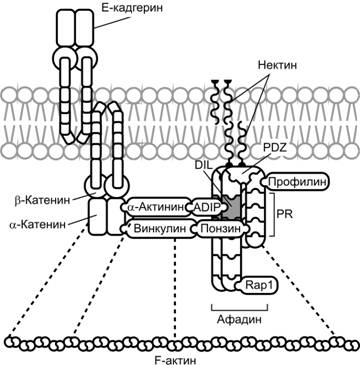
Другая молекула межклеточной адгезии, нектин, через белок афадин также связана с F–актином цитоскелета (рис. 4-7). Нектины (нектин-1, -2, -3 и -4) — Ca2+-независимые белки семейства иммуноглобулинов. Молекула нектинов имеет внеклеточный домен с тремя петлями, одним трансмембранным участком и цитоплазматическим участком. Молекула нектинов (за исключением -1b, -3g и -4) содержит мотив из 4 аминокислотных остатков (Glu/Ala-X-Tyr-Val) на COOH–конце, и этот мотив связывается с PDZ-доменом афадина.
Афадин (белок AF6) связывает нектин с актиновым цитоскелетом (рис. 4-7). Необходим для совместной организации нектина и E-кадгерина в промежуточном контакте. Афадин содержит два Ras-ассоциированных домена, forkhead-ассоциированный домен, DIL-домен, PDZ-домен и богатые пролином (PR) домены. F–актин связывается с участком молекулы, содержащим третий PR-домен. Афадин связан с цитоплазматическим участком нектина и, через F–актинсвязывающий домен, с F–актином. Дефект гена AF-6 (хромосомная аберрация) проявляется при острой миелоидной лейкемии.
ADIP (Afadin DIL domain-Interacting Protein, SSX2-SSX2-interacting protein) — широко распространённый белок адгезии, участвующий в организации и присутствующий в промежуточных адгезионных контактах, связывает афадин и a–актинин (рис. 4-7). Молекула содержит три биспиральных участка, состоит из 615 аминокислот, Mr 70,954 . ADIP объединяет комплексы нектин–афадин и E-кадгерин–катенин с участием a–актинина. Кроме того, ADIP участвует в организации актинового цитоскелета в области промежуточного контакта через афадин и a–актинин.
Рис. 4-7. Промежуточный контакт. Взаимодействие между системами нектин–афадин и кадгерин–катенин. Белок адгезии ADIP соединяет a–актинин с афадином. Афадин связывает нектин, понзин, ADIP через различные участки молекулы: нектин связывается с PDZ-доменом, понзин — с третьим богатым пролином (PR) доменом, ADIP связывается с DIL-доменом. Афадин напрямую может связывается с a–катенином. Таким образом, F–актин связывающий белок афадин может служить как опора для организации различных белков в опосредованном нектином межклеточном адгезионном контакте. [44]
Функция. Промежуточный контакт скрепляет не только мембраны соседних клеток, но и стабилизирует их цитоскелет, объединяя клетки с их содержимым в единую жёсткую систему.
Примеры: каёмчатый эпителий кишки (этот тип контактов известен как опоясывающая десмосома, т.к. контакт образует сплошной поясок вокруг клетки); секреторный эпителий (ацинозные клетки экзокринной части поджелудочной железы); вставочные диски в миокарде; эпендимные клетки ЦНС.
Десмосома
Десмосома (рис. 4-8) — самый распространённый и наиболее сложно организованный тип межклеточных контактов. Объединяет две формы соединений. Одна из них (цитоплазматическая пластинка) осуществляет связь промежуточных филаментов клетки с плазматической мембраной; вторая — связь плазматической мембраны с внеклеточным межмембранным материалом (десмоглеей) в пределах десмосомы.
Структура. Участки клеточных мембран, входящие в состав десмосомы, разделены слоем десмоглеи толщиной 20–30 нм. С внутренней стороны к плазматической мембране примыкает цитоплазматическая пластинка толщиной 10–40 нм с вплетёнными в неё промежуточными филаментами. В десмосомах всех клеточных типов присутствуют следующие белки: плакоглобин, десмоплакины, десмоглеины, десмоколлины.
· Плакоглобин (синонимы — DP3, PKGB, PDGB, g–катенин, десмоплакин III, DP3) — белок цитоплазматической пластинки десмосом и промежуточных контактов. Плакоглобин относится к семейству катенинов, образует комплекс с кадгерином, опосредуя связь с актиновыми филаментами. Плакоглобин также связывается с цитоплазматическим доменом десмоглеина I. Мутация гена плакоглобина приводит к развитию болезни (синдрома) Наксоса. Болезнь Наксоса — аутосомно-рецессивное расстройство, проявляющееся в неэпидермолитической ладонно-подошвенной кератодермии, курчавости волос и аритмогенной кардиомиопатии правого желудочка.
· Десмоплакин (DESP) — крупный белок десмосом, относящийся к семейству плакинов, содержит 17 повторов плектина и 2 повтора спектрина. NH3-Домен служит для закрепления в цитоплазматической пластинке и связывается с NH3-доменом плакофилина 1. COOH-Домен взаимодействует с промежуточными филаментами, обеспечивая их закрепление в цитоплазматической пластинке. Десмоплакин участвует также в организации комплекса кадгерин–плакоглобин. Дефекты десмоплакина являются причиной keratosis palmoplantaris striata II (ppks2) (полосчатая ладонно-подошвенная кератодермия II), а также синдрома Carvajal (кератодермия, расширенная кардиомиопатия левого желудочка, курчавые волосы). Дефекты десмоплакина — причина семейной аритмогенной дисплазии правого желудочка, характеризующейся частичной дегенерацией миокарда правого желудочка, его электрической нестабильностью и внезапной смертью.
· Десмоглеины (DSG1–DSG4) — Ca2+-связывающие гликопротеины семейства кадгеринов, участвуют во взаимодействии белков цитоплазматической пластинки с промежуточными филаментами.
à Десмоглеин 1 (DSG1). Дефект DSG1 — причина полосчатой ладонно-подошвенной кератодермии I (ppks1), аутосомно-доминантного заболевания, характеризующегося утолщением кожи на ладонях и подошвах, продольными гиперкератозными поражениями кожи ладоней, удлинением всех пальцев.
à Десмоглеин 3 (130 кД pemphigus vulgaris антиген) (DSG3) — аутоантиген аутоиммунного потенциально летального заболевания кожи pemphigus vulgaris (пузырчатки обыкновенной), при котором происходит генерализованное высыпание пузырей и образование обширных эрозированных поверхностей вследствие разрушения межклеточной адгезионных контактов аутоантителами против десмоглеина 3.
· Десмоколлины (DSC1–DSC4) — Ca2+-связывающие гликопротеины, относящиеся, наряду с десмоглеинами, к надсемейству кадгеринов; участвуют в формировании десмосом.
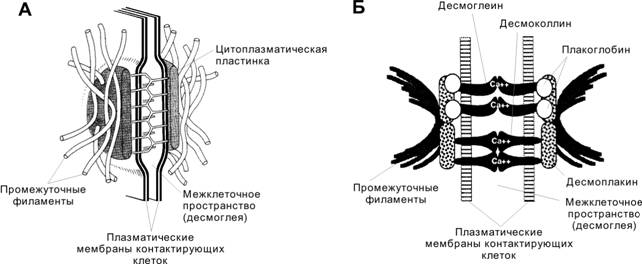
Рис. 4-8. Десмосома: строение (А) и организация (Б). Плазматические мембраны клеток разделены промежутком 20–30 нм, в котором находятся внемембранные части Ca2+-связывающих белков десмоглеина и десмоколлина. К внутренней (цитоплазматической) поверхности плазматической мембраны прилегает цитоплазматическая пластинка с вплетёнными в неё промежуточными филаментами. В состав этой пластинки входят десмоплакины, плакоглобин и часть молекулы десмоглеина. [17]
Цепь молекулярных взаимодействий (рис. 4-8). Молекулы образуют две линии связи: (1) плакоглобин (цитоплазматическая пластинка) — десмоглеин (Ca2+-связывающий белок в плазматической мембране одной клетки) — десмоглеин (Ca2+-связывающий белок в плазматической мембране другой клетки) — плакоглобин (цитоплазматическая пластинка); (2) десмоплакины (цитоплазматическая пластинка) — десмоколлин (Ca2+-связывающий белок в плазматической мембране одной клетки) — десмоколлин (Ca2+-связывающий белок в плазматической мембране другой клетки) — десмоплакины (цитоплазматическая пластинка).
Функция. Десмосомы поддерживают структурную целостность ткани, скрепляя клетки между собой. Десмосомы в комплексе с промежуточными филаментами придают ткани упругость и поддерживают в ней усилие натяжения.
Примеры. Десмосомы скрепляют клетки одного типа (кератиноциты, кардиомиоциты) и различных типов (тактильная клетка Меркеля–кератиноцит).
Полудесмосома обеспечивает прикрепление клетки к базальной мембране (например, кератиноцитов базального слоя эпидермиса, миоэпителиальных клеток). Полудесмосома, как и десмосома, содержит цитоплазматическую пластинку с вплетёнными в неё промежуточными филаментами.
В составе полудесмосомы присутствует по крайней мере 5 различных белков: рецептор a6b4-интегрина для ламинина-5; антигены буллёзного пемфигоида BP180 (Bullous Pemphigoid, или Bullous Pemphigoid Antigen) (BPAG2, или коллаген XVII типа) и BP230 (или BPAG1-e); CD151 и плектин.
· Интегрин a6b4 играет центральную роль в сборке полудесмосомы. Недостаточность a6b4-интегрина вследствие мутации гена, кодирующего или a, или b-субъединицу, вызывает одну из форм атрезии пилоруса, ассоциированной с epidermolysis bullosa (PA-JEB) (Pyloric Atresia associated Junctional Epidermolysis Bullosa), — болезнь, для которой характерна хрупкость кожи и образование многочисленных пузырей. При этом полудесмосомы рудиментарны или полностью отсутствуют.
· Коллаген типа XVII (BP180) (COL17A1) — трансмембранный белок, имеет участки для связывания с ламинином-5. Коллаген XVII содержит три a-цепи по 180 кД, образующие тример, содержащий участки тройной спирали коллагенового типа, состоящие из повторов типичных для коллагена последовательностей Gly-X-Tyr. Каждая a-цепь содержит внутриклеточный NH3-домен, состоящий из 466 аминокислот, трансмембранный участок и крупный COOH-домен из 1008 аминокислот. Коллаген XVII типа опосредует адгезию клеток к подлежащей базальной мембране. Мутация гена приводит к развитию буллёзного эпидермолиза (JEB).
· BP230 и плектин — цитоплазматические белки, относящиеся к семейству плакинов, участвующих в организации цитоскелета.
Плотный контакт
Плотный контакт формирует в различных клеточных слоях регулируемый барьер проницаемости, разделяющий разные по химическому составу среды (например, внутреннюю и внешнюю), обеспечивает полярное распределение мембранных молекул на апикальной и базолатеральной сторонах клеток. Примеры локализации плотных контактов: наружные клетки морулы и клетки трофобласта, каёмчатые клетки эпителия кишки, эндотелий капилляров, периневральные клетки, альвеолоциты, эпителиальные клетки почечных канальцев.
Структура
Плотные контакты представлены в виде лент, состоящих из цепочек округлых зон (бляшек) размером 10 нм и с расстоянием между центрами соседних бляшек примерно 18 нм. Белки, составляющие многомолекулярный комплекс плотного контакта, можно разделить на три группы.
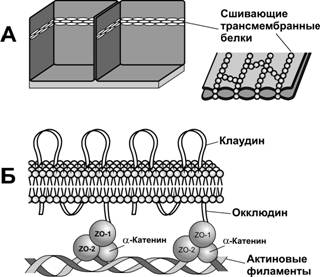
Интегральные белки, пересекающие апикальное межклеточное пространство и формирующие регулируемый барьер проницаемости. К ним относятся окклюдины, клаудины и молекула адгезионного контакта JAM (Junction Adhesion Molecule).
· Окклюдины (гены OCLN). Молекула белка проходит через плазмолемму 4 раза, образуя две внеклеточные петли и одну короткую цитоплазматическую петлю. Первая внеклеточная петля богата тирозином и глицином, соседняя петля содержит значительное количество заряженных аминокислотных остатков. COOH- и NH3-домены находятся в цитоплазматической части молекулы. Для COOH–конца характерно высокое содержание серина, треонина и тирозина, служащих мишенями для ряда протеин- и тирозинкиназ. Цитоплазматический домен окклюдина через белки zonula occludens ZO-1, ZO-2 и ZO-3 связан с актином кортикального цитоскелета (рис. 4-9). Окклюдины также участвуют в регуляции барьера параклеточной проницаемости.
Окклюдин в области плотного контакта находится в фосфорилированном состоянии. Дефосфорилированный окклюдин образует точечные локализации вдоль базолатеральной плазмалеммы. В стимулировании фосфорилирования окклюдина участвуют киназы — классическая протеинкиназа C (cPKC) и новая протеинкиназа C (nPKC), активированные диацилглицеролом.
· Клаудины (гены CLDN). Клаудины составляют семейство из 24 белков 20–27 кД. Молекула клаудина, как и окклюдина, проходит через плазмолемму 4 раза. Аминокислотный состав двух внеклеточных петель существенно варьирует у разных клаудинов, давая в результате широкий размах изоэлектрических точек. COOH-конец молекулы клаудинов, за исключением клаудина-12, заканчивается участком, связывающимся с PDZ-доменом ZO-1, ZO-2 и ZO-3.
Дефекты CLDN3 могут быть причиной ряда сердечно-сосудистых и опорно-двигательных аномалий, наблюдаемых при синдроме Williams-Beuren (WBS) (синдром делеции смежного гена, затрагивающий гены хромосомы 7q11.23).
· Молекула адгезионного контакта JAM (JAM-1–JAM-4) (F11R) относится к семейству иммуноглобулинов, Mr 43 кД. JAM-1 проходит сквозь плазмолемму один раз и образует 2 внеклеточных V-петли; первая петля, имеющая NH2-конец, взаимодействует со своим гомологичным партнёром JAM-1 соседней клетки. Короткий внутриклеточный COOH-конец, содержащий PDZ-мотив, связывается с PDZ3-доменом ZO-1 и с PDZ9-доменом белка MUPP-1 (Multi-PDZ domain Protein 1).
Белки бляшки плотного контакта, многие из которых экспрессируют PDZ-домены. PDZ-Домен (PSd/SAP90, Discs Large, ZO-1) представляет собой последовательность из 80–90 аминокислот, формирующую своего рода гидрофобный «желобок», с которым связываются COOH–концы белков-мишеней. Белки бляшки плотного контакта являются связующими звеньями между интегральными белками и актиновыми филаментами, а также выступают в роли адаптеров при мобилизации молекул цитозоля, участвующих в межклеточных взаимодействиях.
· PDZ-содержащие белки плотного контакта: белки ZO-1, ZO-2 и ZO-3, которые принадлежат семейству MAGUK (Membrane-Associated Guanylate Kinase); белки MAGI-1, MAGI-2, and MAGI-3 (Membrane-Associated Guanylyl kinase Inverted); MUPP-1; белки PAR-3 и PAR-6 (относящиеся к комплексу полярности PAR3/aPKC/PAR6); белок PALS1 (Protein Associated Lin-7) и белок PATJ (PALS1-Associated Tight Junction). Оба белка относятся к семейству комплекса полярности Crumbs/PALS1/PATJ; белки комплекса полярности Scrib/mDgl/mLgl (Scrib-(Vartul)/mammalian discs large/mLgl).
· Гетеротримерные G–белки образуют связи с ZO-1 и ZO-2. Как сигнальные молекулы участвуют в регуляции барьерной функции плотного контакта.
· Сингулин (CGNL) — белок, связанный с JAM-1, ZO-1, ZO-2, ZO-3 плотного контакта. Формирует поперечные связи с белками плотного контакта, участвуя в образовании пучков нитей F–актина.
Разнородная группа цитоплазматических и ядерных белков, включая регуляторные белки, онкосупрессоры, факторы транскрипции, которые взаимодействуют, прямо или опосредованно, с белками бляшки плотного контакта для координации таких различных функций, как регуляция параклеточной проницаемости, клеточная пролиферация, полярность, онкосупрессия.
· Симплекин (SYMPK) находится в составе бляшки плотного контакта совместно с ZO-1, а также присутствует в ядре. Участвует в процессинге пре-мРНК.
· ZONAB (ZO-1-Associated Nucleic Acid Binding Protein) связан с ZO-1 в плотном контакте. Является фактором транскрипции Y-box; связывая CDK4, ZONAB регулирует клеточную пролиферацию, также может регулировать экспрессию ErbB2.
· GEF-H1 (Guanine nucleotide Exchange Factor) — фактор, входящий в состав плотного контакта. Регулирует параклеточную проницаемость.
· Rab3b, Rab13 привлекаются в состав адгезионных комплексов, формируемых при межклеточных контактах; могут участвовать в транспорте пузырьков к участкам межклеточной адгезии.
· Sec6/Sec8 участвуют в транспорте пузырьков в области межклеточной адгезии.
Сборка
Сборка плотного контакта запускается гомофильным взаимодействием между E-кадгерином и нектином плазмолемм соседних клеток. Цитоплазматические домены нектина и E-кадгерина взаимодействуют между собой через комплекс афадин-b катенин, при этом афадин связан с COOH–концом нектина, а b катенин — с COOH–концом E-кадгерина. В ходе начальной стадии сборки JAM-1 соединяется с нектином (через белки, связанные с ZO-1 и афадином); по окончании сборки JAM-1 и нектин разделяются. В ходе сборки контакта с JAM-1 могут связываться и другие цитоплазматические белки (сингулин, Ca2+/кальмодулин-зависимая сериновая протеинкиназа CASK). В регуляции сборки плотных контактов участвуют белки комплексов полярности PAR-3/aPKC/PAR-6, Crumbs3/PALS1/PATJ и Scrib/mDlg/mLgl. Белки комплексов полярности также играют центральную роль в асимметричном клеточном делении, в установлении передне-задней полярности зародыша в эмбриогенезе, организации апикально-базальной полярности эпителиальных клеток.
Рис. 4-9. Плотный контакт. (А) Сшивающие трансмембранные белки образуют непроницаемые для молекул цепочки локальных соединений между смежными плазматическими мембранами. (Б) В верхней части смежные клетки соединены при помощи клаудина, в нижней — окклюдина, длинный внутриклеточный домен которого соединён с белками ZO. Через белки ZO трансмембранные белки связаны с актиновыми филаментами цитоскелета. [17]
Проницаемость
Некоторые лиганды влияют на проницаемость контакта. Например, в ответ на гистамин эндотелиальные клетки в результате взаимодействия актиновых и миозиновых филаментов отделяются друг от друга, приобретают округлую форму, увеличивая проницаемость сосуда.
Плотный контакт как мишень для инфекционных агентов
Вирусы
· Реовирусы. Прикрепление к клетке и эндоцитоз реовирусов запускается взаимодействием вирусного белка прикрепления s с JAM-1. Это взаимодействие стимулирует активацию ядерного фактора kB (NF-kB), что приводит к апоптозу клетки.
· Вирус Коксаки B и аденовирус. Рецепторы CAR этих вирусов локализованы базальнее плотного контакта. Первичная вирусная инфекция может развиться вследствие повреждения эпителия, при этом вирус получает доступ к своему CAR-рецептору. Белок вирусного капсида связывается с CAR-рецептором, после чего вирус проникает в клетку, где происходит его репликация.
· Аденовируса и папилломавирусные онкобелки. Онкобелки EF-ORF1 аденовируса и E6 папилломавируса связываются через PDZ-домены с MUPP-1 и MAGI-1. Аденовирусный белок EF-ORF1 связывается также с ZO-2. Такое связывание вызывает деградацию белков-онкосупрессоров в составе плотного контакта, чем объясняется, по крайней мере частично, онкогенный эффект вирусных белков.
Бактерии
· Энтеротоксин, продуцируемый Clostridium perfringens, ответственен за пищевые отравления. COOH-конец этого пептида связывается с клаудином-3 и клаудином-4, тогда как NH2-конец формирует поры в плазмолемме эпителиальных клеток кишечника.
· Helicobacter pylori прикрепляются к комплексу адгезионных контактов эпителиальных клеток. Направляющим на плотный контакт сигналом для H. Pylori служит бактериальный белок CagA. В молекулярные взаимодействия с H. Pylori вовлекаются ZO-1 и JAM-1, вследствие чего барьерная функция плотного контакта разрушается, изменяется форма клетки. Клиническими проявлениями такого взаимодействия, если оно длительно, являются язвенная болезнь и/или рак желудка.
Паразиты. Вдыхаемые аллергены домашней пыли могут вызывать приступы астмы. Цистеиновые и сериновые пептидазы, выделяемые живущими на частицах домашней пыли паразитами Dermatophagoides pteronyssinus (Der p 1), специфически расщепляют окклюдин и ZO-1, что ведёт к разрушению плотных контактов, снижению защитного барьера против вдыхаемых аллергенов и запуску иммунного ответа.
Коммуникационные контакты
Контакты этого типа — щелевые и синапсы.
Щелевой контакт
Щелевой контакт обеспечивает ионное и метаболическое сопряжение клеток. Плазматические мембраны клеток, образующих щелевой контакт, разделены щелью шириной 2–4 нм. Коннексон — трансмембранный белок цилиндрической конфигурации; состоит из 6 СЕ коннексина. Два коннексона соседних клеток соединяются в межмембранном пространстве и образуют канал между клетками (рис. 4-10). Канал коннексона диаметром 1,5 нм пропускает ионы и молекулы с Mr до 1,5 кД. Известно несколько коннексинов. Коннексин-43 экспрессируют кардиомиоциты, особенно важен при развитии миокарда. Коннексин-32 входит в состав щелевых контактов между гепатоцитами, шванновскими клетками. Коннексин-37 экспрессируют клетки различных тканей и органов, включая сердце, матку, яичник, эндотелиальные клетки кровеносных сосудов.
Рис. 4-10. Щелевой контакт. Шесть белковых СЕ в плазматической мембране образуют коннексон. При совмещении коннексонов смежных плазматических мембран формируется канал диаметром 1,5 нм, проницаемый для молекул с Mr не более 1,5 кД, участвующих в метаболической кооперации контактирующих клеток. [17]
Функция. Через щелевые контакты проходят низкомолекулярные вещества, регулирующие рост и развитие клеток. Для клеток нейроглии щелевой контакт имеет важное значение в регуляции уровня внутриклеточного Ca2+. Щелевые контакты обеспечивают распространение возбуждения — переход ионов между мышечными клетками миокарда и между ГМК.
Синапс
Синапс — специализированный межклеточный контакт, обеспечивает передачу сигналов с одной клетки на другую. Сигнальная молекула — нейромедиатор. Синапсы формируют клетки возбудимых тканей [нервные клетки между собой, нервные клетки и мышечные волокна (нервно-мышечный синапс)]. В синапсе различают пресинаптическую часть, постсинаптическую часть и расположенную между клетками синаптическую щель (см. подробнее в главе 8).
Гибель клеток
Развитие многоклеточного организма, формирование тканей и их функционирование предполагают наличие баланса между клеточной пролиферацией, клеточной дифференцировкой и гибелью клеток. Клетки гибнут в различных ситуациях, как нормальных, так и патологических. Так, массовую гибель клеток в раннем онтогенезе называют запрограммированной. Клетки, выполнившие свои функции, погибают в течение всей жизни организма. Наконец, клетки гибнут при повреждении и некрозе ткани, а также при различных заболеваниях, избирательно поражающих отдельные типы клеток (дегенерация).
Запрограммированная гибель клеток — естественный процесс массовой гибели клеток и элиминации целых клонов в ходе эмбрионального развития, гистогенеза и морфогенеза органов. В данном случае речь идёт о гибели клеток, не достигших состояния терминальной дифференцировки. Примером служит запрограммированная гибель нейробластов (от 25 до 75%) на определённых этапах развития мозга. Запрограммированная гибель клеток реализуется путём апоптоза.
Гибель клеток, выполнивших свою функцию, наблюдают при удалении клонов иммунокомпетентных клеток при иммунном ответе. Эозинофилы погибают после дегрануляции. Клетки, выполнившие свою функцию, гибнут путём апоптоза. Механизм гибели клеток, достигших состояния терминальной дифференцировки и выполнивших свою функцию, изучен недостаточно, но ясно, что он генетически детерминирован. Так, экспрессия гена fos служит маркёром терминальной дифференцировки и одновременно предшествует гибели клеток.
Некроз — гибель клеток вследствие повреждения. Некроз — всегда патологическая ситуация. Механизмы некроза иные, чем при апоптозе. Некроз индуцируется физическими и химическими агентами и характеризуется нарушением целостности мембран, набуханием клетки и ядра, неупорядоченной деградацией ДНК, деструкцией органелл и местным воспалением.
Дегенерация. При некоторых патологических состояниях наблюдают относительно избирательную гибель клеток, например, в нервной системе при боковом амиотрофическом склерозе (болезнь Шарко) и болезни Альцхаймера. Врождённая форма бокового амиотрофического склероза обусловлена мутацией гена Cu/Zn супероксиддисмутазы 1. Продукт дефектного гена не способен ингибировать ИЛ1b-конвертирующий фермент и образующийся ИЛ1b воздействует на двигательные нейроны и вызывает их апоптоз.
Апоптоз
Апоптоз — регулируемый процесс удаления ненужных, постаревших и повреждённых клеток. В отличие от некроза, смерть клетки при апоптозе является следствием экспрессии определённых генов, поэтому апоптоз — генетически запрограммированная гибель клетки. В противоположность некрозу, апоптоз энергозависим и требует синтеза РНК и белков. Апоптоз — феномен программируемой самодеструкции клеток, приводящей к их гибели и сопровождаемой характерными цитологическими признаками и молекулярными событиями (табл. 4-3). Часто термины «апоптоз» и «программируемая гибель клеток» используются как синонимы.
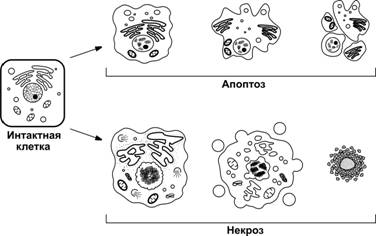
Морфологические проявления. Целостность плазматической мембраны при апоптозе не нарушается, хотя происходит ее выпячивание и "пузырение" за счет изменений цитоскелета. При апоптозе цитоплазма клетки уплотняется, конденсируется хроматин, ядро подвергается пикнозу с последующим кариорексисом. Характерным признаком апоптоза служит межнуклеосомное расщепление ядерной ДНК и формирование фрагментов кратных 200 п. н., при развитии другого пути апоптоза ДНК может расщепляться на более крупные фрагменты. Ядро в дальнейшем распадается на отдельные везикулы. На заключительных стадиях апоптоза наблюдается конденсация цитоплазмы (рис. 4-11). В конечной стадии апоптоза фрагментации подвергаются сами клетки с формированием так называемых апоптозных телец — фрагментов хроматина, окружённых мембраной. Клетки, вошедшие в апоптоз, и апоптозные тельца фагоцитируются макрофагами и гранулоцитами; фагоцитоз при этом не сопровождается местным воспалением.
Рис. 4-11. Морфологическая картина апоптоза и некроза клеток. При апоптозе клетка сморщивается, хроматин конденсируется, ядро перемещается на периферию. Наблюдается образование апоптозных телец, содержащих органеллы, цитозоль и фрагменты ядра. Апоптозные тельца быстро фагоцитируются и не возбуждают воспалительный ответ. При некрозе клетка набухает, от неё отделяются везикулы различных размеров, а затем клетка полностью разрушается, её содержимое поступает во внеклеточный матрикс и инициирует воспалительный ответ. [108]
Молекулярные сигналы апоптоза
Каспазы
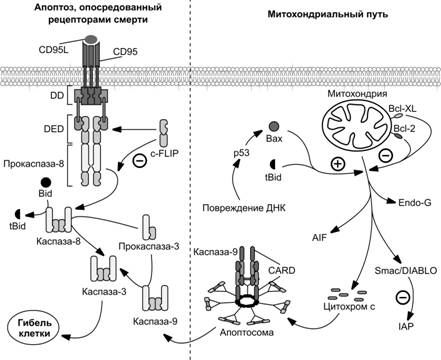
По определению апоптоз — каспаза-зависимый процесс. Англоязычное слово CASPASE — аббревиатура Cysteine Aspartate Specific proteASE. Программированная клеточная гибель предполагает активацию каспаз и обусловленную ими деградацию белка в клетке. Каспазы принадлежат семейству ICE-подобных (ICE — Interleukin-1b-Converting Enzyme) цистеиновых аспартат-специфичных протеаз, присутствующих в клетке в виде неактивных предшественников. Каспазы расщепляют белок за остатком аминокислоты аспартата (Asp). Этот сайт расщепления уникален для каспаз и протеазы гранзим В. В своих активных центрах каспазы содержат остатки аминокислоты цистеина. Идентифицировано не менее 14 изоформ каспазы, которые подразделяют на ингибиторные, эффекторные и воспалительные. Инициаторные (запускающие апоптоз) каспазы, такие как каспаза-8 и каспаза-9, расщепляют эффекторные каспазы, например каспазу-3, в результате чего эффекторные каспазы активируются (трансактивация) и расщепляют другие эффекторные каспазы или специфические белки, выполняющие в клетке конкретную функцию. Расщепление специфических белков неизбежно приводит к гибели клетки путём апоптоза. Следовательно, программируемая клеточная гибель характеризуется чередой протеолитических реакций, или протеолитическим каскадом последовательного расщепления и активации каспаз. Переход от предшественников каспаз (прокаспаз) к активным каспазам осуществляется двумя путями: в результате взаимодействия лигандов с рецепторами смерти (рис. 4-12) и в ходе митохондриального пути. При активации прокаспаза расщепляется на большую и малую субъединицы, которые в конечном счете объединяются с образованием тетрамера из двух малых и двух больших субъединиц (рис. 4-13). Активные каспазы представляют собой тетрамеры, состоящие из двух малых (~10 кД) и двух больших (~20 кД) субъединиц. И те, и другие образуются в результате расщепления прокаспаз. Каспазы содержат активный сайт, представленный консервативной последовательностью QACXG, который, в свою очередь, включает активный сайт с остатком цистеина. При активации прокаспазы расщепление происходит тоже по остатку аминокислоты аспартат (Asp). Ингибиторный продомен, который содержит DED (Death Effector Domain) или CARD (Caspase Recruitment Domain), отщепляется и удаляется.
Рис. 4-12. Сигналы смерти активируют внутриклеточные сигнальные пути. В цитоплазматической части молекулы рецептора смерти присутствуют домены смерти DD (Death Domain), которые образуют тетрамерные комплексы с эффекторными доменами смерти DED (Death Effector Domain) в составе предшественника инициаторной каспазы-8. Этот комплекс назван смерть-индуцирующим сигнальным комплексом DISC (Death-Inducing Signaling Complex). Находясь в составе данного комплекса, прокаспаза-8 приобретает способность к активации путём аутопротеолитического расщепления, в результате которого образуется активная инициаторная каспаза-8. Она имеет гетеротетрамерную структуру, т.е. состоит из двух малых и двух больших субъединиц. Каспаза-8 активирует эффекторные каспазы, которые вовлекаются в апоптоз. [108]
Рис. 4-13. Главные внутриклеточные пути реализации апоптоза: опосредованный рецепторами смерти и митохондриальный путь. Рецепторы смерти образованы молекулой CD95 (известной также, как Apo-1, или Fas) или представителями надсемейства рецепторов фактора некроза опухоли (TNF-R). Некоторые члены этого надсемейства имеют в составе молекулы домен смерти (DD). Этот домен участвует в белок–белковых взаимодействиях и обладает способностью связываться с адапторными белками, например белком FADD (Fas-Associated Death Domain). FADD содержит эффекторный домен смерти (DED). Аналогичный домен присутствует в составе неактивного профермента каспазы-8. При взаимодействии вышеупомянутых гомологичных доменов каспаза-8 связывается с FADD и формируется смерть-индуцирующий сигнальный комплекс DISC. В этом комплексе каспаза 8 олигомеризуется и активируется путём самопроцессинга. Имеющий гетеротетрамерную структуру активный фермент покидает DISC, в то время как продомен, содержащий два DED, остаётся в составе комплекса. Взаимодействие рецепторов смерти со своими лигандами CD–95L или фактором некроза опухоли a (TNFa) активирует каспазу-8. Опосредуемый рецепторами смерти апоптоз может быть заблокирован на уровне формирования DISC. Подобная картина, например, наблюдается в T–лимфоцитах. Для этой цели в геноме закодированы специальные белки, способные посредством собственных DED связываться с аналогичными доменами FADD и каспазы 8, препятствуя тем самым взаимодействию последних. Эти белки называются FLIPs (FLICE Inhibitory Proteins; FLICE — FADD–Like IL-1b-Converting Enzyme). [95]
Расщепляя белки, каспазы могут их активировать, например другие каспазы, ICAD (Inactive Caspase-Activated DNase), или инактивировать, например протеинкиназу PKB/Akt, Raf-1 и PARP-1 (Poly (ADP-Ribose) Polymerase). В целом действует правило: белки, поддерживающие апоптоз, активируются, а белки, поддерживающие выживание, инактивируются.
Участие каспаз в апоптозе
Каспаза-9, действуя на молекулы комплекса ядерной поры, увеличивает её размеры, в результате чего каспаза-3 и каспаза-7 проникают в ядро.
Проникшая в ядро каспаза-3 расщепляет ингибиторную субъединицу ICAD. Отщепленная от ICAD часть в виде CAD (Caspase-Activated DNase) «разрезает» ДНК между нуклеосомами.
Под действием каспаз в клетке, вступившей в апоптоз, появляются метки для последующего их распознавания и фагоцитоза. Подобной меткой служит принадлежащий к фосфолипидам внутреннего слоя плазматической мембраны фосфатидилсерин. В результате действия каспазы этот сигнал «выставляется» на поверхности клетки и распознаётся фагоцитом при участии молекулы CD14.
Каспазы индуцируют реорганизацию цитоскелета и дезинтеграцию клетки с образованием апоптозных телец.
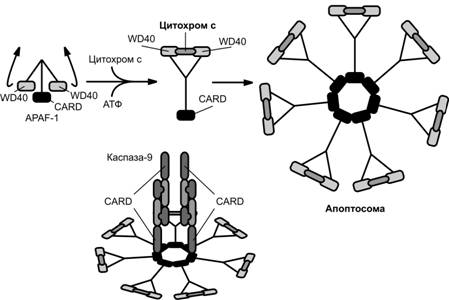
Митохондрии играют ключевую роль в апоптозе. В ходе апоптоза возрастает проницаемость мембран митохондрий, в результате чего из митохондрий выходят некоторые факторы, поддерживающие апоптоз. Среди них AIF (Apoptosis Inducing Factor), эндонуклеаза G, Smac/DIABLO (Second Mitochondrial Activator of Caspases/Direct IAP Binding protein with Low pI, IAP —Inhibitors of Apoptosis Proteins) и цитохром c. Выход цитохрома c из митохондрий наиболее значим, т.к. инициирует процесс сборки апоптосомы и последующую активацию инициаторной каспазы-9. Апоптосома собирается из трёх белков: адапторный белок APAF-1 (Apoptosis-Activating-Factor-1), прокаспаза-9 и цитохром c. В состав двух первых белков входит домен CARD (Caspase Recruitment Domain), обеспечивающий их взаимодействие (рис. 4-14). CARD присутствует в прокаспазах 2, 8, 9 и 10. Взаимодействие CARD инициирует аутокаталитический процессинг прокаспазы-9, в результате которого образуется активная инициаторная каспаза-9. Мишенью этой инициаторной каспазы, как и инициаторной каспазы-8, образованной в ходе опосредованного рецепторами смерти апоптозного пути, является прокаспаза-3. Последующая интенсивная активация эффекторных каспаз приводит к протеолизу практически во всех клеточных компартментах и смерти клетки.
Рис. 4-14. Формирование апоптосомы. Конформационная перестройка молекулы APAF-1, осуществляемая под влиянием цитохрома c и АТФ, позволяет собрать гептамерную колесоподобную структуру, называемую апоптосомой. С CARD доменами молекул APAF-1, расположенными в центральной части и образующими ступицу колеса апоптосомы, через аналогичные домены присоединены молекулы прокаспазы-9, которые в результате подобного взаимодействия активируются с последующим отщеплением димеров и сборкой активной каспазы-9. [108]
Важное звено в реализации митохондриального пути апоптоза представлено белками семейства Bcl-2 (B-Cell Lymphoma). Оно включает про- (Bax, tBid) и антиапоптозные (Bcl-2, Bcl-XL) белки. Повреждение ДНК через транскрипционный фактор p53 смещает равновесие в пользу усиления действия проапоптозных факторов.
Разрушение/повреждение ДНК
Апоптоз запускается при повреждении ДНК. Важным регулятором этого процесса служит транскрипционный фактор — белок p53, который кодируется геном супрессором опухоли. Специальный белковый фактор MDM2 ингибирует активность p53 в ходе процесса убиквитинизации последнего. При повреждении ДНК фактор MDM2 угнетается, и это приводит к активации p53. Транскрипционный фактор p53 индуцирует транскрипцию многих генов, включая Bax, что поддерживает апоптоз за счет выхода из митохондрий цитохрома c и формирования апоптосом.
Ядерный фермент PARP-1 (Poly (ADP-Ribose) Polymerase) контролирует в клетке выбор между тремя состояниями: репарация ДНК, некроз или апоптоз. В процессе репарации ДНК PARP-1 катализирует присоединение полимера АДФ-рибозы из 50–200 остатков к ядерным белкам, таким как гистоны. Повышенная активность PARP-1 вызывает истощение NAD+ и последующее снижение уровня АТФ. Это приводит к ослаблению работы ионных насосов, нарушению осморегуляции и некрозу клетки. С другой стороны, истощение NAD+ в митохондриях индуцирует выход из них в цитоплазму через образованные поры проницаемости флавопротеина AIF (Apoptosis Inducing Factor), который транслоцируется в ядро, расщепляет ДНК на фрагменты ~50 kb и в конечном итоге приводит к апоптозу.
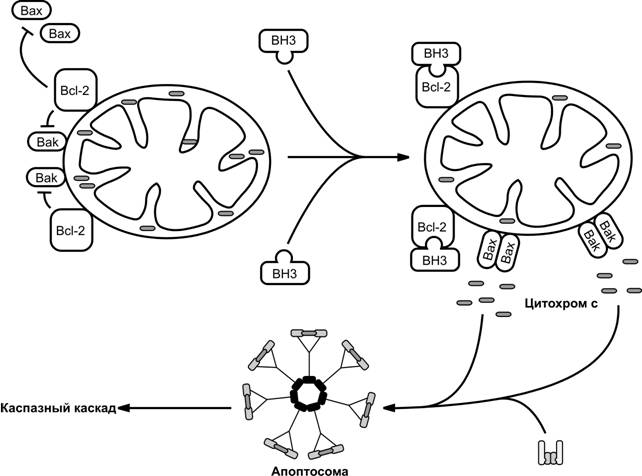
Семейство Bcl-2 объединяет множество белков-регуляторов апоптоза, обладающих как про-, так и антиапоптозной активностью. Белки этого семейства содержат BH (Bcl-2 Homology) домены: BH1, BH2, BH3 и BH4. Все белки семейства Bcl-2 участвуют в регуляции проницаемости мембраны митохондрий. Проапоптозные белки (Bax, Bak and BAD) содержат все 4 известные BH домены. Антиапоптозные белки (Bcl-2, Bcl-xL и Bcl-w) включают в свой состав не все BH домены. Так, проапоптозный белок Bid (BH3-Interacting Domain death agonist) и его усечённая форма tBid (truncated) образованы только BH3 доменом. Проапоптозные белки способствуют образованию пор перехода проницаемости в мембране митохондрий и таким образом поддерживают проницаемость для ряда факторов, активирующих апоптоз и выходящих из митохондрий в цитозоль (рис. 4-15). Антиапоптозные белки, наоборот, блокируют проницаемость мембраны митохондрий.
Рис. 4-15. Митохондрии — ключевой регулятор молекулярного механизма апоптоза. В жизнеспособной клетке проапоптозные (содержащие только домен BH3, Bax, Bak,) и антиапоптозные (Bcl-2) представители семейства белков-регуляторов апоптоза Bcl-2 находятся в антагонистических взаимоотношениях. В ответ на действие апоптозного стимула представители семейства Bcl-2, содержащие только домен BH3, активируются в результате усиления транскрипции (Bax, Noxa, Puma), внутриклеточного перераспределения (Bim, Bmf), дефосфорилирования (Bad) или протеолиза (Bid). Содержащие только домен BH3 активированные белки сдерживают действие антиапоптозное представителей семейства Bcl-2. Кроме того, они могут прямо индуцировать конформационные превращения белков Bax и Bak, которые приобретают способность олигомеризоваться и встраиваться в митохондриальную мембрану, формируя поры или ассоциируясь с комплексом поры перехода проницаемости. В результате из внутренней мембраны митохондрий в цитозоль выходят проапоптозные факторы, такие как цитохром с, который участвует в сборке апоптосом и последующей активации каспазного каскада. [108]
Существуют разные представления о механизме регуляции проницаемости мембраны митохондрий со стороны белков-регуляторов апоптоза из семейства Bcl-2. Согласно одному из них, белки этого семейства образуют гомо- или гетеродимеры. В процессе димеризации участвует BH3 домен. Гетеродимеризация про- и антиапоптозных членов этого семейства подавляет активность проапоптозных белков. Согласно другому представлению, белки семейства Bcl-2 способны формировать ионные каналы, что показано для Bcl-xL, Bcl-2 и Bax на искусственных липидных мембранах. Наиболее популярно представление о формировании белками из семейства Bcl-2 пор перехода проницаемости. Эти каналы неселективны, через них могут транспортироваться любые молекулы с Mr менее 1,5 кД. Предполагается, что белок Bcl-2 ингибирует открытие пор перехода проницаемости, а проапоптозные белки, например Bax и Bak, поддерживают их проницаемость для цитохрома c и AIF. Существует предположение, что канал, сформированный проапоптозным белком Bax, позволяет цитохрому c выходить из митохондрий в цитозоль. Согласно другому предположению, этот канал позволяет молекулам воды проникать внутрь митохондрии и вызывать разрывы наружной мембраны. Вместе с тем имеются данные о том, что выход цитохрома c из митохондрий может осуществляться не через поры.
Некоторые белки семейства Bcl-2 могут регулировать апоптоз, не влияя на процесс проницаемости митохондриальной мембраны. Одно из предположений об антиапоптозной роли белка Bcl-xL основано на данных о возможности его связывания с адапторным белком APAF-1. Происходящее при этом секвестрирование APAF-1 снижает вероятность образования апоптосом и вступление клетки в апоптоз.
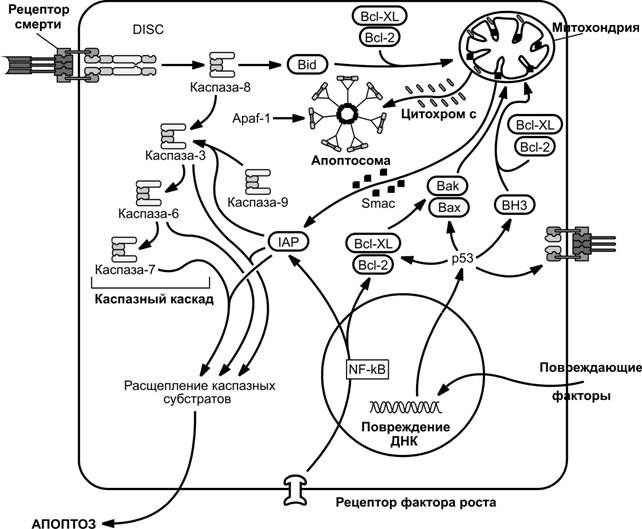
Рассмотренные выше ключевые молекулярные события апоптоза сведены в итоговую схему, которая поможет сформировать представление о всем процессе в целом (рис. 4-16).
Рис. 4-16. Основные молекулярные события при апоптозе. Апоптоз индуцируется различными вне- и внутриклеточными сигналами. Внеклеточными сигналами могут быть специальные сигналы смерти (TNFa, FasL, TRAIL), которые, будучи лигандами, взаимодействуют со своими рецепторами смерти (TNFR1, Fas, DR5). Вызывающие смерть внеклеточные сигналы могут действовать на клетку не только через специальный рецепторный вход. Ими могут быть различные повреждающие факторы, облучение, стресс, действие фармакологических препаратов, вирусов и др. Опосредованная рецепторами смерти разновидность апоптоза инициируется сборкой смерть-индуцирующего сигнального комплекса DISC, который контролирует активацию инициаторной каспазы-8. Активированная каспаза-8 запускает каспазный каскад, действуя на эффекторные каспазы-3, -6 и -7, которые, в свою очередь, расщепляют многочисленные белки во всех компартментах клетки. Это повсеместное расщепление белков лежит в основе морфологических и биохимических сдвигов, характеризующих апоптоз. В некоторых клеточных системах подобные сдвиги являются достаточными для запуска апоптоза [сигнальный путь (апоптоз) 1 типа]. В других клеточных сиcтемах для вступления клетки в апоптоз сигнал из DISC должен быть усилен путём протеолитической активации инициаторной каспазой-8 содержащего только BH3-домен белка Bid с последующим вовлечением в процесс митохондриального сигнального пути [сигнальный путь (апоптоз) 2 типа]. На этом пути развития событий ключевым звеном является выход цитохрома c из митохондрий в цитозоль, который в присутствии АТФ запускает сборку апоптосомы из белка Apaf-1. Формирование апоптосомы обеспечивает процесс активации другой инициаторной каспазы —каспазы-9 с последующим включением каспазного каскада, начиная с каспазы-3. Другим проапоптозным фактором, выходящим как и цитохром c из митохондрий, является Smac/DIABLO (Second Mitochondrial Activator of Caspases/Direct IAP Binding protein with Low pI). Этот белок выходит из митохондрий через поры перехода проницаемости и подавляет активность ингибиторов апоптозных белков IAP (Inhibitors of Apoptosis Proteins) (c-IAP, XIAP, сурвивин и др.). IAP, такие как ливин, прямо подавляют активность определённых каспаз, например каспазы-3 и -8. Экспрессия IAP возрастает при действии на клетку через свои рецепторы факторов роста, что поддерживает выживание клеток. Этот эффект опосредуется увеличением экспрессии транскрипционного фактора NF-kB, который также поддерживает экспрессию антиапоптозных белков из семейства Bcl-2 (Bcl-2, Bcl-XL). Эти белки угнетают действие других белков, принадлежащих к семейству Bcl-2, но обладающих проапоптозным действием (Bax, Bak, Noxa, Puma). Апоптозные стимулы, возникающие в самой клетке, часто происходят из ядра вследствие повреждения ДНК при облучении, применении лекарств, стрессе. В большинстве случаев повреждение ДНК сопровождается активацией транскрипционного фактора p53, который поддерживает экспрессию проапоптозных членов семейства белков-регуляторов апоптоза Bcl-2 и рецепторов смерти и угнетает экспрессию противоапоптозных белков Bcl-2 и Bcl-XL. Кроме ядра и митохондрий в апоптозе участвуют и другие органеллы. Так, эндоплазматическая сеть и лизосомы также вовлечены в апоптоз. [108]
Значение и некоторые примеры апоптоза в норме
· Запрограммированная гибель клеток в раннем онтогенезе (имплантация, эмбриогенез, органогенез).
· Удаление клеток в обновляющихся клеточных популяциях.
· Гибель клеток иммунной системы, В- и T–лимфоцитов при дефиците цитокинов, гибель аутореактивных T–клеток в тимусе.
· Гибель клеток в ходе гормон-зависимых процессов: отторжение эндометрия во время менструального цикла, атрезия фолликулов в яичниках в менопаузе и регрессия молочной железы после прекращения лактации.
Значение и некоторые примеры апоптоза в условиях патологии
· Дисрегуляция апоптоза является причиной многих заболеваний. Недостаток апоптоза приводит к возникновению опухолевого роста, избыток апоптоза приводит к потере клеток.
· Гибель клеток, вызванных действием цитотоксических T–клеток, например, при отторжении трансплантата и болезни «трансплантат против хозяина».
· Повреждении клеток при некоторых вирусных заболеваниях, например, при вирусном гепатите, когда фрагменты клеток, погибших путём апоптоза, обнаруживаются в печени (тельца Каунсильмана).
· Гибель заражённых вирусом клеток.
Таблица 4-3. Сравнительные признаки апоптоза и некроза
|
Признак |
Апоптоз |
Некроз |
|
Гибель клетки |
Программируемая |
Спонтанная |
|
Объём клетки |
Уменьшение |
Увеличение, набухание и лизис клеток |
|
Регулируемость процесса элиминации клетки |
Да |
Нет |
|
Фрагментация клеток на везикулы с внутриклеточным содержимым |
Да |
Нет |
|
Зависимость от наличия АТФ |
Да |
Нет |
|
Образование активных форм кислорода |
Да |
Нет |
|
Активация каспаз |
Да |
Нет |
|
Распространенность |
Одиночная клетка |
Группа клеток |
|
Воспалительный ответ |
Нет |
Обычно есть |
|
Ядро |
||
|
Распад на части |
Да |
Нет |
|
ДНК |
Внутриядерная конденсация с разрывом нитей в межнуклеосомных участках |
Диффузная локализация в некротизированной клетке |
|
Конденсация хроматина по периферии ядра |
Да |
Нет |
|
Плазматическая мембрана |
||
|
Целостность мембраны в поздней стадии процесса |
Сохранена |
Нарушена |
|
Сморщивание мембраны |
Да |
Нет |
|
Переход фосфатидилсерина из внутреннего монослоя мембраны в наружный |
Да |
Нет |
|
Митохондрии |
|
|
|
Увеличение объёма |
Да |
Да |
|
Выход цитохрома с в цитоплазму |
Да |
Нет |
|
Лизосомы |
Интактные |
Высвобождение ферментов |
Классификация тканей